15 CÂU HỎI
Phản ứng thuận nghịch là phản ứng
A. chỉ xảy ra theo một chiều nhất định.
B. xảy ra giữa hai chất khí.
C. xảy ra theo hai chiều ngược nhau trong cùng điều kiện.
D. có phương trình hoá học được biểu diễn bằng mũi tên một chiều.
Nhận xét nào sau đây không đúng?
A. Trong phản ứng một chiều, chất sản phẩm không phản ứng được với nhau tạo thành chất đầu.
B. Trong phản ứng thuận nghịch, các chất sản phẩm có thể phản ứng với nhau để tạo thành chất đầu.
C. Phản ứng một chiều là phản ứng luôn xảy ra không hoàn toàn.
D. Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều trái ngược nhau trong cùng điều kiện.
Yếu tố nào sau đây luôn luôn không làm dịch chuyển cân bằng của hệ phản ứng?
A. Nhiệt độ.
B. Áp suất.
C. Nồng độ.
D. Chất xúc tác.
Phản ứng nào sau đây là phản ứng thuận nghịch?
A. Mg + 2HCl → MgCl2 + H2.
B. 2SO2 + O2 2SO3.
C. C2H5OH + 3O2 2CO2 + 3H2O.
D. 2KClO3 2KCl + 3O2
Trong các phát biểu sau đây, phát biểu nào đúng khi một hệ ở trạng thái cân bằng?
A. Phản ứng thuận đã dừng.
B. Phản ứng nghịch đã dừng.
C. Nồng độ chất tham gia và sản phẩm bằng nhau.
D. Nồng độ của các chất trong hệ không đổi.
Các yếu tố có thể ảnh hưởng đến cân bằng hoá học là
A. nồng độ, nhiệt độ và chất xúc tác.
B. nồng độ, áp suất và diện tích bề mặt.
C. nồng độ, nhiệt độ và áp suất.
D. áp suất, nhiệt độ và chất xúc tác.
Cho phản ứng hoá học sau:
Yếu tố nào sau đây cần tác động để cân bằng trên chuyển dịch sang phải?
A. Thêm chất xúc tác.
B. Giảm nồng độ N2 hoặc H2.
C. Tăng áp suất.
D. Tăng nhiệt độ.
Hằng số cân bằng KC của một phản ứng thuận nghịch phụ thuộc vào yếu tố nào sau đây?
A. Nồng độ
B. Nhiệt độ
C. Áp suất
D. Chất xúc tác
Biểu thức tính hằng số cân bằng (KC) của phản ứng tổng quát: aA + bB cC + dD là
A.
B.
C.
D.
Xét cân bằng sau:
Nếu tăng nồng độ SO2(g) (các điều kiện khác giữ không đổi), cân bằng sẽ chuyển dịch theo chiều cao?
A. Chuyển dịch theo chiều nghịch.
B. Chuyển dịch theo chiều thuận.
C. Có thể chuyển dịch theo chiều thuận hoặc nghịch tùy thuốc vào lượng SO2 thêm vào.
D. Không thay đổi.
Cho phản ứng hoá học sau: H2(g) + Br2(g) 2HBr(g)
Biểu thức hằng số cân bằng (KC) của phản ứng trên là
A. .
B. .
C. .
D. .
Biểu thức nào sau đây là biểu thức hằng số cân bằng (KC) của phản ứng:
C(S) + 2H2 (g) CH4(g)?
A.
B.
C.
D.
Viết biểu thức tính hằng số cân bằng của phản ứng sau:
CH3COOH(l) + C2H5OH(l) CH3COOC2H5(l) + H2O(l)
A. 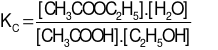
B. 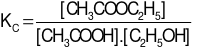
C.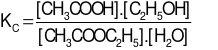
D. 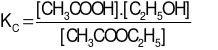
Biểu thức tính hằng số cân bằng của phản ứng: CaO(s) + CO2(g) CaCO3(s) là
A. 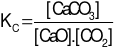
B. 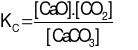
C. 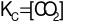
D. 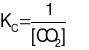
Xét cân bằng:
(1) H2(g) + I2(g) 2HI(g) KC(1)
(2)  H2(g) +
H2(g) +  I2(g) HI(g) KC(2)
I2(g) HI(g) KC(2)
Mối quan hệ giữa KC(1) và KC(2) là
A. KC(1) = KC(2).
B. KC(1) = (KC(2))2.
C. 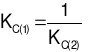
D.