Giải SBT Hóa học 12 CTST Bài 12: Thế điện và nguồn điện hóa học có đáp án
25 câu hỏi
Trong pin điện hoá, quá trình oxi hoá
A. chỉ xảy ra ở cực dương. B. chỉ xảy ra ở cực âm.
C. xảy ra ở cả hai cực. D. không xảy ra ở cả hai cực.
Cho pin điện hoá Fe – Cu. Biết EFe2+/Feo=−0,44V và ECu2+/Cuo=0,34V.Sức điện động chuẩn của pin điện hoá Fe – Cu là
A. 1,66V. B. 0,1V. C. 0,78V. D. 0,92V.
Cho pin điện hoá Al – Pb. Biết EAl3+/Alo=−1,66V .và EPb2+/Pbo=−0,13V. Sức điện động của Pin điện hoá Al – Pb là
A. 1,79V. B. -1,79V. C. -1,53V. D. 1,53V.
Cho E0Pin (Ni – Cu) = 0,59V và ECu2+/Cuo=0,34V . Thế điện cực chuẩn của cặp oxi hoá – khử Ni2+/Ni (ENi2+/Nio) là
A. 0,34V. B. 0,35 V. C. -0,35V. D. -0,25V.
Cho pin điện hoá Zn– Fe, xác định các chất ion đóng vai trò là chất khử, chất oxi hoá trong pin:
A. Zn là chất khử, Fe2+ là chất oxi hoá.
B. Zn là chất oxi hoá, Fe2+ là chất khử.
C. Zn2+ là chất khử, Fe là chất oxi hoá.
D. Zn2+ là chất oxi hoá, Fe là chất khử.
Dãy các kim loại được sắp xếp theo chiều tính khử giảm dần là
A. K > Ca > Mg > Cu > Fe > Al.
B. Ca > K > Mg > Cu > Fe > Al.
C. K > Ca > Mg > Al > Fe > Cu.
D. Ca > K > Cu > Mg> Fe > Al.
Dãy các ion được sắp xếp theo chiều tính oxi hoá giảm dần là
A. K+ > Mg2+ > Al3+ > Fe2+ > Cu2+.
B. Fe2+ > Cu2+ > K+ > Mg2+ > Al3+.
C. Cu2+ > Fe2+ > K+ > Mg2+> Al3+.
D. Cu2+ > Fe2+ > Al3+ > Mg2+> K+.
Cho pin điện hoá Zn-Cu. Quá trình xảy ra ở cực dương của pin là
A. Zn2+ + 2e → Zn.
B. Cu2+ + 2e → Cu.
C. Zn → Zn2+ + 2e.
D. Cu → Cu2+ + 2e.
Cho pin điện hoá Al-Pb. Quá trình xảy ra ở cực âm của pin là
A. Al3+ + 3e →Al.
B. Pb2+ + 2e →Pb.
C. Al → Al3+ + 3e.
D. Pb → Pb2+ + 2e.
Cho các kim loại: Al, Ag, Fe, Cu, Mg, Na, K, Zn. Hãy sắp xếp các kim loại trên theo thứ tự tính khử giảm dần.
Cho các cation kim loại: Ag+, Na+, Fe2+, Fe3+, Al3+, Cu2+, Mg2+. Hãy sắp xếp các cation kim loại trên theo thứ tự tính oxi hoá giảm dần.
Cho các kim loại Al, Mg, Fe, Cu lần lượt tác dụng với lượng dư mỗi dung dịch chứa lần lượt ion Fe3+, Cu2+, Ag+. Viết phương trình hoá học của các phản ứng xảy ra (nếu có).
Cho các thí nghiệm sau, hãy điền vào chỗ trống:
a. Cho Mg tác dụng với dung dịch FeCl3 dư thu được dung dịch X.
Chất tan trong X gồm:……………………………………………
b. Cho Fe tác dụng với dung dịch AgNO3 dư thu được dung dịch Y.
Chất tan trong Y gồm:…………………………………………....
c. Cho Mg, Al tác dụng với dung dịch Cu(NO3)2 thu được dung dịch Z chứa 2 muối.
Công thức của hai muối trong Z là………………………………….
Trong các hoạt động của pin điện hóa Al-Zn nồng độ của các ion trong dung dịch biến đổi như thế nào?
Cho sức điện động chuẩn của các pin điện hoá sau:
Epin(T-X) = 2,46 V; E°pin (T – Y) = 2,00 V; E°pin (Z – Y) = 0,90 V (với X, Y, Z, T là bốn kim loại). Hãy sắp xếp các kim loại này theo chiều tăng dần tính khử.
Khi nhúng một lá kẽm vào dung dịch muối Cu2+, sau một thời gian nhận thấy có một lớp kim loại đồng phủ ngoài lá kẽm. Khi nhúng lá chì vào dung dịch muối Cu2+ cũng sau một thời gian như trên, không nhận thấy hiện tượng nào xảy ra. Sắp xếp các cặp oxi hóa – khử của những kim loại trên theo chiều tăng dần tính oxi hóa của cation.
Cho sức điện động chuẩn của các pin điện hoá sau: Epin(Cu-X) = 0,46 V; E°pin (Y – Cu) = 2,71 V; E°pin(Z- Cu) = 0,78 V (với X, Y, Z là ba kim loại). Hãy sắp xếp các kim loại X, Y, Z trên theo chiều tăng dần tính khử.
Cho giá trị thế điện cực chuẩn của một số cặp oxi hoá - khử: EFe2+/Feo=−0,44V; ECu2+/Cuo=0,34V; EAg+/Ago=0,80V
Hãy cho biết ion nào có thể oxi hoá được kim loại Fe.
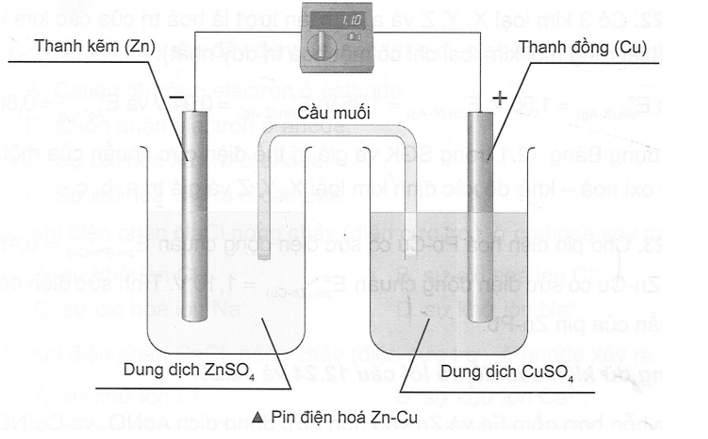
Cho ECu2+/Cuo=0,34V. Quan sát thí nghiệm như hình bên dưới và tính thế điện cực chuẩn của Zn2+/Zn.
Cho biết giá trị thế điện cực của một số cặp oxi hoá- khử như sau: EFe2+/Feo=−0,44V;EPb2+/Pbo=−0,13V;ECu2+/Cuo=0,34V;.
Hãy dự đoán hiện tượng xảy ra khi:
a) trộn dung dịch lead(II) nitrate với dung dịch copper(II) nitrate.
b) Nhúng một lá chì vào dung dịch copper(II) nitrate.
c) Nhúng một lá đồng vào dung dịch lead(II) nitrate.
d) Nhúng một lá kẽm trong dung dịch copper(II) nitrate và lead(II) nitrate.
Viết các phương trình hoá học xảy ra (nếu có).
Cho biết giá trị thế điện cực chuẩn của một số cặp oxi hoá – khử như sau: EM2+/Mo=−2,37V;EX2+/Xo=−0,44V;EY2+/Yo=−0,76V;EZ2+/Zo=0,34V . Viết phương trình hoá học phản ứng có thể xảy ra khi cho mỗi kim loại (M, X, Y, Z) phản ứng với từng dung dịch chứa các ion tương ứng của từng kim loại đó
Có 3 kim loại X, Y, Z và a, b, c lần lượt là hóa trị của các kim loại đó (biết rằng mỗi kim loại có một hóa trị duy nhất).
Cho E°pin(X-Ag) = 1,56 V; E°pin (Y – Ag) = 1,05 V; E°pin(Z- Ag) = 0,94 V và EAg+/Ago=0,80V. Sử dụng bảng 12.1 trong SGK về giá trị thế điện cực chuẩn của một số cặp oxi hóa – khử để xác định kim loại X, Y, Z và giá trị a, b, c.
Cho pin điện hóa Pb – Cu có sức điện động chuẩn E°pin (Pb – Cu) = 0,47 V, pin Zn – Cu có sức điện động chuẩn E°pin (Zn – Cu) = 1,10 V. Tính sức điện động chuẩn của pin Zn – Pb.
Xác định công thức hóa học của 2 muối trong dung dịch X
Xác định hai kim loại trong chất rắn Y



