Đề thi thử tốt nghiệp THPT môn Hóa học Chuyên KHTN- Lần 1 có đáp án
40 câu hỏi
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Cr = 52; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Ba = 137.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Cho biết: . Sự sắp xếp nào đúng với tính oxi hóa của các cation Al3+, Fe2+ và Cu2+?
Cu2+ > Fe2+ > Al3+.
Fe2+ > Cu2+ > Al3+.
Cu2+ > Al3+ > Fe2+.
Al3+ > Fe2+ > Cu2+.
Năng lượng hóa học của một số phản ứng được ghi ở các sơ đồ dưới đây:
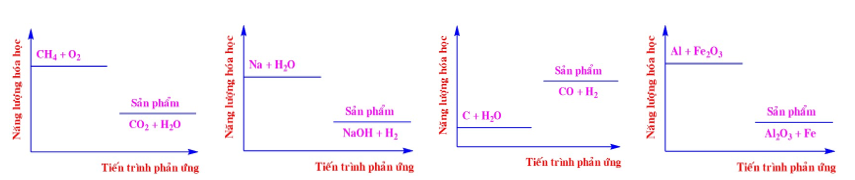
Số phản ứng tỏa nhiệt là
2.
4.
1.
3.
Khi cho khí chlorine vào dung dịch KI dư thì thu được dung dịch X. Nhỏ vài giọt hồ tinh bột vào dung dịch X thì dung dịch chuyển màu gì?
Vàng lục.
Xanh tím.
Tím đen.
Đỏ nâu.
Cho sơ đồ phản ứng sau: 2-Chlorobutane .
Trong đó: X là sản phẩm chính của phản ứng (1). Chất Y là
CH3CH2CH2CH2OH.
(CH3)3C-OH và (CH3)2CH-CH2OH.
CH3-CH2CH(OH)-CH3 và CH3CH2CH2CH2OH.
CH3-CH2-CH(OH)-CH3.
Cho các polymer sau:
Polymer được điều chế bằng phản ứng trùng hợp methyl acrylate là
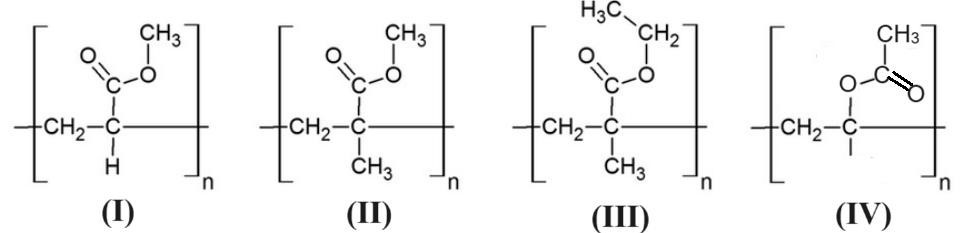
(I).
(II).
(III).
(IV).
Chất nào sau đây là thành phần chính của chất giặt rửa tổng hợp ?
CH3[CH2]16-COONa.
CH3[CH2]11-C6H4-SO3Na.
CH3[CH2]14-COOK.
(CH3[CH2]16-COO)2Ca.
Dạng mạch vòng của glucose có cấu tạo như hình dưới đây. Nhóm -OH hemiacetal ở vị trí của carbon nào?
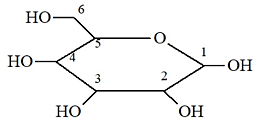
số 4.
số 6.
số 1.
số 2.
Chất nào sau đây có thể điều chế trực tiếp được bằng phản ứng oxi hóa ethylene?
CH3-CHO.
polyethylene.
CH3-CH3.
CH3-CH2-OH.
Trên thực tế, khí thải chứa SO2 được dẫn vào dung dịch Ca(OH)2, sản phẩm cuối cùng thu được là CaSO4.2H2O (thạch cao). Hãy cho biết ngoài khí SO2 còn có khí nào sau đây tham gia phản ứng?
H2.
H2S.
HCl.
O2.
Mô hình mô tả quá trình tạo liên kết hóa học sau đây phù hợp với xu hướng tạo liên kết hóa học của nguyên tử nào?
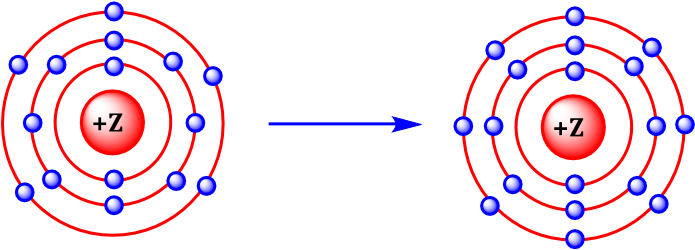
Oxygen (8O).
Nitrogen (7N).
Aluminium (13Al).
Phosphorus (15P).
Một acid béo có công thức cấu tạo là
![]()
Acid béo này thuộc loại omega nào sau đây?
Omega-6.
Omega-3.
Omega-9.
Omega-5.
Acetic acid trong giấm ăn có thể được sử dụng để loại bỏ CaCO3 bám vào vật dụng. Sử dụng 200 mL dung dịch giấm ăn (D = 1,05 g/mL) chứa CH3COOH 5% có thể làm sạch tối đa bao nhiêu CaCO3 bám vào vật dụng?
8,75 gam.
9,25 gam.
12,00 gam.
6,75 gam.
Cho 9,48 gam phèn chua (K2SO4.Al2(SO4)3.24H2O) vào nước thu được 500 mL dung dịch. Nồng độ ion K+ có trong phèn chua là
0,02.
0,01.
0,04.
0,05.
Cho biết sức điện động chuẩn của các pin sau:
Pin điện hóa | X - Y | M - Y | M - Z |
Sức điện động chuẩn (V) | 0,20 | 0,60 | 0,30 |
Sự sắp xếp nào đúng với tính khử của các kim loại X, Y, Z, M?
M < Z < Y < X.
Y < X < Z < M.
X < Y < M < Z.
X < Y < Z < M.
Một amino acid có công thức cấu tạo CH3-CH(NH2)-COOH có tên thay thế là
α-amino propionic.
2-amino propanoic.
2-amino propionic.
alanine.
Glutamic acid có các dạng tồn tại và giá trị pH mà dạng tồn tại đó là chủ yếu (≈ 100%) sau:
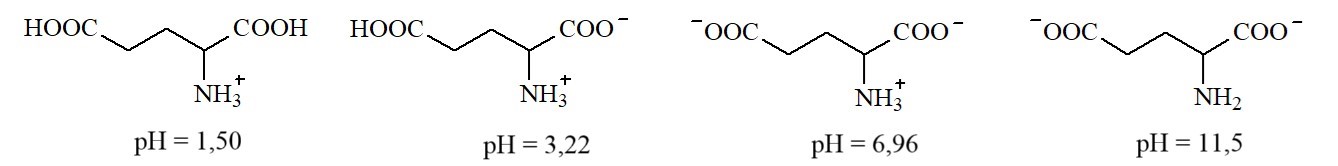
Giá trị pH của dung dịch bằng bao nhiêu thì glutamic acid không bị điện di?
11,5.
3,22.
1,50.
6,96.
Ở 3000oC, phản ứng: N2(g) + O2(g) 2NO(g) ΔrHo = 186,2 kJ.
Tác động nào sau đây làm cân bằng trên chuyển dịch về phía thuận?
tăng nhiệt độ hệ phản ứng.
tăng áp suất chung của hệ phản ứng.
giảm áp suất chung của hệ phản ứng.
giảm nhiệt độ của hệ phản ứng.
Một phương pháp xử lí nước thải chứa các cation kim loại nặng bằng cách điện phân dung dịch nước thải (pH ≤ 5, mật độ dòng điện khoảng 10mA/cm2) để tạo ra các chất kết tủa tại khu vực điện cực. Hãy cho biết quá trình kết tủa này xảy ra ở khu vực điện cực nào trong điện phân?
tại cathode.
tại bề mặt dung dịch.
cả anode và cathode.
tại anode.
a) Salbutamol tác dụng với NaOH theo tỉ lệ mol 1 : 3.
b) Một vận động viên thể thao có cân nặng 80 kg thì trong vòng 24h chỉ được sử dụng liều tối đa là 1600 µg salbutamol.
c) Khi cho salbutamol tác dụng với HBr dư thu được hợp chất có công thức phân tử là C13H22NO3Br
d) Salbutamol tác dụng với Na theo tỉ lệ mol 1 : 3.
a) Để tăng hiệu suất chiết ethyl acetate từ bình hứng, thêm muối ăn (NaCl) hoặc thêm dung dịch muối ăn bão hòa vào.
b) Phản ứng điều chế ethyl acetate từ các nguyên liệu trên được gọi là phản ứng ester hóa.
c) Vai trò H2SO4 là xúc tác và hút nước để chuyển dịch cân bằng trong phản ứng ester hóa.
d) Trong quá trình phản ứng, phần hơi tách ra từ bình cầu có nhánh sang bình hứng là ethyl acetate và nước.
a) Dung dịch X làm quỳ tím chuyển sang màu xanh.
b) Thủy phân X có thể thu được tối đa 5 dipeptide.
c) Thủy phân hoàn toàn X trong dung dịch NaOH dư đun nóng, thu được tối đa 4 muối.
d) X là hexapeptide.
a) Bề dày của miếng sắt (A) bằng 0,055 (cm)
b) Đường cong số (1) mô tả tốc độ thoát khí từ miếng sắt (A).
c) Đường cong số (2) mô tả tốc độ thoát khí từ miếng sắt (B)
d) Bán kính nguyên tử sắt 1,28Ao.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Ethanol có thể được sản xuất từ cellulose. Loại ethanol này được dùng để sản xuất xăng E5 (chứa 5% ethanol về thể tích). Ethanol thu được từ 1 tấn mùn cưa (chứa 50% cellulose, phần còn lại là chất trơ) có thể dùng để pha chế bao nhiêu L xăng E5?
Biết hiệu suất quá trình sản xuất ethanol từ cellulose là 60% và ethanol có khối lượng riêng là 0,8 g.mL–1. (Làm tròn kết quả đến hàng đơn vị)
Nhôm (Aluminium) được sản xuất bằng phương pháp điện phân Al2O3 tinh khiết. Quặng nhôm thường chứa thạch anh, silicate (chứa Si) và một số tạp chất khác cần được loại bỏ. Một loại quặng bauxite gồm Al2O3.3H2O và 10,0 % kaolin Al2Si2O7.2H2O được dùng để sản xuất nhôm theo quy trình Bayer. Tính tỉ lệ hao hụt của nhôm trong quá trình tinh chế, biết silic thường được loại bỏ ở dạng bùn aluminosilicat (Na6Al6Si5O22.5H2O). (Làm tròn kết quả đến hàng phần trăm)
Hydrogen hóa chất béo lỏng để chuyển thành chất béo rắn là quá trình phá vỡ các liên kết C=C để chuyển thành các liên kết C-C.
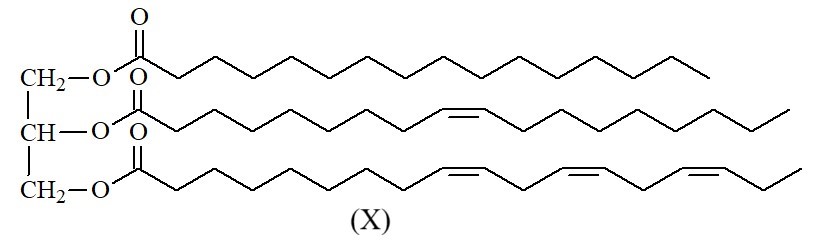
Chất béo E có chứa X và các triglyceride no. Hydrogen hóa hoàn toàn 10 kg E thu được tối đa 10,05 kg chất béo no. Thành phần % theo khối lượng của X có trong E là bao nhiêu %? (Làm tròn kết quả đến hàng phần mười).
Cho sơ đồ sau:
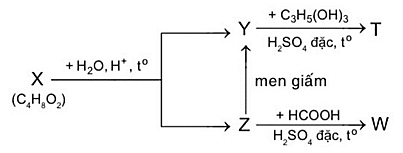
Trong đó: X, Y, Z, T, W là các hợp chất hữu cơ khác nhau; T chỉ chứa một loại nhóm chức. Xác định phân tử khối của T?
Dùng phương pháp mạ zinc để bảo vệ các tấm thép có tổng diện tích bề mặt là 2m2. Khi đó, các tấm thép cần mạ là cathode; dung dịch mạ chứa phức chất [Zn(OH)4]2- và các tấm zinc nguyên chất là anode. Tiến hành mạ với mật độ dòng điện là 200 A/m2 và lớp mạ có độ dày 6,5 μm. Tính thời gian (theo giờ) hoàn thành lớp mạ đó? (Làm tròn đến hàng phần trăm). Cho biết khối lượng riêng DZn = 7,14 g/cm3 và 1 mol điện lượng = 1F (F: hằng số faraday) = 96485 C.
Để xác định hàm lượng oxygen (O2) tan trong nước, người ta lấy 100,0 mL nước rồi cho ngay manganese sulphate (MnSO4, dư) và sodium hydroxide (NaOH) vào nước. Sau khi lắc kĩ (không cho tiếp xúc với không khí), manganese(II) hydroxide (Mn(OH)2) bị O2 oxi hóa thành manganese oxohydroxide (MnO(OH)2). Thêm acid (dư) và cho tiếp potassium iodide (KI, dư) vào hỗn hợp, thì ion idodine (I-) bị MnO(OH)2 oxi hóa thành ioddine (I2). Lượng I2 sinh ra phản ứng vừa đủ với 10,5 mL dung dịch Na2S2O3 0,01M (sodium thiosulphate). Biết các phản ứng xảy ra như sau:
Mn2+ + OH- → Mn(OH)2 (1)
Mn(OH)2 + O2 → MnO(OH)2 (2)
MnO(OH)2 + I- + H+ → Mn2+ + I2 + H2O (3)
I2 + Na2S2O3 → Na2S4O6 + NaI (4)
Hàm lượng O2 tan trong nước (tính theo mg O2/1L) là a. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến hàng phần mười).








