20 bài tập Hóa 10 Kết nối tri thức Bài 19: Tốc độ phản ứng hóa học (có lời giải)
30 câu hỏi
Cho phản ứng của các chất ở thể khí: 2NO + 2H2 ![]() N2 + 2H2O
N2 + 2H2O
Hãy viết biểu thức tính tốc độ trung bình theo sự biến đổi nồng độ chất đầu và chất sản phẩm của phản ứng trên.
Cho phản ứng: 6CH2O + 4NH3 ![]() (CH2)6N4 + 6H2O. Hãy viết biểu thức tính tốc độ trung bình theo sự biến đổi nồng độ chất đầu và chất sản phẩm của phản ứng trên.
(CH2)6N4 + 6H2O. Hãy viết biểu thức tính tốc độ trung bình theo sự biến đổi nồng độ chất đầu và chất sản phẩm của phản ứng trên.
Hoàn thành bảng sau, cho biết mỗi thay đổi sẽ làm tăng hay giảm tốc độ của phản ứng?
Yếu tố ảnh hưởng | Tốc độ phản ứng |
Đun nóng chất tham gia | Tăng |
Thêm chất xúc tác phù hợp |
|
Pha loãng dung dịch |
|
Ngưng dùng enzyme (chất xúc tác) |
|
Giảm nhiệt độ |
|
Tăng nhiệt độ |
|
Giảm nhiệt tích bề mặt |
|
Tăng nồng độ chất phản ứng |
|
Chia nhỏ chất phản ứng thành mảnh nhỏ |
|
Hoàn thành bảng sau, cho biết yếu tố chính ảnh hưởng đến tốc độ phản ứng trong từng trường hợp.
Tình huống | Yếu tố ảnh hưởng |
Duy trì thổi không khí vào bếp để than cháy đều |
|
Than đá được nghiền nhỏ dùng trong quá trình luyện kim loại |
|
Thức ăn được tiêu hóa trong dạ dày nhờ acid và enzyme |
|
Xác của một số loài động vật được bản quản nguyên vẹn ở Bắc cực và Nam cực hàng ngàn năm |
|
Vụ nổ bụi xảy ra tại một xưởng cưa |
|
Hoàn thành bảng sau, cho biết yếu tố chính ảnh hưởng đến tốc độ phản ứng trong từng trường hợp.
Tình huống | Yếu tố ảnh hưởng |
Than củi đang cháy, dùng quạt thổi thêm không khí vào, sự cháy diễn ra mạnh hơn |
|
Phản ứng oxi hóa SO2 thành SO3 diễn ra nhanh hơn khi có mặt V2O5 |
|
Aluminium (Al) dạng bột phản ứng với dung dịch hydrochloric acid nhanh hơn so với Al dạng lá |
|
Để thực phẩm trong tủ lạnh giúp cho thực phẩm được tươi lâu hơn |
|
Sử dụng nồi áp suất để hầm thức ăn giúp thức ăn nhanh chín |
|
Sử dụng các loại men thích hợp để làm sữa chua, lên men rượu, giấm,… |
|
Sục khí CO2 vào bình chứa dung dịch Na2CO3.
Tốc độ hấp thụ khí CO2 sẽ thay đổi như thế nào nếu thêm các chất sau đây vào dung dịch Na2CO3?
(i) HCl; (ii) NaCl; (iii) H2O; (iv) K2CO3.
Sục khí CO2 vào bình chứa dung dịch Na2CO3.
Nếu tăng áp suất, tốc độ phản ứng thay đổi như thế nào?
Cho các phản ứng hóa học sau:
(1) FeCl3 + 3NaOH ![]() Fe(OH)3 + 3NaCl
Fe(OH)3 + 3NaCl
(2) 3Fe + 2O2 ![]() Fe3O4
Fe3O4
(3) 4K + O2 ![]() 2K2O
2K2O
(4) CH3COOH + C2H5OH ![]() CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
Ở điều kiện thường, phản ứng nào xảy ra nhanh, phản ứng nào xảy ra chậm?
Cho phản ứng hóa học sau:
CH3COOC2H5(l) + H2O(l) ![]() CH3COOH(l) + C2H5OH(l)
CH3COOH(l) + C2H5OH(l)
Tốc độ các phản ứng trên sẽ thay đổi như thế nào nếu ta thêm nước vào bình phản ứng?
Cho phản ứng hóa học sau:
Zn(s) + H2SO4(aq) ![]() ZnSO4(aq) + H2(g)
ZnSO4(aq) + H2(g)
Tốc độ các phản ứng trên sẽ thay đổi như thế nào nếu ta thêm nước vào bình phản ứng?
Cho phản ứng hóa học sau:
H2C2O4(aq) + 2KMnO4(aq) + 8H2SO4(aq) ![]() 10CO2(g) + 2MnSO4(aq) + 8H2O(l)
10CO2(g) + 2MnSO4(aq) + 8H2O(l)
Tốc độ các phản ứng trên sẽ thay đổi như thế nào nếu ta thêm nước vào bình phản ứng?
Áp suất ảnh hưởng đến tốc độ phản ứng nào sau đây?
N2(g) + 3H2(g) ![]() 2NH3(g) (1)
2NH3(g) (1)
CO2(g) + Ca(OH)2(aq) ![]() CaCO3(s) + H2O(l) (2)
CaCO3(s) + H2O(l) (2)
SiO2(s) + CaO(s) ![]() CaSiO3(s) (3)
CaSiO3(s) (3)
BaCl2(aq) + H2SO4(aq) ![]() BaSO4(s) + 2HCl(aq) (4)
BaSO4(s) + 2HCl(aq) (4)
Thực hiện hai phản ứng phân hủy H2O2: một phản ứng có xúc tác MnO2, một phản ứng không có xúc tác. Đo thể tích khí oxygen theo thời gian và biểu diễn trên đồ thị như hình dưới:
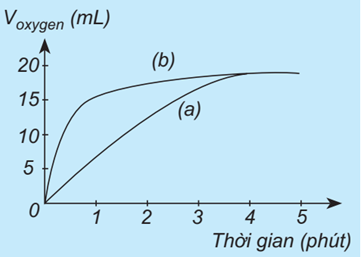
Đường phản ứng nào trên đồ thị tương ứng với có xúc tác, với phản ứng không có xúc tác?
Hãy cho biết trong các phản ứng sau, phản ứng nào có tốc độ nhanh, phản ứng nào có tốc độ chậm.
a) Đốt cháy nhiên liệu.
b) Iron (Fe) bị gỉ.
c) Trung hòa acid – base.
Xét phản ứng: H2 + Cl2 ![]() 2HCl
2HCl
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị như sau:
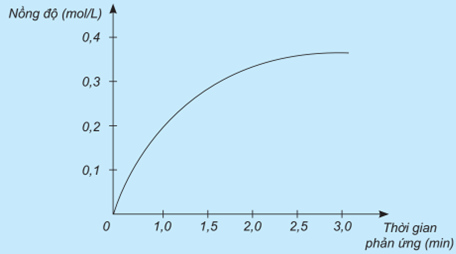
a) Đồ thị này mô tả sự thay đổi nồng độ theo thời gian của chất nào?
Xét phản ứng: H2 + Cl2 ![]() 2HCl
2HCl
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị như sau:
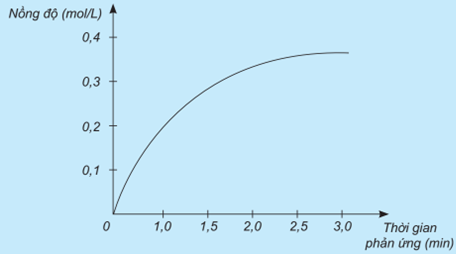 Nêu đơn vị của tốc độ phản ứng trong trường hợp này.
Nêu đơn vị của tốc độ phản ứng trong trường hợp này.
Thực hiện phản ứng: 2ICl + H2 ![]() I2 + 2HCl
I2 + 2HCl
Nồng độ đầu của ICl và H2 được lấy đúng theo tỉ lệ hợp thức. Nghiên cứu sự thay đổi nồng độ các chất tham gia và chất tạo thành trong phản ứng theo thời gian, thu được đồ thị sau:
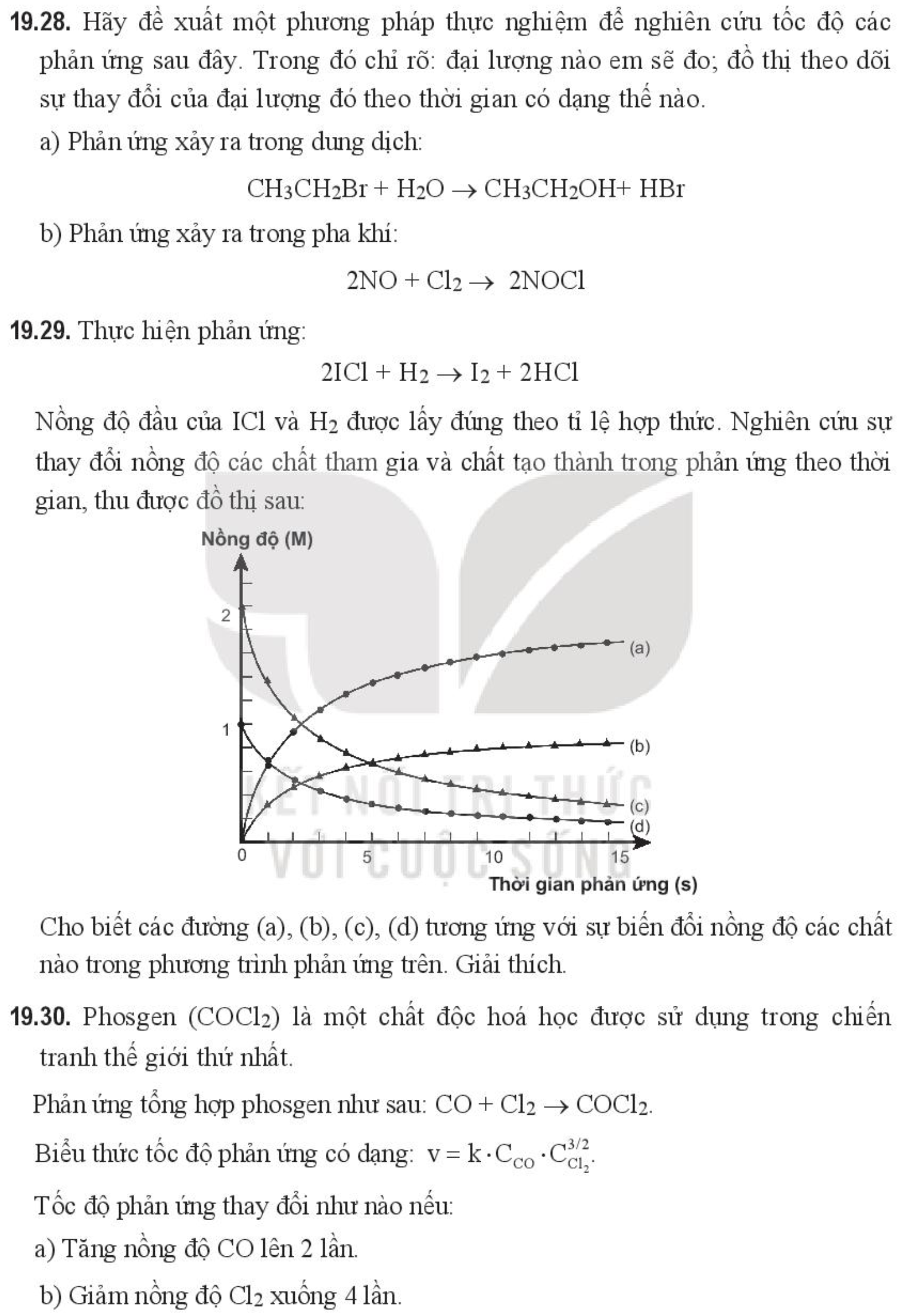
Cho biết các đường (a), (b), (c), (d) tương ứng với sự biến đổi nồng độ các chất nào trong phương trình phản ứng trên. Giải thích.
Cho khoảng 2 gam zinc (Zn) dạng hạt vào một cốc đựng dung dịch H2SO4 2 M (dư) ở nhiệt độ phòng. Nếu chỉ biến đổi một trong các điều kiện sau đây (các điều kiện khác giữ nguyên) thì tốc độ phản ứng sẽ thay đổi thế nào (tăng lên, giảm xuống hay không đổi)?
Thay Zn hạt bằng Zn bột cùng khối lượng và khuấy đều.
Cho khoảng 2 gam zinc (Zn) dạng hạt vào một cốc đựng dung dịch H2SO4 2 M (dư) ở nhiệt độ phòng. Nếu chỉ biến đổi một trong các điều kiện sau đây (các điều kiện khác giữ nguyên) thì tốc độ phản ứng sẽ thay đổi thế nào (tăng lên, giảm xuống hay không đổi)?
Thay dung dịch H2SO4 2 M bằng dung dịch H2SO4 1 M có cùng thể tích.
Cho khoảng 2 gam zinc (Zn) dạng hạt vào một cốc đựng dung dịch H2SO4 2 M (dư) ở nhiệt độ phòng. Nếu chỉ biến đổi một trong các điều kiện sau đây (các điều kiện khác giữ nguyên) thì tốc độ phản ứng sẽ thay đổi thế nào (tăng lên, giảm xuống hay không đổi)?
Thực hiện phản ứng ở nhiệt độ cao hơn (khoảng 50 ℃).
Hai bạn Tôm và Vừng thực hiện một thí nghiệm về sự phân hủy của hydrogen peroxide với chất xúc tác manganese dioxide (MnO2). Hai bạn thất rằng phản ứng sủi bọt nhiều và khí thoát ra mạnh khi thêm manganese dioxide.
Hoàn thành các câu sau đây nói về thí nghiệm của hai bạn.
Phương trình của phản ứng là:……
Hai bạn Tôm và Vừng thực hiện một thí nghiệm về sự phân hủy của hydrogen peroxide với chất xúc tác manganese dioxide (MnO2). Hai bạn thất rằng phản ứng sủi bọt nhiều và khí thoát ra mạnh khi thêm manganese dioxide.
Hoàn thành các câu sau đây nói về thí nghiệm của hai bạn.
Chất khí thoát ra là…… và có thể kiểm tra (nhận biết) ra nó bằng cách……
Hai bạn Tôm và Vừng thực hiện một thí nghiệm về sự phân hủy của hydrogen peroxide với chất xúc tác manganese dioxide (MnO2). Hai bạn thất rằng phản ứng sủi bọt nhiều và khí thoát ra mạnh khi thêm manganese dioxide.
Hoàn thành các câu sau đây nói về thí nghiệm của hai bạn.
Sau một thời gian nhất định, Vừng nói với Tôm là phản ứng đã kết thúc vì……
Hai bạn Tôm và Vừng thực hiện một thí nghiệm về sự phân hủy của hydrogen peroxide với chất xúc tác manganese dioxide (MnO2). Hai bạn thất rằng phản ứng sủi bọt nhiều và khí thoát ra mạnh khi thêm manganese dioxide.
Hoàn thành các câu sau đây nói về thí nghiệm của hai bạn.
Hai bạn biết rằng chất xúc tác chỉ làm tăng tốc độ phản ứng mà không thay đổi về bản chất hóa học nên Tôm sẽ thu lại manganese dioxide sau khi phản ứng kết thúc bằng cách……
Chè (trà) xanh là thực phẩm được dùng phổ biến để nấu nước uống, có tác dụng chống lão hóa, giảm nguy cơ bị ung thư, phòng một số bệnh về tim mạch và giảm cân,… Tuy nhiên, uống nhiều nước chè xanh hay nước chè đặc sẽ gây thiếu hụt hồng cầu máu, đau dạ dày, xót ruột, buồn nôn. Caffeine là chất kích thích cũng có nhiều trong lá chè, làm thần kinh căng thẳng, mất ngủ, suy giảm trí nhớ và dễ gây nghiện.
Hãy làm rõ yếu tố nồng độ các chất có trong lá chè xanh, caffeine ảnh hưởng đến sức khỏe con người trong khuyến cáo trên.
Bộ chuyển đổi xúc tác là thiết bị được sử dụng để giảm lượng khí thải từ động cơ đốt trong của ô tô và các loại phương tiện giao thông hiện đại. Thiết bị có sử dụng các kim loại platium, rhodium và palladium để thúc đẩy quá trình nhường, nhận electron của chất trong khí thải, nó hoạt động theo cơ chế phản ứng oxi hóa – khử, chuyển đổi khoảng 98% khí thải độc hại thành khí ít độc hại hoặc không độc hại cho môi trường. Khí thải chứa các hydrocarbon bị oxi hóa thành carbon dioxide, các oxide của nitrogen và oxygen giải phóng ra môi trường.

Thiết bị trên vận dụng yếu tố nào để tác động đến phản ứng?
Hệ thống phun nhiên liệu điện tử (Electronic Fuel Injection – EFI) được sử dụng trong động cơ ô tô, xe máy giúp tiết kiệm nhiên liệu, xe vận hành êm và giảm ô nhiễm môi trường. Hệ thống sử dụng bộ điều khiển điện tử để can thiệp vào bước phun nhiên liệu vào buồng đốt, nhiên liệu được phun giọt cực nhỏ (1); hệ thống điều chỉnh chính xác tỉ lệ nhiên liệu – không khí trước khi phun vào buồng đốt, một cách đồng đều, nhiên liệu được đốt cháy hoàn toàn (2). Khi phương tiện thay đổi vận tốc (tăng hoặc giảm), hệ thống sẽ nhanh chóng thay đổi lượng nhiêu liệu – không khí phù hợp để phun vào buồng đốt (3), nên tiết kiệm nhiên liệu và giảm lượng khí thải gây ô nhiễm môi trường. Các ý (1), (2), (3) vận dụng yếu tố nào ảnh hưởng đến tốc độ phản ứng.
Trong công nghiệp, vôi sống được sản xuất bằng cách nung đá vôi. Phản ứng hóa học xảy ra như sau: CaCO3 ![]() CaO + CO2
CaO + CO2
Khi nung, đá vôi cần phải được đập nhỏ nhưng không nên nghiền mịn đá vôi thành bột. Giải thích.
Khí oxygen và hydrogen có thể cùng tồn tại trong một bình kín ở điều kiện bình thường mà không nguy hiểm. Nhưng khi có tia lữa điện hoặc một ít bột kim loại được thêm vào bình thì lập tức có phản ứng mãnh liệt xảy ra và có thể gây nổ.
Tia lửa điện có phải chất xúc tác không? Giải thích.
Khí oxygen và hydrogen có thể cùng tồn tại trong một bình kín ở điều kiện bình thường mà không nguy hiểm. Nhưng khi có tia lữa điện hoặc một ít bột kim loại được thêm vào bình thì lập tức có phản ứng mãnh liệt xảy ra và có thể gây nổ.
Bột kim loại có phải chất xúc tác không? Giải thích








