10 bài tập Hóa 10 Kết nối tri thức Bài 22: Nhóm Halogen Halide. Muối Halide có lời giải
21 câu hỏi
Viết PTHH của phản ứng xảy ra trong trường hợpKim loại Mg phản ứng với dung dịch HBr
Viết PTHH của phản ứng xảy ra trong trường hợp:Dung dịch KOH phản ứng với dung dịch HCl.
Viết PTHH của phản ứng xảy ra trong trường hợp:Muối CaCO3 phản ứng với dung dịch HCl
Viết PTHH của phản ứng xảy ra trong trường hợp:Dung dịch AgNO3 phản ứng với dung dịch CaI2
Viết PTHH khi cho dung dịch hydrochloric acid lần lượt tác dụng với: Fe, MgO, Cu(OH)2, AgNO3.
Hoàn thành phương trình hóa học của phản ứng sau:
HCl(aq) + KMnO4(s) ![]() KCl(aq) + MnCl2(aq) + Cl2(g) + H2O(l)
KCl(aq) + MnCl2(aq) + Cl2(g) + H2O(l)
Hoàn thành phương trình hóa học của phản ứng sau:
MnO2(s) + HCl(aq) ![]() MnCl2(aq) + ? + H2O(l)
MnCl2(aq) + ? + H2O(l)
Hoàn thành phương trình hóa học của phản ứng sau:
Cl2(g) + ? ![]() ? + NaClO3(aq) + H2O(l)
? + NaClO3(aq) + H2O(l)
Hoàn thành phương trình hóa học của phản ứng sau:
NaBr(aq) + H2SO4(l) ![]() NaHSO4(s) + ? + SO2(g) + H2O(g)
NaHSO4(s) + ? + SO2(g) + H2O(g)
Hoàn thành phương trình hóa học của phản ứng sau:
HI(g) + ? ![]() I2(g) + H2S(g) + H2O(l)
I2(g) + H2S(g) + H2O(l)
Nối mỗi chất trong cột A với những tính chất tương ứng của chúng trong cột B
Cột A | Cột B |
a) Hydrogen fluoride | 1. Là chất khí ở điều kiện thường. |
b) Hydrofluoric acid | 2. Các phân tử tạo liên kết hydrogen với nhau. |
c) Hydrogen chloride | 3. Có nhiệt độ sôi cao nhất trong dãy hydrogen halide. |
d) Hydrochloric acid | 4. Là acid mạnh. |
| 5. Ăn mòn thủy tinh. |
| 6. Thường được dùng để thủy phân các chất trong quá trình sản xuất. |
| 7. Hòa tan calcium carbonate có trong đá vôi, magnesium hydroxide, copper(II) oxide. |
Hãy đề xuất cách phân biệt bốn dung dịch hydrohalic acid bằng phương pháp hóa học.
Thực hiện thí nghiệm thử tính tan của hydrogen chloride theo các bước sau:
- Bước 1: chuẩn bị một bình khô chứa khí HCl, đậy bằng nút cao su có ống thủy tinh xuyên qua và một cốc nước.
- Bước 2: nhúng ống thủy tinh vào cốc nước, thấy nước phun vào bình như hình dưới.
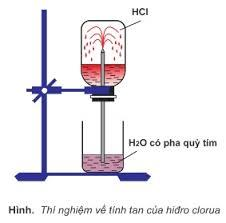
Hiện tượng nước phun vào bình cho thấy áp suất khí HCl trong bình đã tăng hay giảm rất nhah? Giải thích?
Thực hiện thí nghiệm thử tính tan của hydrogen chloride theo các bước sau:
- Bước 1: chuẩn bị một bình khô chứa khí HCl, đậy bằng nút cao su có ống thủy tinh xuyên qua và một cốc nước.
- Bước 2: nhúng ống thủy tinh vào cốc nước, thấy nước phun vào bình như hình dưới.
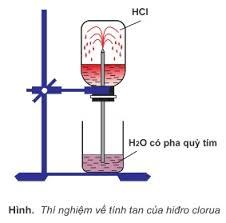
Sự biến đổi áp suất như vậy đã chứng tỏ tính chất gì của khí HCl?
Trong có thể người, dịch vị dạ dày có môi trường acid (HCl), pH = 1,6 ÷ 2,4 giúp hỗ trợ tiêu hóa.
Một bệnh nhân bị đau dạ dày do dư thừa acid được kê đơn thuốc có chứa NaHCO3. Viết PTHH minh họa tác dụng của thuốc.
Trong có thể người, dịch vị dạ dày có môi trường acid (HCl), pH = 1,6 ÷ 2,4 giúp hỗ trợ tiêu hóa.
Ở 37 ℃, tinh bột bị thủy phân thành glucose trong môi trường acid (HCl) có xúc tác enzyme. Viết PTHH của phản ứng xảy ra.
Có hai ống nghiệm, mỗi ống chứa 2 mL dung dịch muối của sodium. Cho vài giọt dung dịch AgNO3 vào ống thứ nhất, thu được kết tủa màu vàng nhạt. Nhỏ vài giọt nước Cl2 vào ống thứ hai, lắc nhẹ, thêm 1 mL benzene và lắc đều, thấy benzene từ không màu chuyển sang màu da cam. Xác định công thức của muối sodium và viết PTHH của phản ứng xảy ra.
Dung dịch hydrobromic acid không màu, để lâu trong không khí thì chuyển sang màu vàng nâu do phản ứng với oxygen trong không khí.
Từ hiện tượng được mô tả trên, hãy dự đoán sản phẩm của quá trình dung dịch hydrobromic acid bị oxi hóa bởi oxygen trong không khí.
Dung dịch hydrobromic acid không màu, để lâu trong không khí thì chuyển sang màu vàng nâu do phản ứng với oxygen trong không khí.
Thực tế, hydrobromic acid được bảo quản trong các lọ tối màu. Giải thích?
Cho bảng thông tin sau:
Đặc điểm | HF | HCl | HBr | HI |
Năng lượng liên kết (kJ/mol) | 565 | 427 | 363 | 295 |
Độ dài liên kết ( | 0,92 | 1,27 | 1,41 | 1,61 |
Hằng số điện li acid (Ka)(*) (*) Đại lượng đo độ mạnh của một acid trong dung dịch | 7.10–4 | 1.107 | 1.109 | 1.1010 |
Sắp xếp theo thứ tự giảm dần tính acid của các hydrohalic acid.
Cho bảng thông tin sau:
Đặc điểm | HF | HCl | HBr | HI |
Năng lượng liên kết (kJ/mol) | 565 | 427 | 363 | 295 |
Độ dài liên kết ( | 0,92 | 1,27 | 1,41 | 1,61 |
Hằng số điện li acid (Ka)(*) (*) Đại lượng đo độ mạnh của một acid trong dung dịch | 7.10–4 | 1.107 | 1.109 | 1.1010 |
Dựa vào bảng thông tin, giải thích thứ tự tính acid của các hydrohalic acid.








