Giải SGK Hóa 11 CTST Bài 1: Khái niệm về cân bằng hoá học có đáp án
25 câu hỏi
Trong các phản ứng hoá học, có một loại phản ứng trong đó các chất sản phẩm có khả năng phản ứng để tạo thành các chất đầu. Do vậy, phản ứng xảy ra không hoàn toàn và thường có hiệu suất không cao. Phản ứng tổng hợp ammonia từ nitrogen và hydrogen thuộc loại phản ứng này. Các phản ứng này được gọi là phản ứng gì? Để tăng hiệu suất của chúng, cần điều chỉnh những điều kiện phản ứng như nhiệt độ, áp suất, nồng độ, … như thế nào?

Dựa vào phương trình hoá học của phản ứng điều chế khí oxygen từ KMnO4, em hãy cho biết phản ứng có xảy ra theo chiều ngược lại được không.
Viết phương trình hoá học của một số phản ứng một chiều mà em biết.
Phản ứng Cl2 tác dụng với H2O có đặc điểm gì khác với phản ứng nhiệt phân thuốc tím?
Trên thực tế có các phản ứng sau:
2H2 + O2 → 2H2O (1)
2H2O →dien phan2H2 + O2 (2)
Vậy có thể viết:
2H2 + O2 ⇌ 2H2O được không? Tại sao?
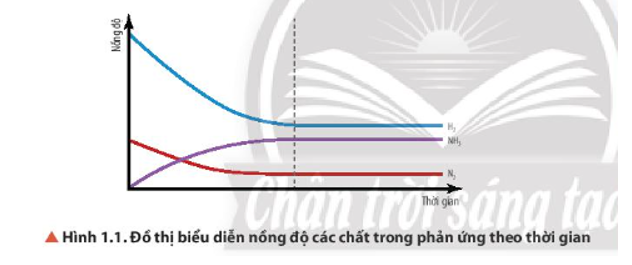
Quan sát Hình 1.1, nhận xét sự biến thiên nồng độ của các chất trong hệ phản ứng theo thời gian (với điều kiện nhiệt độ không đổi
Quan sát Hình 1.2, nhận xét về tốc độ của phản ứng thuận và tốc độ của phản ứng nghịch theo thời gian trong điều kiện nhiệt độ không đổi.

Sử dụng dữ liệu Bảng 1.1, hãy tính giá trị của biểu thức [N2O4][NO2]2 trong 5 thí nghiệm. Nhận xét giá trị thu được từ các thí nghiệm khác nhau.
![Sử dụng dữ liệu Bảng 1.1, hãy tính giá trị của biểu thức [N2O4]/ [NO2]^2 trong 5 thí nghiệm (ảnh 1)](https://video.vietjack.com/upload2/quiz_source1/2023/05/blobid3-1683856087.png)
Viết các biểu thức tính tốc độ phản ứng thuận và tốc độ phản ứng nghịch của phản ứng thuận nghịch sau, cho biết phản ứng thuận và phản ứng nghịch đều là phản ứng đơn giản:
aA + bB ⇌ cC + dD
Lập tỉ lệ giữa hằng số tốc độ phản ứng thuận và hằng số tốc độ phản ứng nghịch ở trạng thái cân bằng.
Cho hệ cân bằng nhau:
2SO2(g) + O2(g) ⇌ 2SO3(g)
Viết biểu thức tính hằng số cân bằng Kc của phản ứng trên.
Nêu hiện tượng xảy ra trong Thí nghiệm 1, từ đó cho biết chiều chuyển dịch cân bằng của phản ứng trong bình 2 và bình 3.
Nhận xét hiện tượng xảy ra trong Thí nghiệm 2.

Khi đun nóng, phản ứng trong bình (1) chuyển dịch theo chiều nào?
Cho biết chiều nào của phản ứng (1) là chiều thu nhiệt và chiều nào là chiều toả nhiệt.
Từ hiện tượng ở Thí nghiệm 1, cho biết khi làm lạnh bình (2) và làm nóng bình (3) thì cân bằng trong mỗi bình chuyển dịch theo chiều toả nhiệt hay thu nhiệt.
Người ta thường sản xuất vôi bằng phản ứng nhiệt phân calcium carbonate theo phương trình nhiệt hoá học sau:
CaCO3(s) ⇌ CaO(s) + CO2(g) ΔrH298o = 178,49 kJ.
Để nâng cao hiệu suất phản ứng sản xuất vôi, cần điều chỉnh nhiệt độ như thế nào? Giải thích.
Khi đẩy hoặc kéo pit – tông thì số mol khí của hệ (2) thay đổi như thế nào?

Phản ứng tổng hợp ammonia:
N2(g) + 3H2(g) ⇌to,xt,p 2NH3(g)
Để thu được NH3 với hiệu suất cao, cần điều chỉnh áp suất như thế nào?
Hãy cho biết cân bằng chuyển dịch theo chiều nào khi thêm một lượng khí CO vào hệ cân bằng (3).
Trong các hang động đá vôi thường xảy ra hiện tượng hình thành thạch nhũ và xâm thực của nước mưa vào đá vôi theo phương trình hoá học sau:
CaCO3(s) + H2O(l) + CO2(aq) ⇌ Ca(HCO3)2(aq)
Hãy giải thích các quá trình này.
Hằng số cân bằng Kc của một phản ứng thuận nghịch phụ thuộc vào yếu tố nào sau đây?
A. Nồng độ.
B. Nhiệt độ.
C. Áp suất.
D. Chất xúc tác.
Yếu tố nào sau đây luôn luôn không làm dịch chuyển cân bằng của hệ phản ứng?
A. Nhiệt độ.
B. Áp suất.
C. Nồng độ.
D. Chất xúc tác.
Viết biểu thức tính Kc cho các phản ứng sau:
(1) CaCO3(s) ⇌ CaO(s) + CO2(g)
(2) Cu2O(s) + 12O2(g)⇌ 2CuO(g)
Xét các hệ cân bằng sau trong một bình kín:
a) C(s) + H2O(g) ⇌ CO(g) + H2(g) ΔrH298o = 131 kJ
b) CO(g) + H2O(g) ⇌ CO2(g) + H2(g) ΔrH298o = -41 kJ
Các cân bằng trên dịch chuyển theo chiều nào khi thay đổi một trong các điều kiện sau?
(1) Tăng nhiệt độ.
(2) Thêm một lượng hơi nước vào hệ.
(3) Thêm khí H2 vào hệ.
(4) Tăng áp suất chung bằng cách nén cho thể tích của hệ giảm xuống.
(5) Dùng chất xúc tác.
Cho phản ứng sau:
COCl2(g) ⇌ CO(g) + Cl2(g) KC = 8,2×10-2 ở 900 K.
Tại trạng thái cân bằng, nếu nồng độ CO và Cl2 đều bằng 0,15 M thì nồng độ COCl2 là bao nhiêu?


