Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 trường THPT Thuận Thành (Bắc Ninh) lần 1 có đáp án
28 câu hỏi
Phương pháp nào sau đây được dùng để sản xuất giấm ăn?
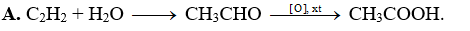
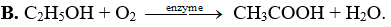
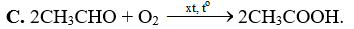
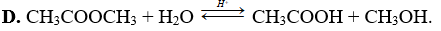
Một quặng chứa magnesium carbonate và barium carbonate, mẫu quặng này được hòa tan trong nitric acid. Làm thế nào để có thể tách riêng biệt hợp chất magnesium và barium ra khỏi dung dịch này?
Thêm H2SO4(aq), lọc magnesium sulfate rắn.
Thêm HCl(aq), lọc magnesium chloride rắn.
Thêm HCl(aq), lọc barium chloride rắn.
Thêm H2SO4(aq), lọc barium sulfate rắn.
Phản ứng nào sau đây không phải là phản ứng thuận nghịch?
Zn + HCl ® ZnCl2 + H2.
HbO2 + CO ⇌ HbCO + O2.
HCOOH + CH3OH ⇌ HCOOCH3 + H2O.
2SO3 ⇌ 2SO2 + O2.
Trong dung dịch NaCl loãng chứa các tiểu phân nào (bỏ qua nước và sự điện li của nước)?
Chỉ có Na+.
Na+ và Cl–.
Chỉ có Cl–.
NaCl, Na+, Cl–.
Phổ MS của chất A cho thấy A có phân tử khối bằng 60 amu. Công thức phân tử nào dưới đây không phù hợp với A?
C3H8O.
C2H8N2.
C2H4O2.
C3H7F.
Cho các thí nghiệm:
(a) Đun nóng C6H5CH2Cl trong dung dịch NaOH
(b) Đun nóng hỗn hợp CH3CH2CH2Cl, KOH và C2H5OH
(c) Cho acetylen tác dụng với H2O có mặt của xúc tác là muối Hg(II) trong H2SO4
(d) Lên men tinh bột với xúc tác enzyme
Có bao nhiêu thí nghiệm tạo sản phẩm chính là alcohol?
3
2
4
1
Alkene X có công thức cấu tạo: CH3–CH2–C(CH3)=CH–CH3. Tên gọi của X theo danh pháp IUPAC là
isohexane.
3-methylpent-3-ene.
3-methylpent-2-ene.
2-ethylbut-2-ene.
Sự có mặt của khí SO2 trong không khí là nguyên nhân chính gây ra hiện tượng mưa acid. Nồng độ của SO2 có thể xác định bằng cách chuẩn độ với dung dịch KMnO4 theo phản ứng sau:
SO2 + KMnO4 + H2O → K2SO4 + MnSO4 + H2SO4.
Biết một mẫu không khí phản ứng vừa đủ với 125mL dung dịch KMnO4 8,0.10-3M. Khối lượng (gam) của SO2 có trong mẫu không khí đó là
16.
1,6. 10-2.
0,16.
160.10-4.
Hợp chất hữu cơ X có công thức cấu tạo như sau:
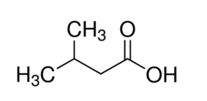
Phát biểu nào sau đây là đúng?
Công thức đơn giản nhất của X là C5H5O.
Trong một phân tử X có 4 nguyên tử carbon.
X có công thức phân tử là C5H8O2.
Phân tử X có chứa nhóm chức -COOH.
Trong tinh dầu thảo mộc có những aldehyde không no tạo nên mùi thơm đặc trưng của tinh dầu. Ví dụ: Tinh dầu quế có aldehyde cinnamic (C6H5CH=CHCHO), tinh dầu sả và chanh có citronellal (C9H17CHO) có công thức cấu tạo là:
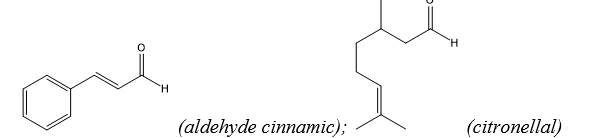
Hoá chất nào sau đây có thể dùng để nhận biết thành phần aldehyde trong tinh dầu?
H2/Ni, to.
Dung dịch NaOH.
Dung dịch HCl.
Thuốc thử Tollens.
Cho cân bằng hóa học sau: N2 (g) + 3H2 (g) ⇌ 2NH3 (g) < 0. Tổng số mol của hỗn hợp khí khi hệ đạt cân bằng ở nhiệt độ 400oC và 500oC là lượt là x và y. Mối quan hệ giữa x và y là
5x = 4y.
x < y.
x = y.
x > y.
Nhóm chức là
nguyên tử hoặc nhóm nguyên tử gây ra những tính chất hóa học đặc trưng của hợp chất hữu cơ.
một nhóm nguyên tử khác biệt trong chất hữu cơ.
một nhóm nguyên tử có cấu trúc không gian đặc biệt mà trong đó các nguyên tử liên kết với nhau không theo quy tắc hoá trị nào.
một nguyên tử bất kì trong phân tử chất hữu cơ.
Bước sơ cứu đầu tiên cần làm ngay khi một người bị bỏng sulfuric acid đặc là
rửa với nước lạnh nhiều lần.
trung hoà acid bằng NaHCO3.
băng bó tạm thời vết bỏng.
đưa đến cơ sở y tế gần nhất.
NOx là tên gọi chung của nhóm các khí thải nitrogen oxide – một trong những nhóm khí thải cực độc gây tác động trực tiếp đến sức khỏe con người. NOx có 30,43% N về khối lượng. Công thức phân tử của NOx là
N2O.
NO.
NO2.
N2O5.
Phần trăm khối lượng carbon trong phân tử alkane Y bằng 83,33%. Công thức phân tử của Y là
C3H8.
C2H6.
C5H12.
C4H10.
Cho các chất sau: H2, KMnO4, NaOH, H2O. Acetylen phản ứng được với bao nhiêu chất (trong điều kiện thích hợp)?
4.
1.
3.
2.
Sulfurphản ứng với chất nào sau đây thể hiện tính khử?
Iron (Fe).
Khí Oxygen (O2).
Khí hydrogen (H2).
Sodium (Na).
Cho các dung dịch loãng có cùng nồng độ mol/L, dung dịch có pH nhỏ nhất là
H2SO4.
NaOH.
HCl.
Ba(OH)2.
Trong quy trình sản xuất sulfuric acid (H2SO4) có giai đoạn dùng dung dịch H2SO4 98% hấp thụ sulfur trioxide (SO3) thu được oleum (H2SO4.nSO3). Sulfur trioxide được tạo thành bằng cách oxi hóa sulfur dioxide bằng oxygen hoặc lượng dư không khí ở nhiệt độ 450 – 500 °C, chất xúc tác vanadium (V) oxide (V2O5) theo phương trình nhiệt hóa học sau:
2SO2(g) + O2(g) ⇌ 2SO3(g)
Ở phản ứng trên, sulfur dioxide đóng vai trò là chất oxi hóa.
Thực hiện phản ứng ở áp suất cao để tăng hiệu suất phản ứng.
Phản ứng trên là phản ứng tỏa nhiệt. Vì vậy, để cân bằng chuyển dịch theo chiều thuận cần tăng nhiệt độ của hệ.
Hằng số cân bằng của phản ứng Kc phụ thuộc vào nồng độ ban đầu của SO2 và O2.
Dòng điện chạy qua được dung dịch nước của một chất X.
Trong dung dịch chất X có các ion dương và ion âm.
Chất X ở dạng rắn khan cũng dẫn điện.
Trong dung dịch chất X có electron tự do.
Chất X là chất điện li.
Geraniol có trong tinh dầu hoa hồng được sử dụng phổ biến trong công nghiệp hương liệu, thực phẩm,… vì có mùi thơm đặc trưng. Citral có trong tinh dầu sả có tác dụng an thần đối với hệ thần kinh, loại bỏ tế bào chết và chất nhờn trên da, hạ sốt, lợi tiểu, chống đầy hơi, khử trùng và kháng khuẩn mạnh. Geraniol và citral có cấu tạo như hình sau:
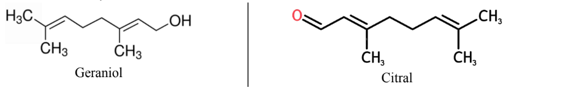
Geraniol có chứa nhóm chức alcohol, citral chứa nhóm chức ketone.
Geraniol thuộc loại hydrocarbon.
Số sóng hấp thụ đặc trưng trên phổ IR của nhóm C=O trong citral khoảng 1740-1685 cm–1.
Số sóng hấp thụ đặc trưng trên phổ IR của nhóm O – H trong geraniol khoảng 1760–1690 cm–1.
Cho bảng nhiệt độ sôi và độ tan trong nước của các chất như sau:
Loại hợp chất | Alkane | Aldehyde | Alcohol | Carboxylic acid |
Công thức cấu tạo | CH3CH2CH2CH3 | CH3CH2CHO | CH3CH2CH2OH | CH3COOH |
M | 58 | 58 | 60 | 60 |
Nhiệt độ sôi (oC) | –0,5 | 49 | 97,2 | 118 |
Độ tan trong nước 200C (g/100 g H2O) | Không tan | 20 | Vô hạn | Vô hạn |
CH3CH2CH2OH có nhiệt độ sôi lớn hơn CH3CH2CHO vì có khối lượng phân tử lớn hơn.
Phân tử alcohol và carboxylic acid tan vô hạn trong nước nhờ phân tử có nhóm chức phân cực và có khối lượng phân tử nhỏ.
Carboxylic acid có nhiệt độ sôi cao nhất vì có nhóm carboxylic acid phân cực và tạo được liên kết hydrogen giữa các phân tử bền nhất.
Phân tử aldehyde có nhiệt độ sôi cao hơn alkane do giữa các phân tử aldehyde tạo được liên kết hydrogen với nhau.
Để tách lấy lượng phân bón Kali người ta thường tách khỏi quặng sinvinit, thành phần chính củaquặng là NaCl, KCl. Vì NaCl và KCl có nhiều tính chất tương tự nhau nên người ta không dùng phươngpháp hóa học để tách chúng. Thực tế người ta dựa vào độ tan khác nhau trong nước theo nhiệt độ để táchhaichấtnày.
Nhiệtđộ | 0 | 10 | 20 | 30 | 50 | 70 | 90 | 100 |
ScủaNaCl | 35,6 | 35,7 | 35,8 | 36,7 | 37,5 | 37,5 | 38,5 | 39,1 |
ScủaKCl | 28,5 | 32,0 | 34,7 | 42,8 | 48,3 | 48,4 | 53,8 | 56,6 |
Bước 1: Hòa tan một lượng quặng sinvinit được nghiền nhỏ vào 1000 gam nước ở 1000C, lọc bỏ phầnkhôngtanthuđượcdungdịchbãohòa.
Bước 2: Làm lạnh dung dịch bão hòa đến 00C (lượng nước không đổi) thấy tách ra m1 gam chất rắn. Tính độ dinh dưỡng của phân Kali có trong m1 gam chất rắn kết tinh trên là bao nhiêu?
(chỉ làm tròn kết quả ở phép tính cuối cùng, kết quả làm tròn đến hàng phần mười).
56,1
Methyl butanoate là ester có mùi táo, thu được khi cho butanoic acid tác dụng với methyl alcohol có mặt H2SO4 đặc làm xúc tác.
Khi thực hiện phản ứng este hoá 1 mol butanoic acid và 1 mol methyl alcohol, lượng ester lớn nhất thu được là 2/3 mol. Để đạt hiệu suất cực đại là 90% (tính theo acid) khi tiến hành ester hoá 1 mol butanoic cần số mol methyl alcohol là x mol. Giá trị của x là? (kết quả làm tròn đến hàng phần trăm)
2,93
Cho sơ đồ phản ứng sau:
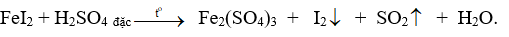
Tổng hệ số tối giản của các chất tham gia phản ứng là bao nhiêu?
8
Để trung hòa 40 mL dung dịch HCl nồng độ xM cần 50 mL dung dịch NaOH 0,2 M. Xác định giá trị của x.
0,25
Có bao nhiêu đồng phân no, mạch hở ứng với công thức phân tử C3H6O?
2
Một đèn cồn thí nghiệm chứa 100 ml cồn 900. Biết khối lượng riêng của ethanol là 0,789 g/mL và nhiệt sinh ra khi đốt cháy 1 mol ethanol là 1371 kJ.mol-1. Tính lượng nhiệt tỏa ra (kJ) khi đốt cháy hết 50% lượng cồn trong đèn?
(kết quả làm tròn đến hàng đơn vị)
1058








