Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 trường THPT Lê Quý Đôn (Nam Định) lần 1 có đáp án
28 câu hỏi
Nitric acid loãng (HNO3) không thể hiện tính oxi hóa khi tác dụng với chất nào sau đây?
FeCO3.
Cu.
FeO.
Cu(OH)2.
Cho biết sức điện động chuẩn của pin Cu-Ag là 0,459 V; thế điện cực chuẩn của các cặp Cu2+/Cu là +0,340 V; Fe2+/Fe là -0,440 V. Sức điện động chuẩn của pin Fe-Ag là
1,239 V.
0,262 V.
1,658 V.
0,581 V.
Tơ capron là loại tơ có tính dai, độ đàn hồi và độ bóng cao, ít thấm nước và được sử dụng để dệt vải may mặc. Tơ capron được tổng hợp từ caprolactam theo phương trình hóa học sau:
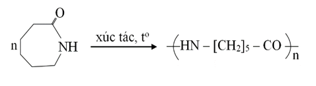
Cho các phát biểu sau:
a) Tơ capron được điều chế bằng phản ứng trùng hợp.
b) Tơ capron là tơ bán tổng hợp.
c) Phản ứng thuỷ phân hoàn toàn tơ capron trong môi trường base thuộc loại phản ứng giữ nguyên mạch polymer.
d) Do tơ capron có các nhóm –CO–NH– nên tơ capron là peptide.
Số phát biểu đúng là
3.
4.
2.
1.
Từ phổ khối lượng MS, phân tử khối của alcohol X được xác định là 46. Công thức phù hợp với X là
C3H7OH.
CH3OH.
C2H5OH.
C4H9OH.
Cho phản ứng hoá học sau: H2 (g) + I2 (g) ⇌ 2HI (g). Biểu thức hằng số cân bằng (KC) của phản ứng trên l
\({{\rm{K}}_{\rm{C}}} = \frac{{2\left[ {{\rm{HI}}} \right]}}{{\left[ {{{\rm{I}}_2}} \right]\left[ {{{\rm{H}}_2}} \right]}}\).
\({{\rm{K}}_{\rm{C}}} = \frac{{\left[ {{{\rm{H}}_2}} \right]\left[ {{{\rm{I}}_2}} \right]}}{{{{\left[ {{\rm{HI}}} \right]}^2}}}\).
\({{\rm{K}}_{\rm{C}}} = \frac{{\left[ {{{\rm{H}}_2}} \right]\left[ {{{\rm{I}}_2}} \right]}}{{2\left[ {{\rm{HI}}} \right]}}\).
\({{\rm{K}}_{\rm{C}}} = \frac{{{{\left[ {{\rm{HI}}} \right]}^2}}}{{\left[ {{{\rm{H}}_2}} \right]\left[ {{{\rm{I}}_2}} \right]}}\).
Thủy phân hoàn toàn 1 mol pentapeptide X mạch hở, thu được 3 mol glycine, 1 mol alanine và 1 mol valine. Mặt khác, thủy phân không hoàn toàn X, thu được hỗn hợp sản phẩm trong đó có Ala-Gly, Gly-Ala, Gly-Gly-Val. Cấu tạo của X là
Ala-Gly-Gly-Val-Gly.
Gly-Gly-Ala-Gly-Val.
Gly-Ala-Gly-Gly-Val.
Gly-Gly-Val-Gly-Ala.
Số đồng phân cấu tạo ester có công thức phân tử C4H8O2 là
4.
2.
3.
5.
Để mạ bạc (Ag) cho chiếc bình bằng thép, người ta điện phân dung dịch chứa AgNO3 với anode là thanh bạc Ag và bình thép nối với cathode. Ở cathode xảy ra quá trình nào sau đây?
2H2O → 4H+ + O2 + 4e
Ag+ + 1e → Ag.
2H+ + 2e → H2.
Ag → Ag+ + 1e.
Ethylene là một trong những hóa chất quan trọng, có nhiều ứng dụng trọng đời sống: kích thích quả mau chín, điều chế nhựa làm sản phẩm gia dụng,… Phản ứng hóa học của ethylene với dung dịch Br2 như sau:
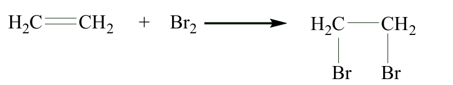
Cơ chế của phản ứng trên xảy ra như sau:
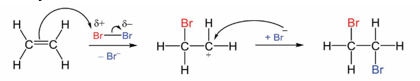
Nhận định nào sau đây không đúng?
Giai đoạn 1, liên kết đôi phản ứng với tác nhân Br-tạo thành phần tử mang điện dương.
Hiện tượng của phản ứng là dung dịch bromine bị nhạt màu.
Phản ứng trên thuộc loại phản ứng cộng.
Giai đoạn 2, phần tử mang điện dương kết hợp với anion Br- tạo thành sản phẩm.
Tên gọi của ester CH3COOCH3 là
ethyl acetate.
ethyl formate.
methyl propionate.
methyl acetate.
Chất nào sau đây chứa liên kết ion?
CH4.
HCl.
NaCl.
N2.
Một loại chất béo trung tính có chứa 75% tristearin về khối lượng (còn lại là các tạp chất trơ). Để sản xuất 3000 bánh xà phòng cần dùng tối thiểu x kg loại chất béo trên cho phản ứng với dung dịch NaOH, đun nóng. Biết rằng trong mỗi bánh xà phòng có chứa 70 gam sodium stearate. Giá trị của x gần nhất với giá trị nào sau đây?
230.
271.
229.
247.
Trong các hợp chất sau, chất nào là hợp chất hữu cơ?
Na2CO3.
CH3COOH.
Al4C3.
CO2.
Số nguyên tử oxygen trong phân tử glutamic acid là
1.
2.
4.
3.
Polymer nào sau đây có chứa nguyên tố chlorine?
PP.
PVC.
PE
PS
Trong quá trình điện phân KCl nóng chảy với các điện cực trơ, ở anode xảy ra quá trình
oxi hóa ion Cl-.
khử ion Cl-.
khử ion K+.
oxi hóa ion K+.
Xăng sinh học E5 (chứa 5% ethanol về thể tích) dùng làm nhiên liệu sạch, được sản xuất thông qua quá trình lên men các chất hữu cơ như tinh bột, cellulose. Thể tích xăng E5 thu được từ một tấn mùn cưa chứa 45% cellulose về khối lượng là (biết hiệu suất cả quá trình đạt 70% và khối lượng riêng của ethanol là 0,789 gam/ml).
9254,2 lít.
4534,6 lít.
5368,4 lít.
4307,8 lít.
Nguyên tử sodium (Na) có số hiệu nguyên tử Z = 11. Cấu hình electron của nguyên tử sodium là
1s22s22p63s1.
1s22s22p63s23p1.
1s22s22p5.
1s22s22p63s2.
Saccharose monolaurate là một trong những chất phụ gia có chức năng kép do khả năng nhũ hóa và hoạt tính kháng khuẩn của nó. Saccharose monolaurate là hợp chất thu được khi cho saccharose tác dụng với lauric acid.
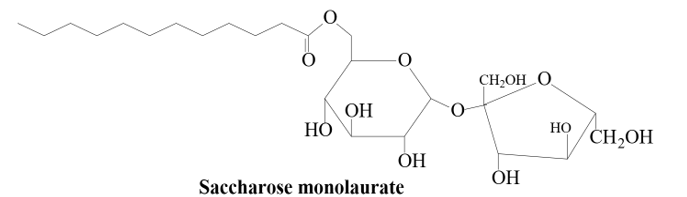
Lauric acid là một carboxylic acid no, đơn chức, mạch hở không phân nhánh.
Từ 400 gam saccharose và 80 gam lauric acid, với hiệu suất phản ứng đạt 47%, có thể điều chế được tối đa 98,512 gam saccharose monolaurate.
Saccharose có phản ứng với thuốc thử Tollens.
Trong phân tử saccharose có chứa liên kết α- 1,2- glycoside.
Hợp chất hữu cơ X mạch hở, công thức phân tử là C3H6O và phổ IR của chất X như sau:
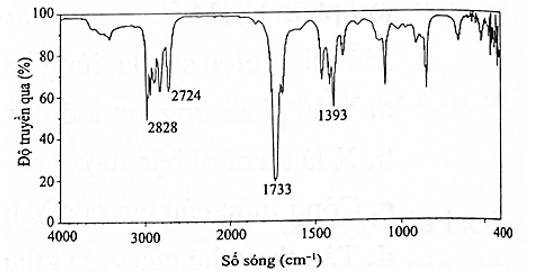
Chất X phản ứng với iodine trong môi trường kiềm tạo ra kết tủa iodoform.
Chất X có phản ứng tráng bạc.
Chất X bị khử bằng LiAlH4 tạo ra alcohol bậc một.
Tên thay thế của X là allyl alcohol.
Thiết lập một pin điện hóa có cấu tạo như hình sau:
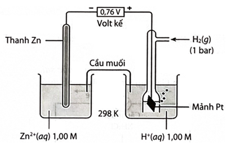
Sức điện động chuẩn của pin là \(0,76\;{\rm{V}}\).
Hai cặp oxi hóa - khử của pin là \({\rm{Z}}{{\rm{n}}^{2 + }}/{\rm{Zn}}\) và \({\rm{P}}{{\rm{t}}^{2 + }}/{\rm{Pt}}\).
Phản ứng hóa học xảy ra trong pin là: 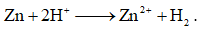
Tại anode xảy ra quá trình: 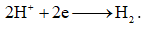
Aniline là một trong nguyên liệu quan trong để tổng hợp phẩm nhuộm, chất hoạt động bề mặt và nhiều ứng dụng khác. Aniline được điều chế theo sơ đồ sau:
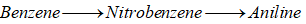
Aniline có tính base, dung dịch aniline làm quỳ tím chuyển màu xanh.
Để phân biệt hai chất lỏng aniline và benzene ta có thể dùng nước bromine.
Để sản xuất được 200 kg aniline theo sơ đồ trên cần 179,4 kg benzene với hiệu suất chung cả quá trình là 85%.
Aniline là amine bậc 1, thuộc aryl amine.
Các dạng tồn tại của glutamic acid ứng với giá trị pH được thể hiện ở bảng sau:
Dạng tồn tại | 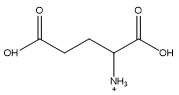 | 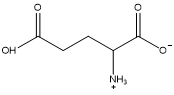 | 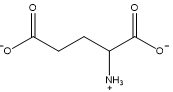 | 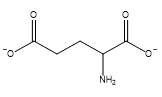 |
pH | 1,5 | 3,22 | 6,96 | 11,5 |
Giá trị pH của dung dịch bằng bao nhiêu thì glutamic acid di chuyển về cực âm trong điện trường?
1,5
Omega-3 là nhóm axit béo thiết yếu gồm DHA, EPA và ALA, cơ thể không tự tạo ra được. Omega-3 giúp tốt cho tim mạch, não bộ, thị lực, giảm viêm; có nhiều trong cá béo, hạt lanh, hạt chia hoặc thực phẩm bổ sung. Cho một số acid béo thường gặp dưới đây:
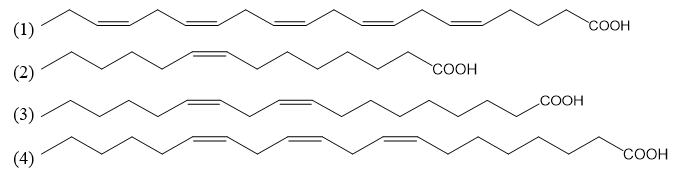
Có bao nhiêu acid béo thuộc nhóm omega-3 ?
1
Nổ bụi là vụ nổ gây ra bởi quá trình bốc cháy nhanh của các hạt bụi mịn phân tán trong không khí bên trong một không gian hạn chế, tạo ra sóng nổ. Nổ bụi xảy ra khi có đủ năm yếu tố: nguồn oxygen, nguồn nhiệt, nhiên liệu (bụi có thể cháy được), nồng độ bụi mịn đủ lớn và không gian đủ kín. Năm 2007, một vụ nổ bụi xảy ra khi các công nhân hàn bảo trì bể chứa bột mì tại phân xưởng sản xuất bột mì ở tỉnh Bình Dương khiến 5 công nhân bị bỏng nặng. Cho các phát biểu sau:
(1) Nổ bụi là một vụ nổ vật lí.
(2) Vụ nổ bụi xảy ra khi có đủ các yếu tố nguồn oxygen, nguồn nhiệt, không gian đủ kín.
(3) Nhiên liệu trong vụ nổ bụi tại phân xưởng bột mì ở Bình Dương là bụi bột mì.
(4) Bụi càng mịn khả năng gây nổ càng cao do phát tán nhanh và dễ lơ lửng trong không khí.
Liệt kê các phát biểu đúng theo thứ tự tăng dần (VD :123, 134..)
34
Tiến hành thí nghiệm về phản ứng của protein:
Bước 1: Ống nghiệm 1: cho khoảng 1 mL dung dịch HNO3 đặc vào ống nghiệm.
Bước 2: Ống nghiệm 2: cho khoảng 1 mL dung dịch NaOH 30% vào ống nghiệm, nhỏ thêm 3-4 giọt dung dịch CuSO4 2%, lắc đều.
Bước 3: Cho khoảng 1 mL lòng trắng trứng vào ống nghiệm 1; cho khoảng 1 mL dung dịch lòng trắng trứng vào ống nghiệm 2, khuấy đều.
Cho các phát biểu sau:
1) Sau bước 3, ở ống nghiệm 1 xuất hiện kết tủa màu vàng.
2) Sau bước 3, ở ống nghiệm 2 có dung dịch màu tím được tạo thành
3) Thí nghiệm ở ống nghiệm 1 nếu thay dung dịch HNO3 đặc bằng dung dịch HCl đặc thì hiện tượng quan sát được sau bước 3 là như nhau.
4) Thí nghiệm ở ống nghiệm 2 có thể dùng để phân biệt dung dịch lòng trắng trứng với dung dịch đường saccharose.
Liệt kê các phát biểu đúng theo thứ tự tăng dần (VD :123, 134..)
124
Sodium là kim loại nhẹ, được sản xuất trong công nghiệp bằng cách điện phân muối ăn nóng chảy ở nhiệt độ khoản 800°C. Sơ đồ bình điện phân được mô tả như hình bên
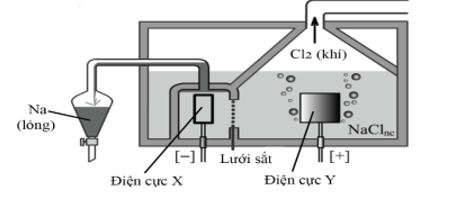
Cho các phát biểu sau:
1) Trong quá trình sản xuất sodium, người ta sử dụng điện cực X làm bằng than chì, điện cực Y làm bằng kim loại Fe.
2) Hệ thống ống dẫn sodium và bình thu sodium nóng chảy luôn được đặt trong môi trường khí trơ.
3) Hệ thống thu kim loại sodium được lắp đặt phía trên bề mặt bình điện phân do sodium là kim loại nhẹ nổi lên trên.
4) Với một quy mô sản xuất ở mức trung bình, người ta dùng cường độ dòng điện là 9000 A thì sau 16,0 giờ sản xuất được 49,42 kg sodium (hiệu suất của cả quá trình đạt 80%. Biết điện lượng được tính theo công thức: q = I.t = n.F. Trong đó t là thời gian (s), I là cường độ dòng điện (A), n là số mol electron trao đổi mỗi điện cực, F = 96500 C/mol. Kết quả được làm tròn đến hàng phần trăm.
Liệt kê các phát biểu đúng theo thứ tự tăng dần (VD :123, 134..)
23
Cho phản ứng đơn giản xảy ra trong bình kín: 2NO (g) + O2 (g) → 2NO2 (g); biết biểu thức tốc độ phản ứng:\[\nu {\rm{ }} = k.{C_{NO}}^2.{C_{{O_2}}}\]. Khi nồng độ NO tăng 3 lần và giữ nguyên nồng độ O2 thì tốc độ phản ứng tăng lên bao nhiêu lần?
9








