Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 trường THPT Bỉm Sơn (Thanh Hóa) lần 1 có đáp án
28 câu hỏi
Nguyên tố nào sau đây mà nguyên tử có 3 electron ở lớp ngoài cùng?
Na (Z=11).
Al (Z=13).
Cl (Z=17).
Ar (Z=18).
Cho phản ứng thuận nghịch: CaCO3(s) ⇌CaO(s) + CO2(g). Biểu thức tính hằng số cân bằng (KC) của phản ứng này là.
KC = \(\frac{{\left[ {{\rm{CaO}}} \right].\left[ {{\rm{C}}{{\rm{O}}_2}} \right]}}{{\left[ {{\rm{CaC}}{{\rm{O}}_3}} \right]}}\).
KC = \(\frac{{[{\rm{CaC}}{{\rm{O}}_3}]}}{{\left[ {{\rm{CaO}}} \right].\left[ {{\rm{C}}{{\rm{O}}_2}} \right]}}\).
KC = [CaO].[CO2].
KC = [CO2].
Dịch dạ dày (pH=2) có môi trường gì?
Acid.
Base.
Trung tính.
Lưỡng tính.
Xà phòng hóa chất nào sau đây thu được glycerol?
Methyl formate.
Benzyl acetate.
Methyl acetate.
Tristearin.
Tên gọi của CH3CH2COOCH3 là
ethyl acetate.
methyl propionate.
propyl acetate.
methyl acetate.
Người ta thường lấy lá chè xanh rửa sạch, có thể vò nhẹ, cho vào ấm rồi đổ nước sôi, ủ từ 3 – 5 phút là có thể sử dụng được làm thức uống rất tốt cho cơ thể. Cách làm này được gọi là hãm chè, dựa trên phương pháp nào sau đây?
Chiết lỏng – rắn.
Cô đặc.
Kết tinh.
Chưng cất.
Hợp chất A là một α-amino acid. Phổ MS của A xuất hiện peak của ion phân tử [M]+ có giá trị lớn nhất m/z = 89. Công thức của A là
H2NCH2COOCH3.
HCOONH3CH3.
H2NCH(CH3)COOH.
H2NCH2COOH.
Methyl amine (CH3NH2) phản ứng được với chất tan trong dung dịch nào sau đây?
HCl.
NaCl.
NaOH.
Na2CO3.
PVC là chất rắn vô định hình, cách điện tốt, bền với acid, được dùng làm vật liệu cách điện, ống dẫn nước, vải che mưa,... PVC được tổng hợp trực tiếp từ monomer nào sau đây?
Vinyl chloride.
Propylene.
Vinyl acetate.
Acrylonitrile.
Tinh thể chất rắn X không màu, vị ngọt, dễ tan trong nước. X có nhiều nhất trong mật ong nên làm cho mật ong có vị ngọt sắc. Trong công nghiệp, thuỷ phân chất Y thu được X và Z (đồng phân của X). Y là chất nào sau đây?
Saccarose.
Maltose.
Glucose.
Fructose.
Trong phòng thí nghiệm, dung dịch chất nào sau đây phù hợp để kiểm tra sự có mặt của ion SO42–(aq)?
NaCl.
NaNO3.
BaCl2.
HCl.
Hiện tượng phú dưỡng là một hiện tượng của môi trường ao, hồ bị ô nhiễm do dư thừa các chất dinh dưỡng. Sự dư thừa dinh dưỡng chủ yếu do hàm lượng các ion nào sau đây vượt quá mức cho phép?
Sodium, potassium.
Camagnesium.lcium,
Ch
Chloride, sulfate.
Trong quá trình hô hấp tế bào, 1 mol glucose bị oxi hóa hoàn toàn sẽ giải phóng một năng lượng là 2880 kJ. Trong khẩu phần ăn hằng ngày của một người trưởng thành có 300 gam gạo (chứa 80% hàm lượng tinh bột). Giả sử 60% lượng tinh bột trong gạo chuyển thành glucose và toàn bộ lượng glucose này tham gia vào quá trình hô hấp tế bào. Năng lượng giải phóng từ sự oxi hóa hoàn toàn lượng glucose trên chiếm bao nhiêu phần trăm so với nhu cầu năng lượng trung bình 2000 cal/ngày của một người trưởng thành.
Cho 1cal = 4184 J. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười.)
51,6%.
30,6%.
27,6%.
38,2%.
Cho X, Y, Z, T là các chất khác nhau trong số 4 chất: CH3NH2, NH3, C6H5OH (phenol), C6H5NH2 (aniline) và các tính chất được ghi trong bảng sau:
Chất | X | Y | Z | T |
Nhiệt độ sôi (oC) | 182 | 184 | -6,7 | -33,4 |
pH (dung dịch nồng độ 0,001M) | 6,48 | 7,82 | 10,81 | 10,12 |
Nhận xét nào sau đây đúng?
Y là C6H5OH.
T là NH3.
Z là C6H5NH2.
X là NH3.
Cho hình vẽ sau của amino acid X trong môi trường pH = 6 dưới tác dụng của điện trường: (Cho điểm đẳng điện của các chất Glycine; Alanine; Lysine; Glutamic acid lần lượt là 5,97; 6,0; 9,8 và 3,2)

X có thể là
Glycine.
Alanine.
Lysine.
Glutamic acid.
Dãy kim loại nào sau đây không tác dụng được với HNO3 đặc, nguội?
Mg, Al.
Al, Zn.
Al, Fe.
Al, Cu.
Cho phản ứng: 2Mg(s) + CO2(g) → 2MgO(s) + C(g)
Biết nhiệt tạo thành chuẩn (\[\Delta _f^{}H_{298}^o\]) của MgO(s) và CO2(g) lần lượt là –601,8 kJ/mol và –393,5 kJ/mol.
Biến thiên enthalpy của phản ứng ở điều kiện chuẩn là
+208,3 kJ.
–208,3 kJ.
+810,1 kJ
–810,1 kJ.
Cho thế điện cực chuẩn của các cặp oxi hóa – khử sau:
\({\rm{E}}_{{\rm{MnO}}_4^ - /{\rm{M}}{{\rm{n}}^{2 + }}}^{\rm{o}} = + 1,51{\rm{ V}}\)và \({\rm{E}}_{{\rm{F}}{{\rm{e}}^{{\rm{3 + }}}}{\rm{/F}}{{\rm{e}}^{2 + }}}^{\rm{o}} = + 0,77{\rm{ V}}\)
Phát biểu nào sau đây sai?
MnO4- có tính oxi hóa mạnh hơn Fe3+.
ion Fe2+ có thể bị oxi hóa bởi ion MnO4-.
Khi cho Fe(NO3)3 vào dung dịch KMnO4, quá trình khử xảy ra là: \({\rm{F}}{{\rm{e}}^{3 + }}(aq) + 1e \to {\rm{F}}{{\rm{e}}^{2 + }}(aq)\).
ion MnO4- có khả năng oxi hóa ion Fe2+ trong dung dịch thành ion Fe3+.
Cho các phát biểu sau về peptide T có công thức cấu tạo dưới đây:
H2N-CH(CH3)-CO-NH-CH2-CO-NH-CH(CH3)-COOH
Peptide T là dipeptide vì có chứa 2 liên kết peptide.
Peptide T có phản ứng màu biuret.
Peptide T tác dụng đủ với dung dịch NaOH theo tỉ lệ mol 1:3.
Khi đun nóng peptide T với dung dịch acid hoặc kiềm dư sẽ xảy ra phản ứng thủy phân thu được 3 muối khác nhau.
Isoamyl acetate có mùi chuối nên được dùng làm hương liệu nhân tạo. Trong ngành sơn, isoamyl acetate được dùng làm dung môi vecni, dung môi sơn mài,... Isoamyl acetate được điều chế theo các bước sau:
Bước 1. Cho vào bình cầu 15 mL isoamyl alcohol (d = 0,81g/mL); 10 mL acetic acid (d = 1,049g/mL) và 7,0 ml H2SO4 đậm đặc, cho thêm vào bình vài viên đá bọt. Lắp ống sinh hàn hồi lưu thẳng đứng miệng bình cầu. Sau đó đun nóng bình cầu trong khoảng 1 giờ.
Bước 2. Sau khi đun, để nguội rồi rót sản phẩm vào phễu chiết, lắc đều rồi để yên khoảng 5 phút, chất lỏng tách thành hai lớp, loại bỏ phần chất lỏng phía dưới, lấy phần chất lỏng phía trên.
Bước 3. Cho từ từ dung dịch Na2CO3 10% vào phần chất lỏng thu lấy ở bước 2 và lắc đều cho đến khi không còn khí thoát ra, thêm tiếp 20 mL dung dịch NaCl bão hoà rồi để yên khi đó chất lỏng tách thành hai lớp.
Isoamyl acetate rất ít tan trong nước và có khối lượng riêng nhỏ hơn khối lượng riêng của nước.
Thêm dung dịch Na2CO3 ở bước 3 nhằm mục đích loại bỏ acid lẫn trong isoamyl acetate.
Sử dụng phương pháp kết tinh để tách isoamyl acetate ra khỏi hỗn hợp sau phản ứng.
Nếu hiệu suất phản ứng ester hoá là 60% và lượng isoamyl acetate bị hao hụt mất 5% trong quá trình tách ester thì khối lượng ester thu được 10,23 gam. (Làm tròn kết quả đến hàng phần trăm).
Trong một pin điện hoá xảy ra phản ứng oxi hoá - khử sau:Fe + Ni2+ ® Fe2+ + Ni
Thanh Ni là cực dương và xảy ra quá trình khử.
Các electron chuyển từ thanh Fe sang thanh Ni qua cầu muối.
Tính oxi hoá của Ni2+ lớn hơn của Fe2+.
Nồng độ của Ni2+ giảm thì sức điện động của pin cũng giảm.
Cho sơ đồ điều chế sulfuric acid từ quặng pyrite theo 3 giai đoạn như sau:
FeS2 \(\mathop \to \limits^{\left( 1 \right)} \) SO2\(\mathop \to \limits^{\left( 2 \right)} \) SO3\(\mathop \to \limits^{\left( 3 \right)} \) H2SO4
Có thể thay thế quặng pyrite bằng khoáng vật sulfua.
Sản xuất sulfuric acid theo qui trình trên gọi là phương pháp tiếp xúc.
Ở giai đoạn 3 người ta dùng nước để hấp thụ SO3, sản phẩm thu được gọi là oleum.
Oleum Z (H2SO4.nSO3) được tạo thành khi cho 100 kg dung dịch H2SO4 98% hấp thụ hoàn toàn 20 kg SO3. Phần trăm khối lượng SO3 trong Z là b%. Giá trị của b = 9,3. (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười.)
Cho biết:
Cặp oxi hoá – khử | Cu2+/Cu | Ag+/Ag | Fe2+/Fe | Ni2+/Ni |
Thế điện cực chuẩn, V | +0,340 | +0,799 | –0,44 | –0,257 |
Trong các kim loại Cu, Ag, Fe và Ni. Số kim loại khử được ion H+ trong dung dịch ở điều kiện chuẩn là bao nhiêu?
2
Xà phòng, chất giặt rửa được dùng để loại bỏ các vết bẩn bấm trên quần áo, bề mặt các vật dụng. Cho công thức của muối (X) sau:
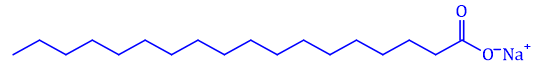
Cho các phát biểu sau:
(1) Muối X có trong thành phần chính của xà phòng và có tên là sodium palmitate.
(2) Khối lượng của 1 phân tử X là 306.
(3) Phân tử X gồm phần phân cực (đuôi dài kị nước là gốc hydrocarbon) và phần không phân cực (đầu ưa nước là nhóm carboxylate).
(4) Trong quá trình sản xuất xà phòng, có thể thêm vào muối X một số chất phụ gia như chất độn, chất tạo màu, chất tạo hương, chất dưỡng da, chất diệt khuẩn,...
Liệt kê phát biểu đúng theo thứ tự tăng dần. (123; 134...)
24
Adrenaline là hormone dẫn truyền thần kinh chủ yếu được tiết ra bởi tuyến thượng thận. Nó đóng vai trò quan trọng trong phản ứng “chiến hoặc chạy” của cơ thể, nhanh chóng chuẩn bị cơ thể đối mặt với các tình huống căng thẳng hoặc nguy hiểm.
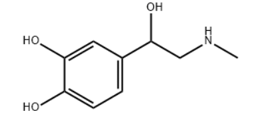
Có bao nhiêu loại nhóm chức có trong phân tử Adrenaline?
3
Các chất X, Y, Z là các hợp chất hữu cơ (đều chứa nguyên tố oxygen trong phân tử) thỏa mãn sơ đồ sau:
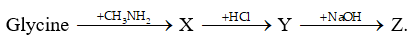
Biết Z là hợp chất ở trạng thái rắn ở điều kiện thường. Phân tử khối của Z là bao nhiêu?
97
Tại nhiều làng nghề thủ công mỹ nghệ, sulfur dioxide được dùng làm chất chống mốc cho các sản phẩm mây tre đan. Trung bình trong một ngày làng nghề đốt cháy 12 kg sulfur để tạo sulfur dioxide làm chất chống nấm mốc cho đũa dùng một lần. Giả thiết chỉ có 20% lượng khí SO2 được sử dụng, phần dư sẽ bay vào khí quyển và chuyển hoá hết thành H2SO4 gây ra hiện tượng mưa acid. Nồng độ mol/L ion H+ có trong 1m3 nước mưa nói trên là bao nhiêu? (Làm tròn kết quả đến hàng phần mười)
0,6
Ammonia có nhiều ứng dụng quan trọng như sản xuất phân đạm, nitric acid, làm dung môi. Hiện nay người ta sản xuất ammonia bằng cách chuyển hoá có xúc tác một hỗn hợp gồm không khí, hơi nước và khí methane (thành phần chính của khí thiên nhiên) theo quy trình Haber.
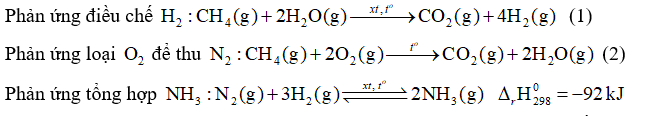
Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí methane theo phương trình hóa học (2). Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của methane là \(100\% \). Biết \(80\% \) lương nhiệt tỏa ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành \(\left( {{\Delta _f}{\rm{H}}_{298}^0} \right)\) của các chất ở điều kiện chuẩn được cho trong bảng sau:
Chất | \({\rm{C}}{{\rm{H}}_4}\left( {{\rm{\;g}}} \right)\) | \({\rm{C}}{{\rm{O}}_2}\left( {{\rm{\;g}}} \right)\) | \({{\rm{H}}_2}{\rm{O}}\left( {\rm{g}} \right)\) |
\(\left( {{\rm{\Delta f}}{{\rm{H}}_{298}}{\;^0}\left( {{\rm{\;kJ\;mo}}{{\rm{l}}^{ - 1}}} \right)} \right.\) | \( - 74,6\) | \( - 393,5\) | \( - 241,8\) |
Để sản xuất được 0,36 tấn khí hydrogen trong giai đoạn trên cần dùng m tấn khí methane. Giá trị của m là?
(Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười)
0,9








