Đề thi thử Tốt nghiệp THPT Hóa học 2025 - 2026 trường THPT Nguyễn Khuyến (Bình Dương) tháng 11 có đáp án
28 câu hỏi
Kim loại dẫn điện tốt nhất là
Au.
Ag.
Al..
Cu
Chromium được sử dụng để cắt thuỷ tinh có thể được giải thích dựa vào tính chất vật lí nào?
Tính cứng.
Tính dẫn điện.
Tính dẻo.
Tính dẫn nhiệt.
Chất nào sau đây thuộc loại ester?
CH3COOC2H5.
CH3COOH.
H2N-CH2-COOH.
CH3CHO.
Trong nước, thế điện cực chuẩn của cặp oxi hóa – khử Mn+/M càng lớn thì dạng khử có tính khử ...(1)… và dạng oxi hóa có tính oxi hóa ...(2)… Các cụm từ cần điền vào (1) và (2) lần lượt là
càng mạnh và càng yếu.
càng yếu và càng yếu.
càng mạnh và càng mạnh.
càng yếu và càng mạnh.
Nguyên tố natri (sodium, Na) có số hiệu nguyên tử là 11. Ở trạng thái cơ bản, cấu hình electron của ion Na+ là
1s22s22p5.
1s22s22p6.
1s22s22p63s1.
1s22s22p63s2.
Sốnguyên tử oxygen trong phân tử peptide Gly-Ala-Val-Gly là
4.
5.
6.
8.
Xét phản ứng: Ag+(aq) + Fe2+(aq) → Ag(s) + Fe3+ (aq). Cặp oxi hoá - khử của sắt trong phản ứng là
Fe2+/Fe.
Fe2+/Fe3+.
Fe3+/Fe2+.
Fe3+/Fe.
Trùng hợp monomer CH2=CH-Cl thu được chất dẻo nào sau đây?
PE.
PP.
PVC.
PS.
Khi điện phân MgCl2 nóng chảy (điện cực trơ), ở anode xảy ra
sự khử ion Cl–.
sự khử ion Mg2+.
sự oxi hóa ion Mg2+.
sự oxi hóa ion Cl–.
Trong cơ thể chất béo bị oxi hóa thành các chất nào sau đây ?
NH3 và CO2.
H2O và CO2.
NH3 và H2O.
NH3, CO2 và H2O
Tơ nào sau đây thuộc loại tơ thiên nhiên?
Tơ nylon-6,6.
Tơ visco.
Tơ tằm.
Tơ nitron.
Một loại chất giặt rửa tổng hợp có thành phần chính là muối sau:
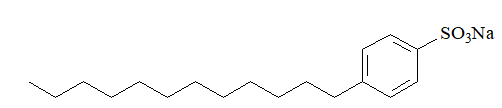
Phần kị nước trong muối trên có bao nhiêu nguyên tử carbon ?
12.
6.
18.
14.
Ở điều kiện chuẩn, thiết lập được điện cực zinc (Zn) bằng cách nhúng thanh Zn vào dung dịch
ZnSO4 0,1 M.
ZnSO4 1 M.
H2SO4 1 M.
NaCl 1 M.
Nhận xét nào sau đây đúng?
Polymer thường nóng chảy ở một nhiệt độ xác định.
Polyamide, polysaccharide đều bị cắt mạch trong môi trường acid.
Đun nóng polystyrene ở nhiệt độ cao mạch polymer không bị biến đổi.
Đun nóng cao su với bột lưu huỳnh (sulfur) thu được cao su buna -S.
Phát biểu nào sau đây là sai?
Cho dung dịch lòng trắng trứng vào Cu(OH)2/OH- thấy xuất hiện màu vàng.
Dung dịch lysine làm xanh quỳ tím.
Aniline tác dụng với nước bromine tạo thành kết tủa trắng.
Dung dịch glycine không làm đổi màu quỳ tím.
Điện phân dung dịch CuSO₄ (anode graphite), ở anode xảy ra quá trình:
2H₂O + 2e → H₂ + 2OH⁻.
2H₂O → 4H⁺ + O₂ + 4e.
Cu²⁺ + 2e → Cu.
Cu → Cu²⁺ + 2e.
Cho sức điện động chuẩn của các pin điện hoá: \(E_{Pin(T - X)}^o = 2,46{\rm{ V}}\); \(E_{Pin(T - Y)}^o = 2,00{\rm{ V}}\) (với X, Y, T là kim loại). Khi pin điện hóa X-Y làm việc ở điều kiện chuẩn, nhận định nào sau đây là đúng?
Y được tạo ra ở cực dương, X được tạo ra ở cực âm.
Y được tạo ra ở cực dương, Xn+ được tạo ra ở cực âm.
Yn+ được tạo ra ở cực âm và X được tạo ra ở cực dương.
Yn+ được tạo ra ở cực âm và Xn+ được tạo ra ở cực dương.
Hằng ngày, cơ thể chúng ta cần cung cấp nhiều thực phẩm có nguồn gốc là carbohydrate như tinh bột, saccharose, glucose, fructose, cellulose…. Cho các phát biểu về các carbohydrate như sau:
a) Glucose phản ứng với methanol khi có mặt HCl khan tạo thành ammonium gluconate.
b) Cellulose và tinh bột đều là các polysaccharide có phân tử khối rất lớn, nhưng phân tử khối của tinh bột lớn hơn nhiều so với cellulose.
c) Amylopectin được cấu tạo từ nhiều đơn vị α-glucose liên kết với nhau qua liên kết α-1,4-glycoside và β-1,6-glycoside hình thành cấu tạo mạch phân nhánh.
d) Phân tử maltose tồn tại dạng mở vòng và dạng vòng, phân tử saccharose chỉ tồn tại ở dạng vòng.
e) Tất cả các loại carbohydrate được liệt kê như tinh bột, saccharose, glucose, fructose, và cellulose đều được cơ thể con người tiêu hóa và hấp thụ để cung cấp năng lượng.
Số phát biểu đúng là
3.
4.
2.
1
Pin quả chanh được thiết lập gồm một dây Cu và dây Zn ghim vào một quả chanh và nối với vôn kế như hình sau:
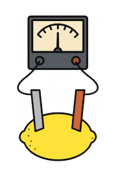
Kim vôn kế quay đồng nghĩa với sự xuất hiện dòng điện.
Tại anode của pin chanh, xảy ra quá trình: 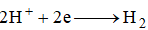
Nếu thay dây Cu bằng dây Zn thì kim vôn kế quay mạnh hơn.
Cho \[E_{Z{n^{2 + }}/Zn}^0 = - 0,763\,V;E_{C{u^{2 + }}/Cu}^0 = + 0,34\,V\]. Vậy thế điện cực chuẩn pin chanh: \[E_{Pin}^0 = 1,103\,V\].
Tiến hành thí nghiệm theo hai bước sau:
Bước 1: Cho 2 mL dung dịch NaOH 10% vào ống nghiệm. Sau đó, thêm 0,5 mL dung dịch CuSO₄ 5% vào, lắc nhẹ.
Bước 2: Cho 3 mL dung dịch saccharose 5% vào ống nghiệm trên rồi lắc đều.
Sau bước 2, kết tủa tan tạo thành phức màu xanh lam.
Ở bước 2, nếu thay saccharose bằng maltose thì hiện tượng xảy ra tương tự.
Thí nghiệm này chứng tỏ saccharose có tính chất của polyalcohol.
Sau bước 2, nếu đun nóng ống nghiệm thu được kết tủa Cu₂O màu đỏ gạch.
Cho sơ đồ điện phân dung dịch bão hòa NaCl bên dưới để điều chế NaOH, Cl2 và H2.
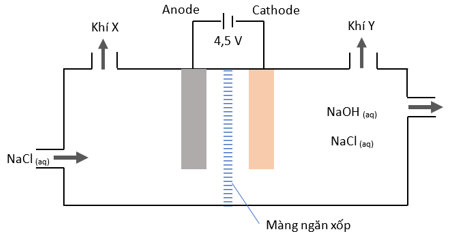
Ở anode xảy ra quá trình oxi hóa: 2Cl- ® Cl2 (g) + 2e.
Khí X trong sơ đồ trên là khí H2.
Trong quá trình điện phân, dung dịch ở khu vực cathode có pH < 7.
Nếu hiệu suất điện phân là 95%, một nhà máy với quy mô sản xuất 200 tấn xút (NaOH) mỗi ngày thì cần m tấn dung dịch NaCl bão hòa. Giá trị của m là 308. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị)
Nhựa Y là một loại chất dẻo có độ bền cơ học cao. Nhựa Y được điều chế từ hydrocarbon X. X là một hydrocarbon mạch hở, phương trình nhiệt hóa học của phản ứng cháy của X như sau:
Cho bảng năng lượng các liên kết như sau:
Liên kết | O=O | H-O | C-H | C=O | C=C | C-C |
Năng lượng liên kết (kJ/mol) | 498 | 467 | 413 | 799 | 611 | 414 |
Công thức cấu tạo của X là CH3-CH=CH2.
Nhựa Y là nhựa PE.
Nhựa Y dễ bị phân hủy trong môi trường acid.
Giá trị của a là 1852. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị)
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá - khử sau:
Cặp oxi hoá – khử | \({\rm{Z}}{{\rm{n}}^{{\rm{2 + }}}}{\rm{/Zn}}\) | \({\rm{F}}{{\rm{e}}^{{\rm{2 + }}}}{\rm{/Fe}}\) | Ag+/Ag | \({\rm{2}}{{\rm{H}}^{\rm{ + }}}{\rm{/}}{{\rm{H}}_{\rm{2}}}\) | \({\rm{C}}{{\rm{u}}^{{\rm{2 + }}}}{\rm{/Cu}}\) |
\({\rm{E}}_{{\rm{oxh/kh}}}^0\)(V) | \( - 0,763\) | \( - 0,440\) | +0,799 | 0 | \(0,340\) |
Số kim loại trong dãy (là các kim loại Zn, Ag, Fe, Cu) ở điều kiện chuẩn phản ứng được với dung dịch HCl ở điều kiện chuẩn là?
2
Cho các bước thực hiện thí nghiệm xà phòng hóa chất béo (không theo thứ tự):
(1) Thỉnh thoảng cho vài giọt nước cất để tránh hỗn hợp phản ứng bị cạn.
(2) Sau khoảng 10 phút thì dừng đun, cho thêm 10 mL dung dịch NaCl bão hòa và khuấy đều.
(3) Đun hỗn hợp sôi nhẹ và khuấy đều bằng đũa thủy tinh.
(4) Cho vào bát sứ khoảng 2 mL dầu thực vật (hoặc khoảng 2 g mỡ) và 4 – 5 mL dung dịch NaOH 40%.
Hãy sắp xếp đúng thứ tự các bước thực hiện thí nghiệm xà phòng hóa chất béo (VD: 1234, 3214,….).
4312
Kết quả phân tích nguyên tố của một α-amino acid X như sau: %C = 46,60%; %H = 8,74%; %N = 13,59% (về khối lượng); còn lại là oxygen. Bằng phổ khối lượng (MS), xác định được phân tử khối của X bằng 103. Số công thức cấu tạo thỏa mãn của X là bao nhiêu?
2
Hai cặp oxi hóa - khử Zn2+/Zn và Ni2+/Ni tạo thành pin có sức điện động chuẩn là 0,505 V, phản ứng xảy ra trong pin: Zn + Ni2+ → Zn2+ + Ni. Pin Zn - Pb có sức điện động chuẩn là 0,636 V, thế điện cực chuẩn của cặp oxi hóa – khử Pb2+/Pb là -0,126 V. Thế điện cực chuẩn của cặp Ni2+/Ni có giá trị là bao nhiêu vôn? (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần mười)
-0,3
Xăng sinh học E10 là nhiên liệu hỗn hợp (10% ethanol và 90% octane theo thể tích). Hiện nay có khoảng 40 nước trên thế giới đang sử dụng nhiên liệu này trong các động cơ đốt trong của xe. Từ nguyên liệu 1,5 tấn gỗ (có 42% cellulose về khối lượng) điều chế ethanol, sau đó lượng ethanol được tách và trộn với octane để sản xuất xăng E10. Biết hiệu suất quá trình chuyển hoá cellulose thành ethanol là 80%, trong quá trình tách và trộn để sản xuất xăng E10, lượng ethanol bị thất thoát 6%. Thể tích xăng E10 thu được là bao nhiêu lít? Cho khối lượng riêng của ethanol là 0,789 g/ml. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị.)
3410
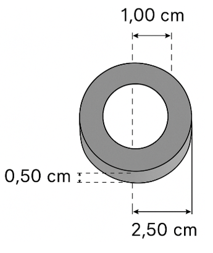
Một đồ vật được làm bằng kim loại Fe dạng hình trụ rỗng có bán kính trong là 1,00 cm, bán kính ngoài là 2,50 cm và chiều cao là 0,50 cm (hình bên).
Người ta mạ kim loại Ni cho đồ vật trên bằng cách sử dụng kim loại Ni và đồ vật này làm hai điện cực rồi nhúng vào trong dung dịch NiSO4 1 M để tiến hành điện phân. Để đạt yêu cầu về mặt kĩ thuật thì lớp kim loại Ni phải có độ dày là 0,05 mm và phủ đều trên các bề mặt của đồ vật. Biết khối lượng riêng của kim loại Ni là 8,90 g/cm³; lấy π = 3,14; F = 96500 C/mol và Ni = 59. Tính thời gian (theo phút) của quá trình mạ điện nếu sử dụng dòng điện có cường độ không đổi là 1,50 A. (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị.)
71








