Đề tham khảo ôn thi tốt nghiệp THPT môn Hóa có đáp án (Đề số 50)
28 câu hỏi
Thuỷ phân ester X trong môi trường kiềm, thu được sodium acetate và ethanol. Công thức cấu tạo của X là
CH3COOC2H5.
C2H3COOC2H5.
CH3COOCH3.
C2H5COOCH3.
Theo quy định, tất cả các loại chất lỏng, tinh dầu được coi là chất lỏng dễ cháy và là hàng hoá nguy hiểm nếu có điểm chớp cháy nhỏ hơn 60°C không được vận chuyển qua đường hàng không. Cho điểm chớp cháy của một số loại tinh dầu thường gặp như sau:
Tinh dầu | Trầm hương | Quế | Đinh hương | Tràm gió | Oải hương | Thông |
Điểm chớp cháy (°C) | 51 | 87 | 87 | 52 | 68 | 65 |
Trong các tinh dầu trên, theo quy định có bao nhiêu tinh dầu hành khách không được phép mang theo lên máy bay ?
2.
4.
5.
6.
Hợp chất hữu cơ X có công thức phân tử CxHyO. Trên phổ phổ khối lượng MS, X có giá trị lớn nhất là 60 và phổ hồng ngoại IR, X có tín hiệu hấp thụ trong vùng 3500 - 3200 cm-1. Số đồng phân cấu tạo của X là
4.
5.
3.
2.
Tinh bột là một trong những chất dinh duỡng cơ bản của người và động vật. Tinh bột thuộc loại
polysaccharide.
disaccharide.
lipid.
monosaccharide.
Cao su Buna-S (hay còn gọi là cao su SBR) là loại cao su tổng hợp được sử dụng rất phổ biến, ước tính 50% lốp xe được làm từ SBR. Thực hiện phản ứng trùng hợp các chất nào dưới đây thu được sản phẩm là cao su Buna-S?
CH2=CH-CH=CH2 và CH2=CH-CN.
CH2=CH-CH=CH2 và CH2=CH-Cl.
CH2=CH-CH=CH2 và CH2=CH-C6H5.
CH2=CH-CH=CH2 và Sulfur.
Trong phản ứng với nước bromine, aniline thể hiện phản ứng nào sau đây?
Phản ứng cộng hợp halogen vào vòng benzene.
Phản ứng cộng halogen vào nhóm -NH2.
Phản ứng thế hydrogen trên vòng benzene.
Phản ứng thế hydrogen của nhóm -NH2.
Phenylalanine (Phe) là một amino acid thiết yếu (tức là cơ thể người không tổng hợp được mà phải lấy từ thức ăn). Phenylalanine tham gia vào quá trình tổng hợp các chất dẫn truyển thẩn kinh như dopamine, norepinephrine. Phenylalanine còn là tiền chất để tổng hợp tyrosine, và được tìm thấy trong nhiều loại thực phẩm như trứng, thịt và sữa. Công thức cấu tạo thu gọn của phenylalanine như sau:
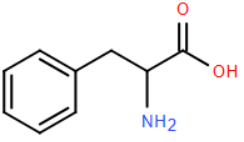
Chọn phát biểu sai về phenylalanine trong các phát biểu sau?
Ở môi trường có pH = 2, phenylalanine di chuyền về phía điện cực dương trong điện trường.
Phenylalanine là một amino acid thiết yếu có mặt trong các thực phẩm chứa protein.
Phenylalanine là chất lưỡng tính.
Phenylalanine có công thức phân tử là C9H11O2N.
Cho phản ứng hoá học: Cu + 2Fe3+ → Cu2+ + 2Fe2+. Phát biểu nào sau đây về phản ứng trên không đúng?
Cu bị Fe3+ oxi hoá thành Cu2+.
Cu2+ có tính oxi hoá mạnh hơn Fe3+.
Fe3+ bị Cu khử thành Fe2+.
Cu là chất khử, Fe3+ là chất oxi hoá.
Kim loại nào sau đây thuộc nhóm IA trong bảng tuần hoàn?
Ba.
Fe.
Na.
Al.
Hầu hết các loại rau và cây ăn trái phát triển tốt nhất trong đất có độ pH từ 6,0 đến 7,0. Trong quá trình trồng trọt, nếu đất có pH = 4,5 đến 5,0 thì người nông dân sử dụng vôi sống để bón vào đất một cách hợp lý. Công thức vôi sống là
Ca(HCO3)2.
Ca(OH)2.
CaCO3.
CaO.
Nước cứng gây nhiều tác hại trong đời sống và sản xuất như đóng cặn đường ống dẫn nước, làm cho xà phòng có ít bọt khi giặt quần áo, làm giảm mùi vị thực phẩm khi nấu ăn. Nước cứng là nước có chứa nhiều các ion
Cl− và SO42-.
Mg2+ và Ca2+.
HCO3− và Cl−.
Na+ và K+.
Copper có độ tinh khiết cao có khả năng dẫn điện tốt, bền về mặt hoá học nên được sử dụng rộng rãi trong các thiết bị điện tử. Copper có độ tinh khiết cao có thể thu được từ copper có độ tinh khiết thấp qua quá trình tinh luyện bằng phương pháp:
điện phân dung dịch CuSO4 với anode làm bằng Pt và cathode là vật bằng Cu với độ tinh khiết cao.
điện phân dung dịch CuSO4 với cathode làm bằng Cu có độ tinh khiết cao và anode là vật bằng Cu với độ tinh khiết thấp.
điện phân dung dịch CuSO4 với cathode làm bằng Cu có độ tinh khiết thấp và anode là vật bằng Cu với độ tinh khiết cao.
điện phân dung dịch CuSO4 với cathode làm bằng than chì và anode là vật bằng Cu với độ tinh khiết cao.
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hoá - khử như sau:
Cặp oxi hóa - khử | Fe2+/Fe | Ni2+/Ni | Sn2+/Sn | Cu2+/Cu | Ag+/Ag |
Thế điện cực chuẩn | -0,440 | -0,257 | -0,137 | +0,340 | +0,799 |
Pin Galvani được thiết lập từ 2 cặp oxi hóa - khử trong số các cặp oxi hóa khử trên có suất điện động lớn nhất là
Ni2+/Ni và Cu2+/Cu.
Sn2+/Sn và Ag+/Ag.
Fe2+/Fe và Ag+/Ag.
Fe2+/Fe và Cu2+/Cu.
Cho peptide X có công thức cấu tạo:
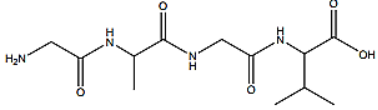
Phát biểu nào sau đây không đúng?
X có thể tham gia phản ứng với dung dịch acid HCl thu được muối.
Thủy phân hoàn toàn X trong NaOH dư thu được 4 muối.
Phân tử X có 3 liên kết peptide.
X phản ứng với Cu(OH)2 trong môi trường kiềm tạo phức chất có màu tím.
"…(1)… là vật liệu được tổ hợp từ hai hay nhiều vật liệu khác nhau, tạo nên vật liệu mới có tính chất vượt trội so với các vật liệu thành phần. Trong đó vật liệu …(2)… có vai trò đảm bảo cho các thành phần cốt của composite liên kết với nhau nhằm tạo ra tính nguyên khối và thống nhất". Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
Chất dẻo, nền.
Composite, cốt.
Chất dẻo, cốt.
Composite, nền.
Sắt (iron) được sử dụng làm lõi trong nam châm điện, chế tạo động cơ điện và máy phát điện, chế tạo biến áp, sử dụng trong thiết bị y tế (Máy MRI (Magnetic Resonance Imaging) để tạo ra từ trường mạnh, giúp chụp ảnh chi tiết bên trong cơ thể). Ứng dụng trên dựa trên tính chất nào sau đây của sắt?
Tính khử.
Tính nhiễm từ.
Tính dẫn nhiệt.
Tính dẻo.
Chất nào sau đây không phản ứng với dung dịch NaOH?
HCl.
Al2O3.
Na2CO3.
NaHCO3.
Cation [Fe(OH2)6]3+ là một phức chất có cấu tạo như hình bên:
![Cation [Fe(OH2)6]3+ là một phức chất có cấu tạo như hình bên: Phát biểu nào sau đây không đúng? (ảnh 1)](https://video.vietjack.com/upload2/quiz_source1/2025/06/blobid2-1749785154.png)
Phát biểu nào sau đây không đúng?
Liên kết giữa phối tử và nguyên tử trung tâm là liên kết cộng hóa trị.
Phức [Fe(OH2)6]3+ có dạng hình bát diện.
Trong phức chất có 6 phối tử H2O.
Nguyên tử trung tâm là nguyên tử Fe (iron).
Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Methyl cinnamate là một ester có công thức phân tử C10H10O2 và có mùi thơm của quả dâu tây (strawberry) được sử dụng trong ngành công nghiệp hương liệu và nước hoa.
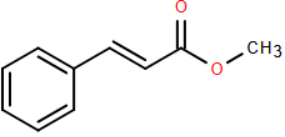
a). Methyl cinnamate phản ứng với Br2/CCl4 theo tỉ lệ 1 : 4.
b). Methyl cinnamate phản ứng với NaOH với tỉ lệ 1 : 2.
c). Methyl cinnamate có đồng phân hình học.
d). Để điều chế methyl cinnamate người ta cho cinnamic acid phản ứng với lượng dư methyl alcohol (H2SO4 đặc, đun nóng nhẹ). Đun nóng 22,2 gam cinnamic acid với methyl alcohol dư, hiệu suất phản ứng 60% thu được 14,58 gam methyl cinnamate.
Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Trong phòng thí nghiệm, một nhóm học sinh tìm hiểu phản ứng giữa kim loại đồng (copper) và dung dịch silver nitrate (AgNO3). Giả thuyết của nhóm học sinh là “khi nhúng lá đồng trong dung dịch silver nitrate, lá đồng tan bớt, có kim loại bạc (silver) bám trên lá đồng”. Để kiểm tra giả thuyết này, nhóm học sinh đã thực hiện thí nghiệm như sau :
- Cân một lá đồng, xác định được khối lượng là đồng ban đầu là 5,24 gam.
- Nhúng lá đồng vừa cân được vào dung dịch silver nitrate.
- Sau một thời gian lấy lá đồng ra, làm khô, cân lại thấy khối lượng lá đồng là 5,39 gam.
a). Đã có 0,15 gam kim loại bạc bám trên lá đồng.
b). Giả thuyết của nhóm học sinh là đúng.
c). Dung dịch từ không màu chuyển sang màu xanh.
d). Thí nghiệm trên chứng minh tính oxi hóa của ion Ag+ mạnh hơn tính oxi hóa của ion Cu2+.
Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Tiến hành thí nghiệm: Xác định hàm lượng muối Fe(II) bằng dung dịch thuốc tím.
• Bước 1: Dùng pipette hút chính xác 5 ml dung dịch FeSO4 nồng độ a mol/L cho vào bình định mức loại 50 mL. Thêm tiếp nước cất và định mức đến vạch, thu được 50 mL dung dịch Y.
• Bước 2: Dùng pipette lấy 10,0 mL dung dịch Y cho vào bình tam giác; thêm tiếp khoảng 10 mL dung dịch H2SO4 10% (lấy bằng ống đong). Cho dung dịch KMnO4 nồng độ 0,02M vào burette, mở khoá burette, nhỏ từng giọt dung dịch xuống bình tam giác, lắc đều. Ban đầu dung dịch trong bình tam giác xuất hiện màu hồng rồi mất màu. Tiếp tục chuẩn độ đến khi màu hồng tồn tại bền trong khoảng 20 giây thì dừng chuẩn độ.
Tiến hành 3 lần chuẩn độ thu được kết quả như sau :
Lần chuẩn độ | Lần 1 | Lần 2 | Lần 3 |
Thể tích KMnO4 (mL) | 8,7 | 8,9 | 8,8 |
a). Phương trình phản ứng chuẩn độ là: 10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O.
b). Điểm tương đương là lúc dung dịch xuất hiện màu hồng ổn định khoảng 20 giây.
c). Tiến hành ngược lại cho dung dịch KMnO4 vào bình tam giác, dung dịch Y vào burette chúng ta cũng thu được kết quả tương tự.
d). Giá trị của a là 0,88.
Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Một nhóm học sinh tiến hành thí nghiệm so sánh tốc độ phản ứng thủy phân của các dẫn xuất halogen khác nhau của alkane. Giả thuyết của nhóm học sinh là: “liên kết cộng hóa trị giữa nguyên tử carbon và nguyên tử halogen (kí hiệu chung là X) càng phân cực thì tốc độ phản ứng thủy phân càng lớn”. Phương trình hóa học của phản ứng thủy phân như sau:
CnH2n+1X + H2O → CnH2n+1OH + HX (∗)
Nhóm học sinh tiến hành như sau:
• Bước 1: Chuẩn bị nước nóng khoảng 50°C bằng cách đun ¾ cốc nước 250 mL. Chuẩn bị ba ống nghiệm, mỗi ống chứa 5 mL ethanol và 4 giọt lần lượt các hợp chất: 1-iodobutane, 1-bromobutane, 1-chlorobutane, có dán nhãn. Đặt các ống nghiệm này vào cốc nước để làm nóng. Cho 5 mL dung dịch AgNO3 0,05M vào ba ống nghiệm khác và cũng đặt vào cốc nước.
• Bước 2: Khi các dung dịch đã ổn định nhiệt, cho nhanh dung dịch AgNO3 0,05M vào ống nghiệm chứa 1-chlorobutane và ethanol, bấm giờ. Ghi thời gian xuất hiện kết tủa (dung dịch chuyển đục).
• Bước 3: Lặp lại bước 2 cho hai ống nghiệm chứa dung dịch dẫn xuất halogen còn lại.
Kết quả như sau:
Hợp chất | 1-iodobutane | 1-bromobutane | 1-chlorobutane |
Thời gian (giây) | 52 | 87 | 606 |
a). Từ kết quả thí nghiệm, kết luận giả thuyết của nhóm học sinh là sai.
b). Ở bước 1, đã xảy ra phản ứng hóa học (∗).
c). Độ phân cực liên kết giảm dần theo thứ tự C – Cl; C – I; C – Br.
d). Không thực hiện ngâm ống nghiệm chứa dung dịch AgNO3 0,05M vào nước nóng thì kết tủa sẽ xuất hiện sớm hơn.
Điện khí, hay còn được gọi là điện được sản xuất từ khí tự nhiên, điển hình nhất là LNG (Liquefied Natural Gas). Đầu tiên, khí tự nhiên được khai thác tại các mỏ khí, được làm sạch và làm lạnh để chuyển đổi thành khí thiên nhiên hóa lòng LNG (thuận tiện cho việc tồn trữ và vận chuyển; thành phần chứa 95% CH4, 5% C2H6 về số mol). Sau đó, LNG được vận chuyển tới các nhà máy điện khí để tạo ra điện năng. Một nhà máy điện khí có sản lượng điện 3,6.106 kWh/ngày (1 kWh = 3600 kJ), các nhiên liệu bị đốt cháy hoàn toàn (biết 60% nhiệt lượng tỏa ra của quá trình đốt cháy được chuyển hóa thành điện năng). Biết CH4, C2H6 cháy theo các phương trình:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g)
C2H6(g) + 3,5O2(g) → 2CO2(g) + 3H2O(g)
Chất | CH4(g) | C2H6(g) | CO2(g) | H2O(g) |
(kJ/mol) | -74,6 | -84,7 | -393,5 | -241,8 |
Mỗi ngày nhà máy điện khí cần sử dụng bao nhiêu tấn LNG (Chỉ làm tròn phép tính cuối, làm tròn đến hàng đơn vị)
Từ 500 tấn quặng hematite chứa 85% Fe2O3 sản xuất được x nghìn chiếc nồi gang có hàm lượng sắt là 95%. Biết rằng mỗi chiếc nồi gang nặng 5 kg và hiệu suất của toàn bộ quá trình là 80%. Giá trị của x là bao nhiêu (kết quả làm tròn đến hàng đơn vị)?
Ion Na+ là một trong những chất điện giải quan trọng trong cơ thể con người, và lượng tiêu thụ của nó có ảnh hưởng lớn đến sức khỏe. Các chuyên gia khuyến nghị rằng lượng sodium hàng ngày của một người trưởng thành không nên vượt quá 2400 mg. Bột ngọt (mì chính) là muối sodium của glutamic acid với công thức C5H8NO4Na. Hỏi khi tiêu thụ 1,0 g bột ngọt, lượng natri trong đó tương đương với bao nhiêu gam muối ăn (NaCl)? (làm tròn kết quả đến hàng phần trăm)
Cho các phát biểu sau về chất béo:
(1) Dầu mỡ bôi trơn máy có chứa thành phần là chất béo.
(2️) Chất béo đều không tan trong nước nhưng tan trong dung môi hữu cơ không phân cực.
(3️) Thủy phân hoàn toàn 1 chất béo bất kì đều thu được sản phẩm là glycerol.
(4) Dầu, mỡ động thực vật chứa thành phần chính là chất béo.
(5) Việc sử dụng hoàn toàn chất béo no làm thực phẩm cho con người tốt hơn sử dụng chất béo không no.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần (ví dụ 234, 12,…)
Trong công nghiệp, nhôm được sản xuất từ quặng bauxite theo 2 giai đoạn chính:
- Giai đoạn 1: Tinh chế quặng bauxite.
- Giai đoạn 2: Điện phân Al2O3 nóng chảy (Al2O3 được trộn cùng với cryolite Na3AlF6).
Sản phẩm điện phân ở cathode là nhôm (lỏng) và ở anode là hỗn hợp khí CO2, CO. Cấu tạo bể điện phân như hình sau:
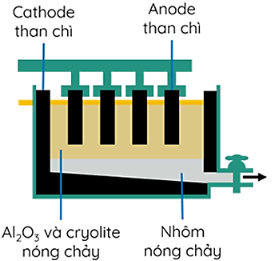
Sau một thời gian điện phân thu được 5,4 tấn Al tại cathode và hỗn hợp khí tại anode gồm CO2 (chiếm 80% theo thể tích) và CO (chiếm 20% theo thể tích). Giả thiết không có thêm sản phẩm nào được sinh ra trong quá trình điện phân. Khi đó khối lượng carbon bị oxi hóa trên anode là bao nhiêu tấn?
Một mẫu nước thải của nhà máy sản xuất có pH = 3. Để thải ra ngoài môi trường thì cần phải tăng pH lên từ 5,8 đến 8,6 (theo đúng qui định), nhà máy phải dùng vôi sống thả vào nước thải. Để nâng pH của 4 m³ nước thải từ 3 lên 7 cần dùng m gam vôi sống. Tính giá trị m. (Bỏ qua sự thủy phân của các muối, kết quả làm tròn đến hàng đơn vị).




