Bộ 3 đề thi cuối kì 2 Hóa 12 Kết nối tri thức cấu trúc mới có đáp án - Đề 1
28 câu hỏi
PHẦN I (4,5 điểm). Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Khi điện phân NaCl nóng chảy (điện cực trơ), ở cathode xảy ra?
Sự khử ion Cl−.
Sự oxi hóa ion Cl−.
Sự oxi hóa ion Na+.
Sự khử ion Na+.
Điện phân dung dịch chất nào sau đây (dùng điện cực trơ), thu được dung dịch có khả năng làm quỳ tím chuyển sang màu đỏ?
NaBr.
NaCl.
CuSO4.
CuCl2.
Trong quá trình mạ bạc cho một chiếc vòng bằng thép thì ở anode xảy ra quá trình
Ag → \[{\rm{A}}{{\rm{g}}^{\rm{ + }}}\]+ 1e.
Fe → \[{\rm{F}}{{\rm{e}}^{{\rm{2 + }}}}\]+ 2e.
2H2O → 4\[{{\rm{H}}^{\rm{ + }}}\]+ O2 + 4e.
C → \[{{\rm{C}}^{{\rm{4 + }}}}\]+ 4e.
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
sự góp chung electron của các nguyên tử kim loại cạnh nhau.
lực hút tĩnh điện giữa các electron hóa trị ở các nút mạng với các ion dương kim loại chuyển động tự do.
lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại chuyển động tự do trong toàn bộ mạng tinh thể.
lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại ở các nút mạng.
Kim loại X là kim loại nhẹ, dẫn điện tốt và có lớp màng oxide bền vững bảo vệ nên được sử dụng rộng rãi làm dây dẫn điện ngoài trời. Kim loại X là
sắt.
bạc.
đồng.
nhôm.
Một mẫu kim loại Cu có lẫn tạp chất là các kim loại Al, Mg. Để loại bỏ tạp chất thì dùng dung dịch nào sau đây?
NaOH.
Cu(NO3)2.
Fe(NO3)3.
Fe(NO3)2.
Cho khí CO (dư) đi qua ống sứ nung nóng đựng hỗn hợp X gồm Al2O3, MgO, Fe3O4 và CuO, thu được chất rắn Y. Cho Y vào dung dịch NaOH dư, khuấy kĩ, thấy còn lại phần không tan Z. Giả sử các phản ứng xảy ra hoàn toàn. Phần không tan Z gồm
Mg, Fe, Cu.
Mg, Al, Fe, Cu.
MgO, Fe, Cu.
MgO, Fe3O4, Cu.
Nguyên tử của các nguyên tố nhóm IA khác nhau về
số electron lớp ngoài cùng của nguyên tử.
cấu hình electron nguyên tử.
số oxi hóa của nguyên tử trong hợp chất.
kiểu mạng tinh thể của đơn chất.
Soda là hoá chất quan trọng trong sản xuất thuỷ tinh, bột giặt, phẩm nhuộm, giấy, sợi. Công thức hoá học của soda là
NaCl.
\({\rm{N}}{{\rm{a}}_2}{\rm{S}}{{\rm{O}}_4}.\)
\({\rm{NaN}}{{\rm{O}}_3}.\)
\({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}.\)
Hợp chất A tan nhiều trong nước; khi được đốt cháy trên ngọn lửa đèn khí thì tạo ra ngọn lửa màu vàng; khi tan trong dung dịch hydrochloric acid tạo ra khí, khí này làm đục nước vôi trong. Hợp chất A có thể là
K2CO3.
Na2CO3.
\({\rm{CaC}}{{\rm{O}}_3}\) hoặc \({\rm{Ca}}{\left( {{\rm{HC}}{{\rm{O}}_3}} \right)_2}.\)
\({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\) hoặc \({\rm{NaHC}}{{\rm{O}}_3}.\)
Nướccứngkhônggâytáchạinàosauđây?
Làmgiảmkhảnăngtẩyrửacủaxàphòng,làm choquầnáomaumụcnát.
Gâylãngphínhiênliệuvàmấtantoàncho cácnồihơi,làmtắccácđườngốngnướcnóng.
Gâyngộđộcchonướcuống.
Làmhỏngdungdịchphachế,làmthựcphẩmlâuchínvà giảmmùivịcủathựcphẩm.
Số electron lớp ngoài cùng của các nguyên tử kim loại thuộc nhóm IIA là
3.
2.
4.
1.
Cho sơ đồ chuyển hoá sau:
CaO→+ XY→+ ZCaCO3→+ Z + XT→+ ECaSO4
Biết: X, Y, Z, T, E là các hợp chất khác nhau; mỗi mũi tên ứng với một phương trình hoá học. Các chất Z, E thoả mãn sơ đồ trên lần lượt là
Na2CO3, H2SO4.
CO2, KHSO4.
NaHCO3, Na2SO4.
CO2, BaSO4.
Trong cốc nước chứa 0,01 mol Na+; 0,02 mol Ca2+; 0,01 mol Mg2+; 0,05 mol HCO3− và 0,02 mol Cl−. Đun sôi cốc nước hồi lâu, nước thu được là
nước cứng tạm thời.
nước mềm.
nước cứng vĩnh cửu.
nước cứng toàn phần.
Trong dãy kim loại chuyển tiếp thứ nhất, hai kim loại nào sau đây đều là kim loại nhẹ (D < 5g/cm3)?
Cr, Mn.
Fe, Co.
Sc, Ti.
Ni, Cu.
Trong dãy kim loại chuyển tiếp thứ nhất, kim loại có tính dẫn điện tốt nhất là
Fe.
Ti.
Cu.
Mn.
Cho phát biểu sau: “Phức chất đơn giản thường có một ...(1)... liên kết với các phối tử bao quanh. Liên kết giữa nguyên tử trung tâm và phối tử trong phức chất là liên kết ...(2)....”. Cụm từ cần điền vào (1) và (2) lần lượt là
cation kim loại, ion.
nguyên tử kim loại, cho − nhận.
nguyên tử trung tâm, cho − nhận.
phối tử, ion.
Số lượng phối tử có trong mỗi phức chất [PtCl4]2− và [Fe(CO)5] là
4 và 5.
5 và 6.
5 và 2.
1 và 2.
PHẦN II (4 điểm). Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Trong không khí ẩm, trên bề mặt của gang, thép luôn có một lớp nước rất mỏng. Lớp nước này hoà tan khí oxygen và carbon dioxide trong khí quyển, tạo thành dung dịch chất điện li. Gang, thép có thành phần chính là sắt và carbon cùng tiếp xúc với dung dịch chất điện li tạo nên vô số pin rất nhỏ mà sắt là anode và carbon là cathode.
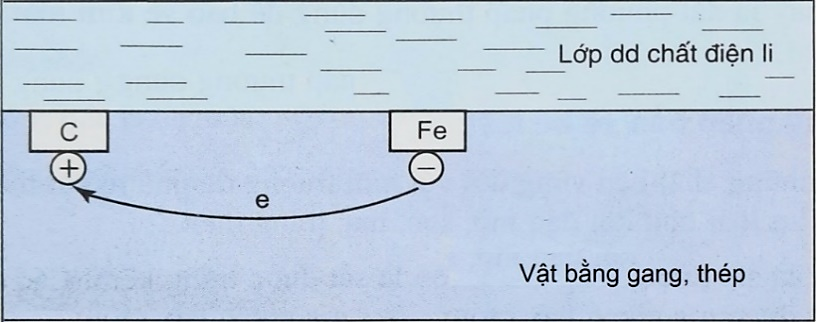
Carbon bị khử tại cathode.
Tại anode, Fe bị oxi hóa thành \(F{e^{2 + }}.\)
Oxygen đóng vai trò là chất oxi hóa.
Dạng ăn mòn hóa học là chủ yếu, do sắt dễ dàng phản ứng oxygen trong không khí.
Thực hiện thí nghiệm: Đốt muối của một số kim loại kiềm
Bước 1: Lấy mẫu muối LiCl, NaCl và KCl cho vào các chén sứ có đánh số lần lượt là 1, 2, 3.
Bước 2: Cho khoảng 3−5 mL alcohol C2H5OH nguyên chất vào mỗi chén sứ.
Bước 3: Đốt cháy các mẫu muối trong chén sứ trên.
Sau bước 3, cả 3 chén đều cháy và cho các màu ngọn lửa khác nhau.
. Sau bước 2 các mẫu muối tan một phần trong alcohol
Trình tự màu của 3 ngọn lửa lần lượt là: màu tím, màu vàng và màu đỏ tía.
Có thể dùng thí nghiệm này để nhận biết các hợp chất khác của hợp chất kim loại kiềm.
Các muối carbonate của kim loại nhóm IIA đều bị phân hủy bởi nhiệt:
MCO3(s) →tο MO (s) + CO2 (g)
Biến thiên enthalpy chuẩn của quá trình trên được cho trong bảng sau:
Muối | MgCO3 (s) | CaCO3 (s) | SrCO3 (s) | BaCO3 (s) |
∆rH˚298 (kJ) | 100,70 | 179,20 | 234,60 | 271,50 |
Phản ứng phân hủy muối carbonate của các kim loại nhóm IIA trên đều là phản ứng thuận lợi về mặt năng lượng.
Độ bền nhiệt các muối carbonate của kim loại nhóm IIA tăng dần khi số hiệu nguyên tử của M tăng dần.
Khi để vôi bột (thành phần chính là CaO) lâu ngoài không khí có hiện tượng vôi bột dần bị chuyển hóa lại thành đá vôi (thành phần chính là CaCO3).
Để sản xuất 1 tấn vôi bột theo phương pháp thủ công, người ta nung đá vôi (có hàm lượng CaCO3 là 72%, còn lại là tạp chất trơ) với than đá (giả sử chỉ chứa carbon và tạp chất trơ), biết ΔfH2980(CO2)= 393,50 kJ.mol−1. Khi đó, thể tích khí CO2 tối thiểu đã thải ra môi trường ở điều kiện chuẩn nhiều hơn 82,0 m3.
Xét phức chất [Ni(NH3)6]2+
Phức chất có thể có dạng hình học tứ diện hoặc vuông phẳng.
Liên kết trong phức chất được hình thành là do phối tử NH3 cho cặp eletron chưa liên kết vào nguyên tử trung tâm Ni+.
Nguyên tử trung tâm trong phức là Ni2+.
Điện tích của phức chất là +2.
PHẦN III (1,5 điểm). Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.Thí sinh trả lời từ câu 1 đến câu 6.
Hiện nay mạ điện được sử dụng rộng rãi trong thực tế, mạ điện là quá trình phủ một lớp kim loại lên bề mặt kim loại khác bằng phương pháp điện phân. Giả sử người tacần mạ Ag lên một mặt của một chiếc đĩa kim loại hình tròn có bán kính 20cm, độ dày lớp mạ là 0,01 mm. Nếu được cung cấp nguồn điện một chiều có cường độ dòng điện I = 2A thì thời gian cần dùng là t giờ. Biết rằng khối lượng riêng của \({\rm{Ag}}\) là \[10,5{\rm{ }}g/c{m^3};{\rm{ }}\pi {\rm{ }} = 3,14;\] hằng số Faraday (F = 96 500 C/mol); hiệu suất điện phân là 100%. Giá trị của t là bao nhiêu? (Làm tròn kết quả đến hàng phần trăm)
1,64
Tiến hành các thí nghiệm sau:
(1) Cho Mg vào lượng dư dung dịch FeCl3.
(2) Cho Ba vào lượng dư dung dịch CuSO4.
(3) Cho Zn vào dung dịch CuSO4.
(4) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3.
Số thí nghiệm thu được kim loại là?
2
NaHCO3 được sử dụng làm bột nở do dễ phân hủy thành khí và hơi tạo ra các lỗ xốp trong bánh. Nếu sử dụng 8,4 gam NaHCO3 thì có thể tạo ra tối đa bao nhiêu lít khí CO2 (đkc)? (Làm tròn kết quả đến hàng phần trăm).
1,24
Làm mềm \(10\;{{\rm{m}}^3}\) nước cứng có tổng nồng độ \({\rm{M}}{{\rm{g}}^{2 + }}\) và \({\rm{C}}{{\rm{a}}^{2 + }}\) là \(5,5{\rm{mmol}}/{\rm{L}}\) bằng \({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\), thu được nước có tổng nồng độ \({\rm{M}}{{\rm{g}}^{2 + }}\) và \({\rm{C}}{{\rm{a}}^{2 + }}\) là \(1,5{\rm{mmol}}/{\rm{L}}\). Coi toàn bộ lượng \({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\) cho vào đều chuyển hết thành kết tủa \({\rm{CaC}}{{\rm{O}}_3}\) và \({\rm{MgC}}{{\rm{O}}_3}\). Khối lượng \({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\) đã dùng là bao nhiêu kg? (Làm tròn kết quả đến hàng phần trăm)
4,24
Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (Cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023M. Thực hiện chuẩn độ 3 lần. Kết quả đạt được như sau:
Lần chuẩn độ | 1 | 2 | 3 |
V dung dịch KMnO4 (ml) | 16,0 | 16,1 | 16,0 |
Theo kết quả chuẩn độ ở trên, hãy tính độ tinh khiết (% khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr? (Làm tròn kết quả đến hàng phần mười)
99,7
Cho phức chất [PtCl4]2−, nguyên tử trung tâm Pt tạo bao nhiêu liên kết s với phối tử Cl−?
4





