Bài tập Ôn tập chương 5 có đáp án
9 câu hỏi
Hệ thống hóa kiến thức trang 89 Sách Hóa học 10: Hoàn thành các nội dung còn thiếu sau đây:
Chất phản ứng⟶ Sản phẩm, > 0 (phản ứng …?... nhiệt)
< 0 (phản ứng …?... nhiệt)
Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành (ở điều kiện chuẩn):
Tính biến thiên enthalpy của phản ứng (mà các chất đều ở thể khí) theo năng lượng liên kết (ở điều kiện chuẩn):
Phản ứng chuyển hoá giữa hai dạng đơn chất của phosphorus (P):
P (s, đỏ)⟶ P (s, trắng) ΔrH298o= 17,6 kJ
Điều này chứng tỏ phản ứng:
A. thu nhiệt, P đỏ bền hơn P trắng.
B. thu nhiệt, P trắng bền hơn P đỏ.
C. toả nhiệt, P đỏ bền hơn P trắng.
D. toả nhiệt, P trắng bền hơn P đỏ.
Cho biết biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
CO (g) + 12O2 (g) ⟶ CO2 (g) ΔrH298o = -283,0 kJ
Biết nhiệt tạo thành chuẩn của CO2: (CO2(g)) = –393,5 kJ/mol.
Nhiệt tạo thành chuẩn của CO là
–110,5 kJ.
+110,5 kJ.
–141,5 kJ.
–221,0 kJ.
Dung dịch glucose (C6H12O6) 5%, có khối lượng riêng là 1,02 g/mL, phản ứng oxi hoá 1 mol glucose tạo thành CO2(g) và H2O(l) toả ra nhiệt lượng là 2 803,0 kJ.
Một người bệnh được truyền một chai chứa 500 mL dung dịch glucose 5%. Năng lượng tối đa từ phản ứng oxi hóa hoàn toàn glucose mà bệnh nhân đó có thể nhận được là
+397,09 kJ
+381, 67 kJ
+389, 30 kJ
+416,02 kJ.
Cho giá trị trung bình của các năng lượng liên kết ở điều kiện chuẩn:
Liên kết | C – H | C – C | C = C |
Eb (kJ/mol) | 418 | 346 | 612 |
Biến thiên enthalpy của phản ứng C3H8(g) ⟶ CH4(g) + C2H4(g) có giá trị là
A. +103 kJ.
B. – 103 kJ.
C. +80 kJ.
D. – 80 kJ.
Methane là thành phần chính của khí thiên nhiên. Xét phản ứng đốt cháy methane:
CH4(g) + 2O2(g) ⟶ CO2(g) + 2H2O(l) ΔrH298o= – 890,3 kJ
Biết nhiệt tạo thành chuẩn của CO2(g) và H2O(l) tương ứng là – 393,5 và – 285,8 kJ/mol. Hãy tính nhiệt tạo thành chuẩn của khí methane.
So sánh nhiệt tỏa ra khi đốt cháy hoàn toàn 1 kg cồn (C2H5OH) và 1 kg tristearin (C57H110O6, có trong mỡ lợn). Cho biết:
C2H5OH(l) + 3O2(g) ⟶ 2CO2(g) + 3H2O(l)
ΔrH298o= – 1 365 kJ
C57H110O6(s) + O2(g) ⟶ 57 CO2(g) + 55H2O(l)
ΔrH298o = – 35 807 kJ
Biết CH3COCH3 có công thức cấu tạo:
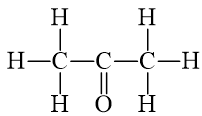
Từ số liệu năng lượng liên kết ở Bảng 12.2, hãy xác định biến thiên enthalpy của phản ứng đốt cháy acetone (CH3COCH3):
CH3COCH3(g) + 4O2(g) ⟶3CO2(g) + 3H2O(g)
Một bình gas (khí hoá lỏng) chứa hỗn hợp propane và butane với tỉ lệ số mol 1:2. Xác định nhiệt lượng toả ra khi đốt cháy hoàn toàn 12 kg khí gas trên ở điều kiện chuẩn.
Cho biết các phản ứng:
C3H8(g) +5O2(g) ⟶3CO2(g) + 4H2O(1) ΔrH298o = –2 220 kJ
C4H10(g)+ O2(g) ⟶4CO2(g) +5H2O (1) ΔrH298o = –2 874 kJ
Trung bình mỗi ngày, một hộ gia đình cần đốt gas để cung cấp 10 000 kJ nhiệt (hiệu suất hấp thụ nhiệt là 80%). Sau bao nhiêu ngày hộ gia đình trên sẽ sử dụng hết bình gas 12 kg?


