Giải SBT Hóa học 12 KNTT Bài 27: Đại cương về kim loại chuyển tiếp dãy thứ nhất có đáp án
49 câu hỏi
Kim loại nào sau đây thuộc dãy kim loại chuyển tiếp thứ nhất?
A. Ti. B. Al. C. Ba. D. Na.
Kim loại được mạ lên sắt để bảo vệ sắt và dùng để chế tạo thép không gỉ (dùng làm thìa, dao, dụng cụ y tế,…) là
A. Na. B. Mg. C. Cr. D. Ca.
Nguyên tử manganese có số oxi hóa +4 trong hợp chất nào sau đây?
A. KMnO4. B. K2MnO4. C. MnO2. D. MnSO4.
Trong hợp chất K2Cr2O7, số oxi hóa của nguyên tử Cr là
A. +6. B. +3. C. +2. D. 0.
Sắt được sử dụng để sản xuất nam châm trong các máy phát điện và nhiều thiết bị (loa, chuông, tivi, máy tính, điện thoại,…) dựa trên tính chất nào sau đây?
A. Tính dẫn điện. B. Tính dẫn nhiệt.
C. Tính dẻo. D. Tính nhiễm từ.
Đồng kim loại được sử dụng để chế tạo dây dẫn điện, thiết bị điện,.. dựa trên tính chất vật lí đặc trưng nào sau đây?
A. Dẫn điện tốt. B. Tính dẻo. C. Dẫn nhiệt tốt. D. Ánh kim.
Ở trạng thái cơ bản, cấu hình electron của nguyên tử nào sau đây có phân lớp 3d bão hòa?
A. Sc (Z = 21). B. Cu (Z = 29).
C. Ni (Z = 28). D. Mn (Z = 25).
Nguyên tố nào sau đây không thể hiện xu hướng có nhiều số oxi hóa trong hợp chất?
A. Cr. B. Mn. C. Fe. D. Mg.
Nguyên tố kim loại có trong hemoglobin làm nhiệm vụ vận chuyển oxygen, duy trì sự sống là
A. sodium. B. magnesium. C. nhôm. D. sắt.
Trong dãy kim loại chuyển tiếp thứ nhất, kim loại có độ cứng cao nhất là
A. Ti. B. Fe. C. Cr. D. Cu.
Trong dãy kim loại chuyển tiếp thứ nhất, hai kim loại nào sau đây đều là kim loại nhẹ (D < 5g/cm3)?
A. Cr, Mn. B. Fe, Co. C. Sc, Ti. D. Ni,Cu.
Cấu hình electron của nguyên tử vanadium ở trạng thái cơ bản là [Ar]3d34s2. Trong bảng tuần hoàn, nguyên tố vanadium thuộc nhóm
A. VB. B. IB. C. VIB. D. IIB.
Muối nào sau đây có khả năng làm mất màu thuốc tím trong môi trường sulfuric acid loãng?
A. Na2SO4 B. FeSO4 C. MgSO4 D. Fe2(SO4)3
Từ cấu hình electron của nguyên tử Cu ở trạng thái cơ bản là [Ar]3d104s1, xác định được cấu hình electron của ion Cu2+ là
A. [Ar]3d9. B. [Ar]3d84s1. C. [Ar]3d10. D. [Ar]3d8.
Trong dãy kim loại chuyển tiếp thứ nhất, kim loại có tính dẫn điện tốt nhất là
A. Fe. B. Ti. C. Cu. D. Mn.
Nguyên tử Cr có cấu hình electron ở trạng thái cơ bản là [Ar]3d54s1. Trong phản ứng hóa học, khi nguyên tử Cr nhường đi 3 electron để tạo thành ion Cr3+, số electron còn lại trên phân lớp 3d là
A. 5. B. 4. C. 3. D. 2.
Nguyên tố nào sau đây được mệnh danh là “nguyên tố của màu sắc” do có khả năng thể hiện màu sắc phong phú?
A. Sắt. B. Đồng. C. Nickel. D. Chromium.
Dung dịch nào sau đây có màu vàng chanh?
A. CuSO4. B. FeCl3. C. KMnO4. D. FeSO4.
Dãy kim loại nào sau đây sắp xếp theo thứ tự tăng dần nhiệt độ nóng chảy?
A. Na, Fe, Mg. B. Na, Mg, Fe. C. Fe, Mg, Na. D. Mg, Fe, Na.
Sự hình thành các nguyên tố chuyển tiếp dãy thứ nhất là do có sự sắp xếp lần lượt các electron vào phân lớp?
A. 3d. B. 4s. C. 4p. D. 3p.
Ion nào sau đây không có electron trên phân lớp 3d và không có màu trong dung dịch nước?
A. Fe3+. B. Cr3+. C. Ti3+. D. Sc3+.
Oxide nào sau đây có màu trắng?
A.Fe2O3. B. Cr2O3. C. Al2O3. D. CuO.
Ion nào sau đây vừa có khả năng thể hiện tính khử, vừa có khả năng thể hiện tính oxi hóa?
A. Cr3+ B. CrO42- C. AlO2- D. Sc3+
Nhỏ vài giọt dung dịch NaOH vào dung dịch FeCl3 thu được kết tủa có màu?
A. keo trắng. B. nâu đỏ. C. xanh lam. D. tím đen.
Trong dung dịch muối sulfate, ion kim loại nào sau đây có màu xanh?
A. Mn2+ B. Fe3+ C. Ti3+ D. Cu2+
Sắt là kim loại phổ biến thứ hai (sau nhôm) trên vỏ Trái Đất do nguyên tử sắt thuộc loại nguyên tử bền. Số neutron có trong một nguyên tử là
A. 30. B. 26. C. 56. D. 28.
Kim loại nào sau đây thể hiện hai hóa trị khi tác dụng với dung dịch HCl và khí Cl2 (toC)
A. Nhôm. B. Sắt.
C. Đồng D. Magnesium.
Hợp chất iron (III) có khả năng thể hiện tính oxi hóa khi tác dụng với chất khử. Quá trình khử ion Fe3+ được biểu diễn là
A. Fe3+ + 1e à Fe2+ B. Fe2+à Fe3+ + 1e
C. Fe2+ + 2e à Fe D. Fe à Fe2+ + 1e
Trong không khí ẩm, gang và thép bị ăn mòn điện hóa. Trong quá trình ăn mòn, sắt bị oxi hóa ở anode tạo thành ion Fe2+ theo quá trình
A. Fe2+ + 2e à Fe B. Fe à Fe2+ + 1e
C. Fe3+ + 1e à Fe2+ D. Fe2+à Fe3+ + 1e
Muối nào sau đây vừa có khả năng thể hiện tính oxi hóa (trong môi trường acid), vừa có khả năng thể hiện tính khử (trong môi trường kiềm)?
A. K2Cr2O7 B.Cr2(SO4)3 C. K2CrO4 D. Na2CrO4
Khi so sánh kim loại Fe với Ca, nhận định nào sau đây không đúng?
A. Có khối lượng riêng lớn hơn. B. Có độ cứng cao hơn.
C. Có tính khử mạnh hơn. D. Có nhiệt độ nóng chảy cao hơn.
Khi so sánh nguyên tử Ti với K, nhận định nào sau đây không đúng?
A. Có bán kính lớn hơn. B. Có số elctron hóa trị nhiều hơn.
C. Có số electron độc thân nhiều hơn. D. Có độ âm điện lớn hơn.
Trong dãy nguyên tử Sc, Ti, V, Cr bán kính nguyên tử thay đổi như thế nào?
A. Tăng dần. B. Không đổi.
C. Giảm dần. D. Không có quy luật.
Các hợp chất ứng với số oxi hóa cao nhất của Cr có tính oxi hóa mạnh. Giá trị thế điện cực chuẩn nào sau đây thuộc về cặp Cr2O72- , H+/Cr3+
A. -0.44V. B. -2,93V. C. 0V. D. +1,36V.
Trong dung dịch K2Cr2O7 tồn tại cân bằng:
Cr2O72- (da cam) + H2O ⇌ 2CrO42- (vàng) + 2H+
Cho vài giọt dung dịch chất X vào dung dịch K2Cr2O7 thì dung dịch chuyển dần từ màu da cam sang màu vàng. Chất phù hợp với X là
A. K2SO4 B. H2SO4 C. KCl D. KOH
Ở trạng thái cơ bản, nguyên tử Cr có cấu hình electron là [Ar]3d54s1
a. Nguyên tố chromium thuộc chu kì 4, nhóm VIB trong bảng tuần hoàn
b. Chromium là kim loại nhẹ, có nhiệt độ nóng chảy thấp
c. Chromium là kim loại chuyển tiếp dãy thứ nhất
d. Nguyên tử chromium có số oxi hóa cao nhất là +3 trong các hợp chất
Tiến hành các thí nghiệm xác định hàm lượng iron (II) sulfate bằng phương pháp chuẩn độ thuốc tím trong môi trường sulfuric acid loãng, dư.
a. Thuốc tím phải cho vào burette, không được cho vào bình tam giác.
b. Cần sử dụng chất chỉ thị để nhận biết điểm kết thúc chuẩn độ
c. Iron(II) sulfate là chất khử, thuốc tím là chất oxi hóa.
d. Phải đun nóng dung dịch trong bình tam giác trước khi chuẩn độ.
a. Đúng. Thuốc tím phải cho vào burette, không được cho vào bình tam giác.
b. Sai. Không cần sử dụng chất chỉ thị để nhận biết điểm kết thúc chuẩn độ do thuốc tím có màu, chỉ cần quan sát sự chuyển màu của thuốc tím.
c. Đúng. Iron(II) sulfate là chất khử, thuốc tím là chất oxi hóa.
d. Sai. Không phải đun nóng dung dịch trong bình tam giác trước khi chuẩn độ.
Ở 20oC, độ tan của CuSO4.5H2O trong nước là 32g trong 100g nước. Ở nhiệt độ này, dung dịch CuSO4 bão hòa có nồng độ là a%. Giá trị của a là bao nhiêu?
Ở điều kiện thường, tinh thể Fe có khối lượng riêng bằng 7,87g/cm3. Giả thiết các nguyên tử Fe là những hình cầu chiếm 68% thể tích tinh thể, phần còn lại là khe rỗng.
Cho biết: công thức tính thể tích hình cầu V= 43πr3
Số Avogadro NA = 6,022.1023 và số pi = 3,1416
Bán kính nguyên tử Fe là bao nhiêu pm?
Dung dịch FeCl3 có môi trường acid do sự thủy phân của ion Fe3+ theo phản ứng đơn giản hóa:
Fe3+ (aq) + H2O (l) ⇌ [Fe(OH)]2+ (aq) + H+(aq) Ka = 10-2,19
Gía trị pH của dung dịch FeCl3 0,1M là
A. 2,19 B. 1,66 C. 0,22 D.1,22
Cân bằng được duy trì ở pH = 6 (không đổi):
Cr2O72- (màu da cam) + H2O ⇌ 2CrO42- (màu vàng) + 2H+ KC = 10-15,2
Phần trăm lượng Cr2O72- ban đầu đã chuyển hóa thành CrO42- là
A. 4,2% B. 3,1% C. 3,9% D. 4,8%
Khi làm lạnh dung dịch FeCl3 thu được tinh thể FeCl3.6H2O. Cho độ tan của FeCl3.6H2O trong nước ở một số nhiệt độ như sau:
Nhiệt độ | 0 | 20 | 30 |
Độ tan | 74,4 | 91,8 | 106,8 |
Dung dịch bão hòa của FeCl3 ở 0oC có nồng độ phần trăm là
A. 22,2% B.17,4% C. 18,2% D. 25,6%
Thuốc tím dễ bị phân hủy khi bảo quản nên trước khi sử dụng thuốc tím pha sẵn cần xác định lại nồng độ bằng cách chuẩn độ với dung dịch H2C2O4. Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cân chính xác lượng oxalic acid ngậm nước (H2C2O4.2H2O, M =126,07) để pha chế được 100mL dung dịch H2C2O4 có nồng độ chuẩn 0,05M.
Bước 2: Dùng pipette hút 5mL dung dịch H2C2O4 vừa pha chế cho vào bình tam giác. Chuyển dung dịch KMnO4 nồng độ a.10-2mol/L vào burette rồi tiến hành chuẩn độ đến khi dung dịch trong bình tam giác có màu hồng nhạt bền khoảng 10 giây thì vừa hết 5,10 mL. Giá trị của a là
A.2,04 B.1,84 C.2,12 D. 1,96
Ở điều kiện thường, tinh thể K và tinh thể Cr đều có cấu trúc lập phương tâm khối. Biết một số thông số của kim loại K và Cr được cho ở bảng sau:
Tính chất | K | Cr |
Bán kính nguyên tử (pm) | 227 | 128 |
Nhiệt độ nóng chảy (oC) | 63,3 | 1900 |
Khối lượng riêng (g/cm3) | 0,862 | 7,19 |
Độ cứng (kim cương – 10) | 0,5 | 8,5 |
a) Tinh thể Cr có liên kết kim loại mạnh hơn tinh thể K
b) Trong cùng một đơn vị thể tích thì khối lượng kim loại trong tinh thể Cr và K bằng nhau
c) Nguyên tử Cr có bán kính nhỏ hơn nguyên tử K vì nguyên tử Cr có số lớp electron ít hơn.
d) K là kim loại nhẹ và Cr là kim loại nặng.
Tinh thể Cu có cấu trúc lập phương tâm mặt với cạnh của hình lập phương là 361pm như mô tả trong hình vẽ bên (biết Cu = 63,54 amu, 1amu =1,66.10-24 g).
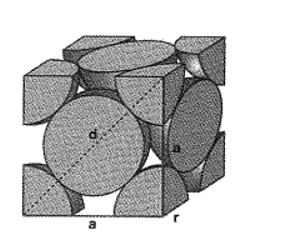
a. Bán kính của nguyên tử Cu là 128pm
b. Tổng số nguyên tử Cu có trong một hình lập phương trên bằng 6
c. Khối lượng riêng của tinh thể Cu là 8,96g/cm3
d. Các quả cầu Cu chiếm 74% thể tích trong tinh thể.
Theo QCVN 01-1:2018/BYT, hàm lượng sắt tối đa cho phép trong nước sinh hoạt là 0,3mg/L
Một mẫu nước có hàm lượng sắt cao gấp 28 lần ngưỡng cho phép, giả thiết sắt trong mẫu nước tồn tại ở dạng Fe2(SO4)3 và FeSO4 với tỉ lệ mol tương ứng là 1:8. Quá trình tách loại sắt trong 10m3 mẫu nước trên được thực hiện bằng cách sử dụng m gam vôi tôi (vừa đủ) để tăng pH, sau đó sục không khí:
Fe2(SO4)3 + Ca(OH)2 à Fe(OH)3 + CaSO4 (1)
FeSO4 + Ca(OH)2 + O2 + H2O à Fe(OH)3 + CaSO4 (2)
Giả thiết vôi tôi chỉ chứa Ca(OH)2. Giá trị của m là bao nhiêu? (Làm tròn kết quả đến phần nguyên)
Các nghiên cứu được thực hiện với một muối carbonate của kim loại M (hóa trị II)
Nghiên cứu 1: Tiến hành phân tích hàm lượng các nguyên tố, xác định M chiếm 48,28% khối lượng muối
Nghiên cứu 2: Nung nóng muối carbonate tới phản ứng hoàn toàn trong các khí quyển khác nhau:
Thí nghiệm | 1 | 2 | 3 |
Khí quyển | N2 | O2 | HCl |
Phần trăm chênh lệch giữa khối lượng mẫu chất rắn sau khi nung so với muối ban đầu ở thí nghiệm 2 là a%. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến phần nguyên)
Iron(II) sulfate thường được bảo quản ở dạng muối Mohr màu xanh nhạt có công thức FeSO4.(NH4)2SO4.nH2O
Thực hiện các thí nghiệm sau:
Thí nghiệm 1: Cân 1,96g muối Mohr rồi hòa tan vào nước, sau đó định mức trong bình 50mL. Chuẩn độ 5mL dung dịch vừa pha cần dùng 5mL dung dịch KMnO4 0,02M trong môi trường H2SO4 loãng. Xác định công thức phân tử muối Mohr.
Thí nghiệm 2: Làm lạnh 100g dung dịch muối Mohr bão hòa ở 30oC đến nhiệt độ ổn định ở 0oC thu được m gam muối Mohr kết tinh. Cho độ tan của muối Mohr trong nước ở các nhiệt độ như sau:
Nhiệt độ | 0 | 10 | 20 | 30 |
Độ tan (g/100 gam nước) | 17,2 | 31 | 36,4 | 45 |
Giá trị của m là bao nhiêu? (Làm tròn kết quả đến hàng phần mười)




