(Đúng sai) 20 bài tập Hóa 10 Kết nối tri thức Bài 17: Biến thiên enthalpy trong các phản ứng hóa học có đáp án
80 câu hỏi
Khi các phản ứng hóa học xảy ra thường có sự trao đổi nhiệt với môi trường, làm thay đổi nhiệt độ của môi trường.
a. Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
b. Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt.
c. Khi than, củi cháy không khí xung quanh ấm hơn do phản ứng tỏa nhiệt.
d. Pha viên C sủi vitamin C vào nước, khi viên C sủi tan thấy cốc nước mát hơn là do phản ứng thu nhiệt.
Mỗi phát biểu sau là đúng hay sai?
a. Biến thiên enthalpy chuẩn của một phản ứng hóa học là lượng nhiệt kèm theo phản ứng đó ở áp suất 1 atm và 25 oC.
b. Nhiệt (tỏa ra hay thu vào) kèm theo một phản ứng được thực hiện ở 1 bar và 298 K là biến thiên enthalpy chuẩn của phản ứng đó.
c. Một số phản ứng khi xảy ra làm môi trường xung quanh lạnh đi là do các phản ứng này thu nhiệt và lấy nhiệt từ môi trường.
d. Một số phản ứng khi xảy ra làm môi trường xung quanh nóng lên là phản ứng thu nhiệt.
Enthalpy tạo thành hay nhiệt tạo thành của một chất là biến thiên enthalpy của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở trạng thái bền vững, ở một điều kiện chuẩn.
a. Enthalpy tạo thành kí hiệu là ![]() .
.
b. Nhiệt tạo thành chuẩn kí hiệu là ![]() .
.
c. Enthalpy tạo thành chuẩn của các đơn chất bền vững nhất đều bằng 0.
d. Nếu ![]() , chất bền hơn về mặt năng lượng so với các đơn chất bền tạo nên nó.
, chất bền hơn về mặt năng lượng so với các đơn chất bền tạo nên nó.
Mỗi phát biểu sau đây là đúng hay sai?
a. Trong phản ứng tỏa nhiệt, dấu của ∆H dương vì năng lượng của hệ chất phản ứng nhỏ hơn năng lượng của hệ chất sản phẩm.
b. Trong phản ứng thu nhiệt, dấu của ∆H âm vì năng lượng của hệ chất phản ứng lớn hơn năng lượng của hệ chất sản phẩm.
c. Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì nhiệt lượng tỏa ra hay thu vào của phản ứng càng nhiều.
d. Các phản ứng xảy ra ở nhiệt độ phòng thường là phản ứng tỏa nhiệt, các phản ứng thu nhiệt thường xảy ra khi đun nóng.
Cho sơ đồ (a) và (b) biểu diễn enthalpy của phản ứng:
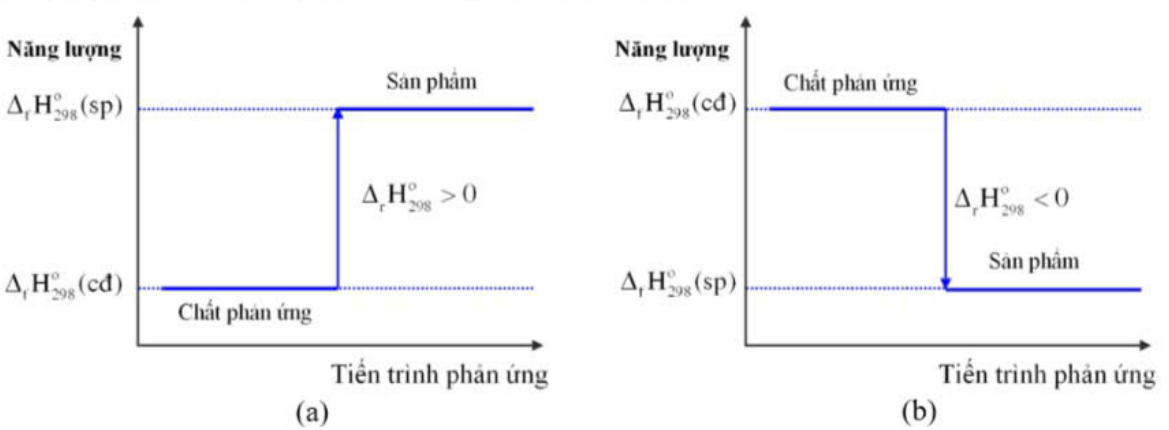
a. Sơ đồ (a) mô tả phản ứng tỏa nhiệt, sơ đồ (b) mô tả phản ứng thu nhiệt.
b. Trong sơ đồ (a), ![]() (cđ) nhỏ hơn
(cđ) nhỏ hơn ![]() (sp).
(sp).
c. Trong sơ đồ (b), ![]() (cđ) lớn hơn
(cđ) lớn hơn ![]() (sp).
(sp).
d. Các phản ứng tỏa nhiệt thường diễn ra thuận lợi hơn phản ứng thu nhiệt.
Biến thiên enthalpy chuẩn là nhiệt lượng tỏa ra hay thu vào của phản ứng ở điều kiện chuẩn.
a. Biến thiên enthalpy của phản ứng kí hiệu là ∆rH.
b. Biến thiên enthalpy chuẩn của phản ứng kí hiệu là ![]() .
.
c. Điều kiện chuẩn là điều kiện ứng với áp suất 1 bar, nồng độ 1 mol/L (đối với chất tan trong dung dịch) và nhiệt độ thường chọn là 0 °C.
d. Phản ứng đốt cháy 2 mol khí hydrogen bằng 1 mol khí oxygen, tạo thành 2 mol nước ở trạng thái lỏng, toả ra nhiệt lượng 571,6 kJ. Phản ứng trên có ![]() .
.
Cho phương trình hóa học của phản ứng:
Zn(s) + CuSO4(aq) ![]() ZnSO4(aq) + Cu(s);
ZnSO4(aq) + Cu(s); ![]()
a. Zn bị oxi hóa.
b. Phản ứng trên tỏa nhiệt.
c. Biến thiên enthalpy của phản ứng tạo thành 3,84 gam Cu là +12,6 kJ.
d. Trong quá trình phản ứng, nhiệt độ hỗn hợp tăng lên.
Phản ứng của 1 mol ethanol lỏng với oxygen xảy ra theo phương trình:
C2H5OH(l) + O2(g) ![]() CO2(g) + H2O(l)
CO2(g) + H2O(l)
a. Đây là phản ứng tỏa nhiệt vì nó tạo ra khí CO2 và nước lỏng.
b. Đây là phản ứng oxi hóa – khử với tổng hệ số cân bằng trong phương trình hóa học là 9.
c. Biến thiên enthalpy chuẩn của phản ứng sẽ thay đổi nếu nước được tạo ra ở thể khí.
d. Sản phẩm của phản ứng chiếm một thể tích lớn hơn so với chất phản ứng.
Cho phản ứng sau: S(s) + O2(g) ![]() SO2(g) và
SO2(g) và ![]()
a. ![]() là lượng nhiệt tỏa ra khi tạo ra 1 mol SO2(g) từ đơn chất S(s) và O2(g), đây là các đơn chất bền nhất ở điều kiện chuẩn.
là lượng nhiệt tỏa ra khi tạo ra 1 mol SO2(g) từ đơn chất S(s) và O2(g), đây là các đơn chất bền nhất ở điều kiện chuẩn.
b. Ở điều kiện chuẩn, ![]() .
.
c. Ở điều kiện chuẩn, ![]() .
.
d. Hợp chất SO2(g) kém bền hơn về mặt năng lượng so với các đơn chất bền S(s) và O2(g).
Cho phương trình nhiệt hóa sau: ½H2(g) + ½I2(g) ![]() HI(g);
HI(g); ![]()
a. Phản ứng trên là phản ứng thu nhiệt.
b. Ở điều kiện chuẩn, cần phải cung cấp 26,5 kJ nhiệt lượng cho quá trình 1 mol H2(g) phản ứng với 1 mol I2(s) để thu được 1 mol HI.
c. Nhiệt tạo thành chuẩn của HI(g) lớn hơn 26,5 kJ/mol.
d. Tổng enthalpy tạo thành của chất tham gia phản ứng trên nhỏ hơn tổng enthalpy của chất sản phẩm.
Cho sơ đồ sau:
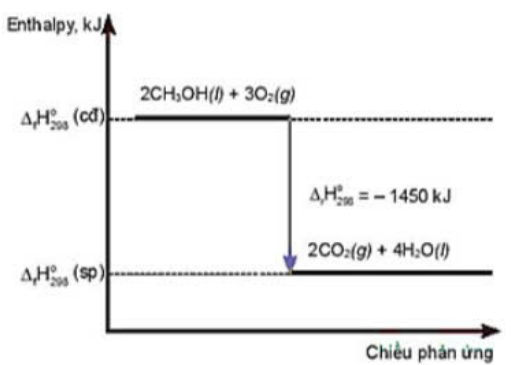
a. Phương trình nhiệt hoá học của phản ứng là: 2CH3OH(l) + 3O2(g) ![]() 2CO2(g) + 4H2O(l).
2CO2(g) + 4H2O(l).
b. Nhiệt lượng toả ra của phản ứng là 1 450 kJ.
c. Công thức tính biến thiên enthalpy của phản ứng dựa vào enthalpy tạo thành là:![]()
![]()
d. Sau phản ứng, sản phẩm có mức năng lượng cao hơn chất ban đầu.
Cho hai phản ứng cùng xảy ra ở điều kiện chuẩn:
(1) N2(g) + O2(g) ![]() 2NO(g);
2NO(g); ![]()
(2) NO(g) + ½O2(g) ![]() NO2(g);
NO2(g); ![]()
a. Enthalpy tạo thành chuẩn của NO là ½![]() (kJ.mol–1).
(kJ.mol–1).
b. Enthalpy tạo thành chuẩn của NO2 là ![]() (kJ.mol–1).
(kJ.mol–1).
c. Biến thiên enthalpy chuẩn của phản ứng giữa 1 mol N2 với 1 mol O2 tạo thành 2 mol NO là ½![]() kJ.
kJ.
d. Biến thiên enthalpy chuẩn của phản ứng giữa 1 mol khí NO với 0,5 mol khí O2 tạo thành 1 mol khí NO2 là ![]() (kJ).
(kJ).
Cho hai phản ứng cùng xảy ra ở điều kiện chuẩn:
(1) N2(g) + O2(g) ![]() 2NO(g)
2NO(g) ![]()
(2) NO(g) + 1/2O2(g) ![]() NO2(g)
NO2(g) ![]()
a. Enthalpy tạo thành chuẩn của NO2 là ![]() kJ/mol.
kJ/mol.
b. Biến thiên enthalpy chuẩn của phản ứng giữa 1 mol N2 với 1 mol O2 tạo thành 2 mol NO là 1/2![]() kJ.
kJ.
c. Biến thiên enthalpy chuẩn của phản ứng giữa 1 mol khí NO với 0,5 mol khí O2 tạo thành 1 mol khí NO2 là ![]() kJ.
kJ.
d. Enthalpy tạo thành chuẩn của NO2(g) là: 1/2![]() +
+ ![]() (kJ/mol).
(kJ/mol).
Cho phản ứng đốt cháy methane (CH4) và acetylene (C2H2) như sau:
(1) CH4(g) + 2O2(g) ![]() CO2(g) + 2H2O(l);
CO2(g) + 2H2O(l); ![]()
(2) C2H2(g) + 2O2(g) ![]() 2CO2(g) + H2O(l);
2CO2(g) + H2O(l); ![]()
a. Cả hai phản ứng trên đều là phản ứng tỏa nhiệt.
b. Khi đốt cháy cùng một lượng thể tích khí CH4 và C2H2 thì lượng nhiệt sinh ra do CH4 nhiều hơn lượng nhiệt sinh ra do C2H2.
c. Biến thiên enthalpy của phản ứng (1), (2) tính theo nhiệt tạo thành:![]()
![]()
![]()
d. Trong thực tế, để hàn, cắt kim loại người ta sử dụng CH4 mà không dùng C2H2.
Cho các phản ứng hoá học sau đây (ở điều kiện chuẩn):
(1) 2H2(g) + O2(g) ![]() 2H2O(l);
2H2O(l); ![]()
(2) CaCO3(s) ![]() CaO(s) + CO2(g);
CaO(s) + CO2(g); ![]()
(3) CaO(s) + H2O(l) ![]() Ca(OH)2(aq);
Ca(OH)2(aq); ![]()
Mỗi phát biểu sau là đúng hay sai?
a. Phản ứng (2) là phản ứng toả nhiệt.
b. Các phản ứng (1) và (3) là phản ứng toả nhiệt.
c. Về mặt năng lượng, phản ứng (3) thuận lợi hơn phản ứng (1) và (2).
d. Nhiệt tạo thành chuẩn của H2O(l) là –571,6.kJ.mol–1.
Phản ứng phân huỷ: H2O(g) ![]() H2(g) + ½O2(g);
H2(g) + ½O2(g); ![]()
Mỗi phát biểu sau là đúng hay sai?
a. Biến thiên enthalpy chuẩn của phản ứng sẽ khác đi nếu nước tham gia phản ứng ở thể lỏng.
b. Phản ứng H2(g) + ½O2(g) ![]() H2O(g) có
H2O(g) có ![]() . Đây là phản ứng tỏa nhiệt.
. Đây là phản ứng tỏa nhiệt.
c. Biến thiên enthalpy chuẩn của phản ứng 2H2O(g) ![]() 2H2(g) + O2(g) là 241,8 kJ.
2H2(g) + O2(g) là 241,8 kJ.
d. Enthalpy tạo thành chuẩn của H2O(g) bằng –241,8 kJ.mol–1.
Propene là nguyên liệu cho sản xuất nhựa polypropylene (PP). PP được sử dụng để sản xuất các sản phẩm ống, màng, dây cách điện, kéo sợi, đồ gia dụng và các sản phẩm tạo hình khác. Phản ứng tạo thành propene từ propyne:
CH3-C≡CH(g) + H2(g) ![]() CH3-CH=CH2(g); (*)
CH3-CH=CH2(g); (*)
Cho năng lượng liên kết đo ở điều kiện chuẩn của một số liên kết như sau:
Liên kết | H–H | C–H | C–C | C=C | C≡C |
Eb (kJ.mol–1) | 432 | 413 | 347 | 614 | 839 |
a. Trong hợp chất CH3-C≡CH có 4 liên kết C–H, 2 liên kết C–C, và 1 liên kết C≡C.
b. Trong hợp chất CH3-CH=CH2 có 5 liên kết C–H
c. Biến thiên enthalpy của phản ứng (*) là –184 kJ.
d. Phản ứng (*) là phản ứng tỏa nhiệt.
Cho hai phản ứng sau:
(1) N2(g) + 3H2(g) ![]() 2NH3(g)
2NH3(g)
(2) ½N2(g) + 3/2H2(g) ![]() NH3(g)
NH3(g)
Biết nhiệt tạo thành chuẩn của NH3 bằng –46 kJ/mol.
a. Phản ứng (1) là phản ứng tỏa nhiệt, phản ứng (2) là phản ứng thu nhiệt.
b. Biến thiên enthalpy của phản ứng (1) gấp 2 lần biến thiên enthalpy của phản ứng (2).
c. Phản ứng (1) thuận lợi về mặt năng lượng hơn so với phản ứng (2).
d. Khi tổng hợp từ 1 tấn NH3(g) thì nhiệt tỏa ra từ cả hai phản ứng là như nhau.
Ở điều kiện chuẩn, 2 mol nhôm tác dụng vừa đủ với khí chlorine tạo muối aluminium chloride và giải phóng một lượng nhiệt 1 390,81 kJ.
a. Phương trình nhiệt của phản ứng: 2Al(s) + 3Cl2(g) ![]() 2AlCl3(s);
2AlCl3(s); ![]() .
.
b. Nhiệt tạo thành của AlCl3(s) ở điều kiện chuẩn là 1 390,81 kJ/mol.
c. Lượng nhiệt được giải phóng khi 10 gam AlCl3 được tạo thành là 52,2 kJ.
d. Để tạo ra được 1,0 kJ nhiệt cần 0,043 gam Al phản ứng với khí chlorine.
Sulfur dioxide là một chất có nhiều ứng dụng trong công nghiệp (dùng để sản xuất sulfuric acid, tẩy trắng bột giấy trong công nghiệp giấy, tẩy trắng dung dịch đường trong sản xuất đường tinh luyện,…) và giúp ngăn cản sự phát triển của một số loại vi khuẩn và nấm gây hư hại cho thực phẩm. Ở áp suất 1 bar và nhiệt độ 25 oC, phản ứng giữa 1 mol sulfur với oxygen xảy ra theo phương trình “S(s) + O2(g) ![]() SO2(g)” và tỏa một lượng nhiệt là 296,9 kJ.
SO2(g)” và tỏa một lượng nhiệt là 296,9 kJ.
a. Enthalpy tạo thành chuẩn của sulfur dioxide bằng –296,9 kJ/mol.
b. Sulfur dioxide vừa có thể là chất khử vừa có thể là chất oxi hóa, tùy thuộc vào phản ứng mà nó tham gia.
c. 0,5 mol sulfur tác dụng hết với oxygen giải phóng 148,45 kJ năng lượng dưới dạng nhiệt.
d. 32 gam sulfur cháy hoàn toàn tỏa ra một lượng nhiệt là 2,969.105 J.








