Đề minh họa tốt nghiệp THPT môn Hóa có đáp án năm 2025 (Đề 9)
40 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Nguyên tử X có tổng số hạt mang điện là 34. Cấu hình electron của anion la
Tách kim loại kẽm bởi phương pháp nhiệt luyện được thực hiện trên theo phản ứng: Phát biểu nào sau đây là đúng?
ZnO đóng vai trò là chất khử trong phản ứng hoá học trên.
Phản ứng xảy ra ở nhiệt độ rất cao, tạo ra kẽm ở dạng hơi.
Phương pháp này còn được dùng để tách kim loại Al khỏi hợp chất
được thêm vào để làm giảm nồng độ CO giúp cân bằng dịch chuyển sang chiều thuận.
Thế điện cực chuẩn của cặp oxi hoá – khử và lần lượt là 0,771 V và 0,340 V. Nhận định nào sau đây là đúng?
Tính khử của Cu yếu hơn tính khử của ion
Tính oxi hoá của ion mạnh hơn tính oxi hoá của ion
Ở điều kiện chuẩn, ion có thể bị khử về ion bởi kim loại Cu.
Ở điều kiện chuẩn, ion có thể khử ion về Cu và bản thân nó bị oxi hoá lên
Trong các phản ứng sau, phản ứng nào làm tăng mạch polymer?
Thủy phân poly(vinyl acetate) trong môi trường kiềm.
Chlorine hóa cao su thiên nhiên để thu được chloroprene.
Phân hủy polystyrene ở
Lưu hóa cao su buna bằng lưu huỳnh.
Sự hình thành thạch nhũ trong các hang động chủ yếu là do phản ứng hóa học nào sau?
Hoá trị của nguyên tử nitrogen trong phân tử HNO3 là
V.
III.
IV.
II.
Polyethylene (PE) là polymer được dùng chế tạo màng bọc thực phẩm, túi nylon, chai đựng mỹ phẩm …. Nó được tổng hợp từ ethylene bằng phản ứng
trùng hợp.
trùng ngưng.
thế.
trao đổi.
Ứng dụng nào sau đây không phải là ứng dụng phổ biến của phức chất?
Làm chất xúc tác.
Làm chất tạo màu trong sản xuất.
Xác định hàm lượng một số kim loại trong dung dịch.
Sản xuất phân bón.
Biến thiên enthalpy chuẩn của phản ứng là . Giá trị năng lượng liên kết lần lượt là và Năng lượng liên kết N–F là
Để lợp mái nhà, các tấm tôn (là tấm thép mỏng thường được mạ kẽm) được gắn vào nhau nhờ các đinh vít bằng thép. Các tấm tôn lợp nhà thường bị gỉ sét nhanh hơn tại các vị trí cố định bằng đinh thép. Nguyên nhân của hiện tượng này là do
việc đóng đinh tạo điều kiện cho nước mưa tiếp xúc với các kim loại trong tấm tôn.
đinh thép đóng vai trò như anode làm cho việc ăn mòn diễn ra nhanh hơn.
do trong đinh thép có carbon, đóng vai trò như cathode thúc đẩy quá trình ăn mòn.
do chất lượng thép của đinh và trong tấm tôn là không đồng nhất.
Ester methyl methacrylate là nguyên liệu của công nghiệp sản xuất polymer. Phát biểu nào sau đây là không đúng?
Methyl methacrylate thuộc loại ester không no, đơn chức, mạch hở.
Công thức phân tử của methyl methacrylate là
Trùng hợp methyl methacrylate tạo ra polymer.
Methyl methacrylate làm mất màu dung dịch bromine.
Dãy các kim loại kiềm được sắp xếp theo chiều tăng dần độ cứng là
Cs < Rb < Na < Li.
Rb < Cs < K < Li.
Li < Na < K < Rb.
Cs < Na < K < Li.
Cho dung dịch riêng rẽ của các chất sau: Để phân biệt các dung dịch trên cần dùng ít nhất các thuốc thử nào sau đây?
Quỳ tím, dung dịch và nước bromine.
Quỳ tím và nước bromine.
Dung dịch và nước bromine.
Kim loại sodium, dung dịch và nước bromine.
Tyrosine (Tyr) là một amino acid tham gia vào việc sản xuất adrenaline và noradrenaline là các hormone giúp cơ thể chống lại tình huống căng thẳng bằng cách tạo ra năng lượng. Công thức cấu tạo của phân tử tyrosine như hình bên dưới.
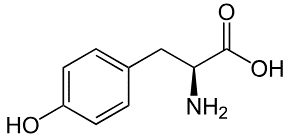
Phát biểu nào sau đây là không đúng?
Tyr là một - amino acid.
Phân tử Tyr có nhóm chức phenol.
Tyr tác dụng được với dung dịch NaOH.
Tyr không thể hiện tính lưỡng cực như các amino acid khác.
Khi bị ốm, mệt mỏi do làm việc quá sức hoặc sau các ca phẫu thuật, nhiều người bệnh thường được truyền dịch “đường” để cơ thể sớm hồi phục. Chất trong dịch truyền có tác dụng trên là
glucose.
saccharose.
amino acid.
amine.
Một số ester đơn chức mạch hở, đồng phân cấu tạo của nhau, phân tử có phần trăm khối lượng các nguyên tố C, H, O lần lượt là 54,54%; 9,10% và 36,36%. Phát biểu nào sau đây về các ester trên là không đúng?
Có 4 ester đồng phân cấu tạo của nhau.
Công thức phân tử của các ester này là
Có ít nhất 1 ester tác dụng được với nước bromine.
Trong các đồng phân ester trên, có đồng phân X thoả mãn sơ đồ phản ứng:
Trong nước, Fe3+ thường tồn tại ở dạng phức chất aqua (phức chất X) với dạng hình học là bát diện. X đóng vai trò là một acid Brønsted – Lowry khi phản ứng với nước để có thể hình thành Y, là phức chất trung hoà, không tan. Phức chất Y có công thức hoá học là
Kết quả phân tích nguyên tố trong phân tử một dipeptide X như sau: %C = 36,36%; %H = 6,06%; %N = 21,21% (về khối lượng); còn lại là oxygen. Từ phổ khối lượng, xác định được phân tử khối của X bằng 132.
Phát biểu nào sau đây về X là không đúng?
Công thức phân tử của X là
Công thức cấu tạo của X là Gly-Gly.
Dung dịch của X có môi trường acid.
Khi nhỏ dung dịch X vào dung dịch acid ở khoảng –5 °C thấy có khí không màu bay ra.
a). Dạng hình học của heme B là bát diện.
b). Mỗi phân tử hemoglobin có khả năng kết hợp tối đa với 2 phân tử O2.
c). Liên kết giữa heme B với O2 bền hơn liên kết giữa heme B với CO.
d). Heme B là phức chất có màu.
a). Dòng điện trong dây dẫn gây bởi sự chuyển động có hướng của các electron.
b). Dòng điện trong dung dịch gây bởi sự chuyển động có hướng của các ion dương và âm.
c). Thế điện cực chuẩn của là 0,76 V và của là 0,90 V.
d). Dòng electron trong pin sinh ra từ điện cực Ag.
a). Sắt, nhôm đều được sử dụng với vai trò là kim loại cơ bản trong sản xuất các hợp kim nặng.
b). Từ quặng bauxite sẽ tách được sắt bằng phương pháp nhiệt luyện, từ quặng hematite sẽ tách được nhôm bằng phương pháp điện phân.
c). Khi tráng một lớp kẽm lên đinh thép sẽ hạn chế được sự ăn mòn sắt trong thép theo phương pháp điện hoá.
d). Nhiệt độ cần để tái chế thép cao hơn nhiệt độ cần để tái chế nhôm.
a). Trong phân tử amine thơm có chứa vòng benzene.
b). Các amine bậc một tác dụng với dung dịch acid ở nhiệt độ thấp (khoảng 5 °C) tạo thành alcohol và giải phóng khí nitrogen.
c). Dung dịch của nhiều amine làm đổi màu quỳ tím thành xanh.
d). Khi cho dung dịch của amine vào dung dịch chứa ion kim loại như Mg2+, Fe3+, Cu2+... tạo được kết tủa hydroxide của kim loại tương ứng.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Cho các chất: ethyl methyl ketone, acetic aldehyde, acetone, propanal. Có bao nhiêu chất tác dụng với dung dịch iodine trong NaOH tạo được kết tủa màu vàng?
Một số amine no, đơn chức, mạch hở, trong phân tử có phần trăm khối lượng nitrogen bằng 23,73%. Có bao nhiêu chất là đồng phân tác dụng được với dung dịch acid ở nhiệt độ thích hợp sinh ra alcohol và khí nitrogen?
Chuẩn độ hàm lượng ion trong môi trường acid (chứa trong bình tam giác) bằng dung dịch đã biết nồng độ (chứa trên burette). Trong quá trình chuẩn độ, nếu dung dịch trên burette được thêm vào bình tam giác quá nhanh thì trong bình sẽ xuất hiện kết tủa nâu theo phản ứng hoá học dưới đây, dẫn đến sai lệch kết quả chuẩn độ:
Giả sử một học sinh thao tác sai, làm 60% lượng chuẩn độ chuyển thành (phần còn lại vẫn phản ứng tạo ), tổng lượng bị oxi hoá là 2,2 mmol. Thể tích dung dịch 0,020 M đã dùng tăng bao nhiêu mL so với khi chuẩn độ với thao tác phù hợp?
Một oleum có công thức Hoà tan 7,38 g oleum vào nước thành 1,0 L dung dịch sulfuric acid. Sau đó, rút 10,0 mL dung dịch acid cho vào bình tam giác, thêm vài giọt dung dịch phenolphathalein. Nhỏ từ từ dung dịch NaOH 0,10 M chứa trên burette vào bình tam giác đến khi dung dịch xuất hiện màu hồng nhạt, đọc thể tích NaOH đã dùng trên burette. Lặp lại thí nghiệm 3 lần, các giá trị thể tích NaOH đọc được lần lượt là 17,9 mL; 18,0 mL; 18,10 mL. Giá trị của n là bao nhiêu?
Trong phòng thí nghiệm, có thể điều chế lượng nhỏ và bằng phương pháp điện phân nước. Một dòng điện 1,04 A đi qua dung dịch sulfuric acid loãng trong 6,00 phút trong một thiết bị điện phân. Tổng số mol và thu được là Giá trị của n là bao nhiêu? (Kết quả làm tròn đến hàng phần trăm).
Cho biết số mol electron đi qua hệ tính theo công thức với I là cường độ dòng điện (A), t là thời gian (giây), là số Faraday.
Một nhà máy sản xuất sợi dệt nhận một đơn đặt hàng cung cấp sợi nguyên liệu nitron cho Công ty dệt may Hà Nội để hoàn thành đơn hàng áo len nam (3 size theo kích cỡ tăng dần là S, M, L), mỗi size 1 000 chiếc. Biết mỗi chiếc áo len size S cần phải dùng khoảng 500 gam sợi nitron và khối lượng len tăng thêm mỗi 10% theo mỗi size. Biết hiệu suất cả quá trình điều chế là 50%. Tính khối lượng nguyên liệu vinyl cyanide (đơn vị: tấn) cần dùng để nhà máy sản xuất được đơn hàng trên. (Kết quả làm tròn đến hàng phần mười)








