Bộ 30 đề thi học kì 1 Hóa 11 có đáp án (Đề 12)
29 câu hỏi
Muối nào sau đây là muối trung hòa?
Na2HPO4
Na2SO3
KHCO3
NH4HSO4
Để nhận biết ion PO43- người ta thường dùng dung dịch AgNO3 vì sản phẩm có
khí không màu hóa nâu trong không khí.
kết tủa màu vàng.
dung dịch màu vàng
khí màu nâu đỏ
Cho sơ đồ phản ứng sau : . Công thức hóa học của chất Y là
P2O5
PH3
P2O3
H3PO4
Phương trình ion thu gọn H+ + OH- → H2O biểu diễn bản chất của phản ứng hóa học nào sau đây ?
H2SO4 + BaCl2 → BaSO4 + 2HCl.
3HCl + Fe(OH)3 → 3FeCl3 + 3H2O.
H2SO4 + 2NaOH → Na2SO4 + 2H2O.
NaOH + NaHCO3 → Na2CO3 + H2O.
Phản ứng nào dưới đây, cacbon thể hiện tính oxi hóa
3C + 4Al Al4C3
C + O2 CO2
C + H2O CO + H2
2CuO + C 2Cu + CO2
"Nước đá khô" không nóng chảy mà thăng hoa nên được dùng để tạo môi trường lạnh và khô rất tiện cho việc bảo quản thực phẩm. Thành phần chính của nước đá khô là:
CO2 rắn
CO rắn
SO2 rắn
H2O rắn
Để điều chế chất X trong phòng thí nghiệm, người ta cho NaNO3 rắn phản ứng với H2SO4 đặc theo bình sau:
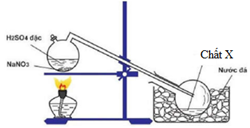
Chất X là:
H3PO4
N2
NH3
HNO3
Cho giá trị pH của một số mẫu chất lỏng sau:
Mẫu | Giấm | Sữa | Dịch dạ dày | Nước mắt |
pH | 3 | 6,5 | 1-2 | 7,4 |
Mẫu dịch lỏng nào có nồng độ ion H+ cao nhất?
Nước mắt.
Dịch dạ dày.
Giấm.
Sữa.
Chất bột X màu đen, có khả năng hấp phụ các chất khí độc nên được dùng trong nhiều loại mặt nạ phòng độc. Chất X là:
Than hoạt tính
Lưu huỳnh
Than đá
Đá vôi
Cho dung dịch AlCl3 0,2M. Nồng độ mol của ion Al3+ và Cl- lần lượt là
0,6 và 0,2
0,2 và 0,3
0,2 và 0,2
0,2 và 0,6
Chất nào sau đây là chất điện li yếu khi hòa tan trong nước ?
H2S
Ba(OH)2
HCl
Na2SO4
Chất nào sau đây là hidroxit lưỡng tính?
NaOH
Ca(OH)2
KOH
Al(OH)3
Phân đạm cung cấp nitơ cho cây trồng dưới dạng ion
NH4+ và PO43-.
NO3- và NH4+.
PO43- và K+.
K+ và NH4+.
Thuốc thử để nhận biết khí NH3 là
dung dịch NaCl
quỳ tím ẩm
dung dịch NaOH
dung dịch NaNO3
Cho dung dịch chứa 0,3 mol KOH vào dung dịch chứa 0,2 mol H3PO4 thu được dung dịch X. Các chất hòa tan có trong dung dịch X là:
K3PO4 và KOH
KH2PO4 và K2HPO4
K2HPO4 và K3PO4
KH2PO4 và K3PO4
Cặp chất nào sau đây có thể tồn tại trong một dung dịch
HCl và AgNO3
KOH và HCl
NaHCO3 và NaOH
NaCl và NH4NO3
Chất nào sau đây là chất điện li ?
Saccarozo
Benzen
Ancol etylic
Axit clohidric
Dung dịch HCl 0,01M có giá trị pH là:
12
13
2
3
Để khắc chữ trên thủy tinh (thành phần chính là SiO2) người ta dùng dung dịch chứa chất tan nào sau đây?
HF
HBr
HI
HCl
Trong phòng thí nghiệm, nito được điều chế theo phương trình nào?
2NH3 + 3CuO 3Cu + N2 + 3H2O
4NH3 + O2 2N2 + 6H2O
NH4Cl + NaNO2 NaCl + N2 + 2H2O
2NH3 + 3Cl2 → N2 + 6HCl
Trung hòa dung dịch chứa 0,2 mol NaOH cần dùng V ml dung dịch HNO3 2M. Giá trị của V là
400
300
100
200
Nhiệt phân hoàn toàn Cu(NO3)2 thu được các sản phẩm là
CuO, NO2, O2
Cu, NO2, O2
Cu(NO2)2, O2
CuO, NO2
Dung dịch nào sau đây có pH < 7?
NaCl
HCl
NaOH
NaNO3
Dung dịch nào sau đây làm quỳ tím chuyển xanh
KCl
HCl
NaOH
Na2SO4
Viết phương trình dạng phân tử và ion thu gọn của các phản ứng sau
a. BaCl2 + K2SO4 →
b. Na2CO3 + … → CO2 + … + …
Hấp thụ hoàn toàn 6,72 lít khí (đktc) khí CO2 vào 400 ml dung dịch KOH 2M. Tính nồng độ mol của các chất có trong dung dịch sau phản ứng (giả sử thể tích dung dịch không thay đổi).
Cho 1,92 gam Cu vào dung dịch HNO3 1,5M loãng lấy dư thu được V lít khí NO (đktc) và dung dịch A. Biết khí NO sinh ra là sản phẩm khử duy nhất của các phản ứng, các phản ứng xảy ra hoàn toàn.
a. Tính V
b. Cho dung dịch A tác dụng với Fe dư, thấy khối lượng Fe đã phản ứng là 2,52 gam và sinh ra khí NO. Tính thể tích dung dịch HNO3 1,5M đã dùng








