Bộ 3 đề thi giữa kì 2 Hóa 12 Kết nối tri thức cấu trúc mới có đáp án - Đề 2
28 câu hỏi
Giá trị thế điện cực chuẩn của cặp oxi hoá − khử nào được quy ước bằng 0?
Na+/Na.
2H+/H2.
Al3+/Al.
Cl2/2Cl–.
Trong số các ion: Ag+, Al3+, Na+, Mg2+, ion nào có tính oxi hoá mạnh nhất ở điều kiện chuẩn?
Na+.
Mg2+.
Ag+.
Al3+.
Điện phân dung dịch chất nào sau đây (dùng điện cực trơ), thu được dung dịch có khả năng làm quỳ tím chuyển sang màu đỏ?
NaBr.
NaCl.
CuSO4.
CuCl2.
Trong quá trình mạ bạc cho một chiếc vòng bằng thép thì ở anode xảy ra quá trình
Ag → Ag+ + 1e.
Fe → Fe2+ + 2e.
2H2O → 4H+ + O2 + 4e.
C → C4+ + 4e.
Trong mạng tinh thể kim loại, liên kết kim loại được hình thành do
sự góp chung electron của các nguyên tử kim loại cạnh nhau.
lực hút tĩnh điện giữa các electron hóa trị ở các nút mạng với các ion dương kim loại chuyển động tự do.
lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại chuyển động tự do trong toàn bộ mạng tinh thể.
lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại ở các nút mạng.
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất?
Li.
Cu.
Ag.
Hg.
Cặp chất không xảy ra phản ứng hoá học là
Cu và dung dịch FeCl3.
Fe và dung dịch HCl.
Fe và dung dịch FeCl3.
Cu và dung dịch FeCl2.
Chất nào dưới đây là thành phần chính của quặng hematite?
Iron(II) oxide.
Iron(III) oxide.
Iron.
Iron(II) sulfide.
Hợp kim nào sau đây được sử dụng để làm cấu trúc thân vỏ máy bay?
Duralumin.
Đồng thau (Brass).
Đồng thiếc (Bronze).
Manganin.
Ngâm một lá sắt trong dung dịch HCl, sắt bị ăn mòn chậm. Nếu cho thêm dung dịch CuSO4 vào dung dịch acid thì sắt bị ăn mòn
chậm hơn.
không thay đổi.
nhanh hơn.
chậm hơn rồi dừng lại.
Quặng nào sau đây có chứa nhiều nguyên tố potassium?
Pyrite.
Sylvinite.
Dolomite.
Calcite.
Kim loại Li nên được bảo quản trong
ethanol.
phenol.
khí trơ.
bình hút ẩm.
Khi điện phân dung dịch A có nồng độ nhỏ hơn 0,5 M người ta thấy độ pH của dung dịch gần một điện cực tăng dần trong quá trình điện phân. Dung dịch A là (bình điện phân có điện cực trơ và có màng ngăn xốp)
dung dịch CuSO4.
dung dịch NaCl.
dung dịch NaNO3.
dung dịch Fe(NO3)2.
Cho luồng khí CO dư qua hỗn hợp các oxide CuO, Fe2O3, Al2O3, MgO nung nóng ở nhiệt độ cao. Sau phản ứng, hỗn hợp chất rắn thu được gồm
Cu, Fe, Al, Mg.
Cu, FeO, Al2O3, MgO.
Cu, Fe, Al2O3, MgO.
Cu, Fe, Al, MgO.
Thí nghiệm nào sau đây xảy ra sự ăn mòn điện hóa học?
Nhúng thanh Cu vào dung dịch FeSO4 và H2SO4.
Nhúng thanh Fe vào dung dịch hỗn hợp CuSO4 và H2SO4.
Nhúng thanh Zn vào dung dịch HCl.
Đốt thanh Fe trong không khí.
Hợp chất A tan nhiều trong nước; khi được đốt cháy trên ngọn lửa đèn khí thì tạo ra ngọn lửa màu vàng; khi tan trong dung dịch hydrochloric acid tạo ra khí, khí này làm đục nước vôi trong. Hợp chất A có thể là
K2CO3.
Na2CO3.
CaCO3 hoặc Ca(HCO3)2.
Na2CO3 hoặc NaHCO3.
Sức điện động chuẩn của pin điện hoá H2–Cu (gồm hai điện cực ứng với hai cặp oxi hoá – khử là 2H+/H2 và Cu2+/Cu) đo được bằng vôn kế có điện trở vô cùng lớn là 0,340V. Từ đó, xác định được thế điện cực chuẩn của cặp Cu2+/ Cu là
0,340 V.
0,000 V.
0,680 V.
+0,340 V.
Cho các kim loại Na, Ca, K, Al, Fe, Cu và Zn, số kim loại tan tốt trong dung dịch KOH là
3.
4.
5.
6.
Xét pin Galvani tạo bởi hai điện cực kim loại:
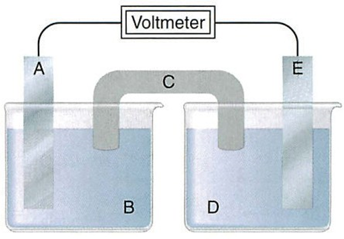
A là anode, E là cathode, C là cầu muối.
Nếu A là Zn thì B phải là ZnSO4.
Nếu C chứa KNO3 thì ion K+ được chuyển từ C vào D.
Chiều dòng điện ở mạch ngoài từ A sang E.
Ở nhiệt độ phòng, các đơn chất kim loại ở thể rắn và có cấu tạo tinh thể (trừ Hg ở thể lỏng).
Các electron nằm ở nút mạng tinh thể và các electron chuyển động tự do xung quanh.
Kiểu mạng lập phương tâm khối có độ đặc khít là 68%.
Tất các kim loại kiềm và kim loại kiềm thổ đều có kiểu mạng lập phương tâm khối nên dễ có tính khử mạnh.
Số phối trí trong kiểu mạng lập phương tâm khối là 8.
Ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim dưới tác dụng của các chất trong môi trường, trong đó kim loại bị oxi hóa.
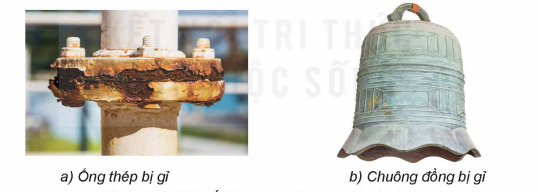
Trong quá trình ăn mòn, kim loại bị oxi hoá thành ion của nó.
Ngâm một lá nhôm trong dung dịch NaOH, xảy ra hiện tượng ăn mòn hóa học.
Bôi dầu mỡ, sơn, mạ, tráng men lên bề mặt vật dụng bằng kim loại để chống sự ăn mòn kim loại.
Sự ăn mòn vỏ tàu trong nước biển là ăn mòn hóa học.
Soda là hoá chất được sử dụng rộng rãi trong ngành công nghiệp hoá chất, hiện nay ở Việt Nam trung bình cần 5 . 1 0 5 tấn/năm. Phương pháp Solvay với nguyên liệu đầu vào là đá vôi và muối ăn nên giá thành rẻ, phù hợp với sản xuất tại Việt Nam.
Soda được dùng để làm mềm nước cứng, sản xuất thuỷ tinh, giấy, hoá chất,...
Phương pháp Solvay giảm thiểu tác động tới môi trường do tuần hoàn tái sử dụng các sản phẩm trung gian như N H 3 , C O 2 , …
Trong phương pháp Solvay, N H 3 được tái chế qua phương trình hoá học sau: 2 N H 4 C l + C a O → 2 N H 3 + C a C l 2 + H 2 O
Phương pháp Solvay chỉ xảy ra theo một giai đoạn sau: 2 N a C l + 2 N H 3 + C O 2 + H 2 O → 2 N H 4 C l + N a 2 C O 3
Hai cặp oxi hoá - khử Ni2+/Ni và Cd2+/Cd tạo thành pin có sức điện động chuẩn là 0,146 V. Phản ứng xảy ra trong pin:
Cd + Ni2+⟶Cd2+ + Ni
Thế điện cực chuẩn của cặp Cd2+/Cd có giá trị là bao nhiêu vôn? (Làm tròn kết quả đến phần trăm)
Cho biết: ở trạng thái chuẩn, pin Ni - Pb có sức điện động 0,131 V; E 0 P b 2 + / P b = − 0 , 1 2 6 V
-0,40
Điện phân dung dịch CuCl2 trong 1 giờ với dòng điện 5A. Sau điện phân, dung dịch còn CuCl2 dư. Khối lượng Cu đã sinh ra tại cathode của bình điện phân là bao nhiêu gam? (Cho Cu = 64).
5,97
Cho 8,4 gam sắt tác dụng với 6,4 gam lưu huỳnh trong bình chân không sau phản ứng thu được m gam chất rắn. Giá trị của m là
14,8
Nhôm (aluminium) được sản xuất bằng phương pháp điện phân Al2O3 tinh khiết. Quặng nhôm thường chứa thạch anh, silicate (chứa Si) và một số tạp chất khác cần được loại bỏ. Một loại quặng bauxite gồm Al2O3.3H2O và 10,0% kaolin Al2Si2O7.2H2O được dùng để sản xuất nhôm theo quy trình Bayer. Tính tỉ lệ hao hụt của nhôm trong quá trình tinh chế, biết silic thường được loại bỏ ở dạng bùn aluminosilicate (Na6Al6Si5O22.5H2O). (Làm tròn kết quả đến hàng phần trăm)
7,55
Cho các phương pháp sau:
(a) Gắn kim loại zinc vào kim loại iron.
(b) Gắn kim loại copper vào kim loại iron.
(c) Phủ một lớp sơn lên bề mặt iron.
(d) Tráng tin lên bề mặt iron.
Số phương pháp điện hóa được sử dụng để bảo vệ kim loại iron không bị ăn mòn là bao nhiêu?
1
Điện phân 2 lít dung dịch NaCl 0,5 M với điện cực trơ, màng ngăn xốp bằng dòng điện có cường độ không đổi 0,2 A. Sau 1930 giây thì dừng điện phân, thu được dung dịch X (giả thiết thể tích dung dịch không đổi). Dung dịch X có pH bằng bao nhiêu? (Làm tròn kết quả đến hàng phần mười).
11,3





