Bài tập Liên kết cộng hóa trị có đáp án
39 câu hỏi
Trong việc hình thành liên kết hóa học, không phải lúc nào các nguyên tử cũng cho, nhận electron hóa trị với nhau như trong liên kết ion. Thay vào đó, chúng có thể cùng nhau sử dụng chung các electron hóa trị để cùng thỏa mãn quy tắc octet. Trong trường hợp này, một loại liên kết hóa học mới được hình thành. Đó là loại liên kết gì?

Quan sát các Hình 10.1 đến 10.3, cho biết quy tắc octet đã được áp dụng ra sao khi các nguyên tử tham gia hình thành liên kết.
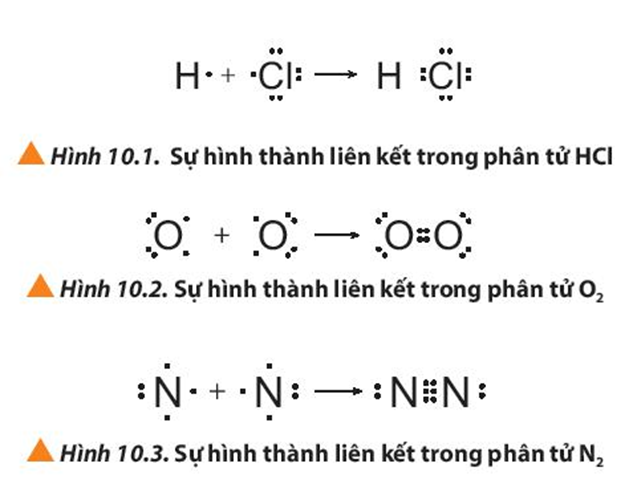
Giải thích sự hình thành liên kết trong các phân tử HCl, O2 và N2.
Thế nào là liên kết đơn, liên kết đôi và liên kết ba?
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử Cl2.
Viết công thức electron, công thức Lewis và công thức cấu tạo của Cl2, H2O, CH4.
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3.
Biết phân tử CO cũng có liên kết cho – nhận. Viết công thức electron và công thức cấu tạo của CO.
Cho biết đặc điểm của nguyên tử “cho” và nguyên tử “nhận” trong phân tử có liên kết cho – nhận.
Trình bày liên kết cho – nhận trong ion NH4+.
Vì sao liên kết cộng hóa trị trong các phân tử Cl2, O2, N2 là liên kết cộng hóa trị không phân cực?
Trong các phân tử HCl, NH3 và CO2, cặp electron chung lệch về phía nguyên tử nào? Giải thích.
Nêu thêm ví dụ về phân tử có liên kết cộng hóa trị không phân cực và liên kết cộng hóa trị phân cực. Viết công thức electron của chúng để minh họa.
Liên kết cộng hóa trị trong phân tử dạng A2 luôn là liên kết cộng hóa trị phân cực hay không phân cực? Giải thích.
Em có nhận xét gì khi cặp electron chung trong liên kết lệch hẳn về một phía nguyên tử.
Cho biết loại liên kết trong các phân tử MgCl2, CO2 và C2H4?
Quan sát các Hình từ 10.5 đến 10.8, cho biết liên kết nào trong mỗi phân tử được tạo thành bởi sự xen phủ trục hoặc xen phủ bên của các orbital.
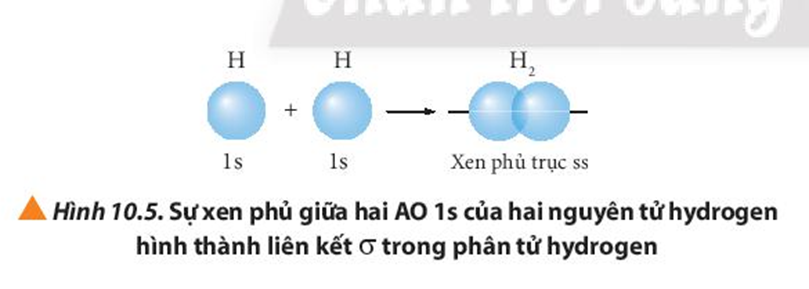
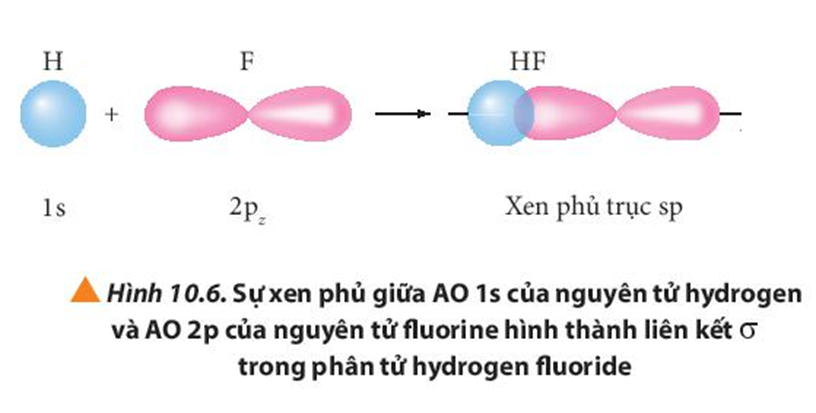
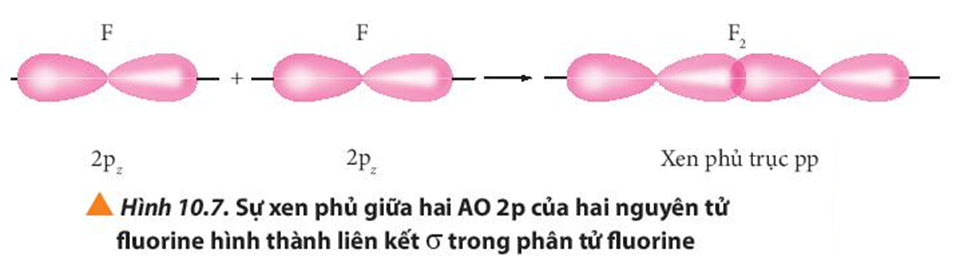
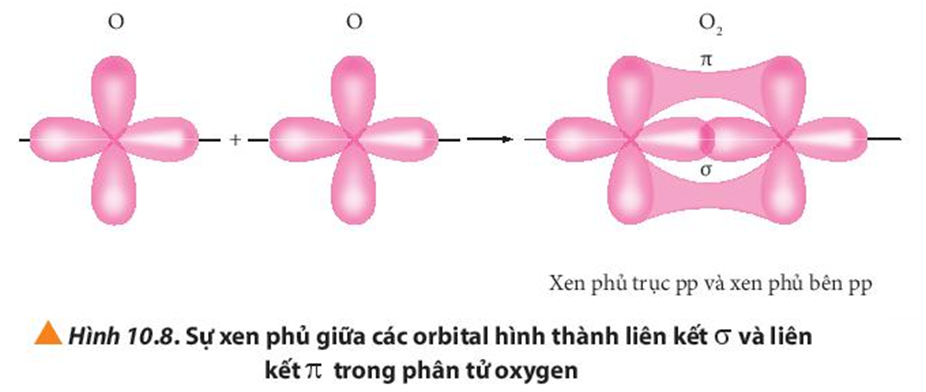
Mô tả sự hình thành liên kết σ.
Mô tả sự hình thành liên kết π.
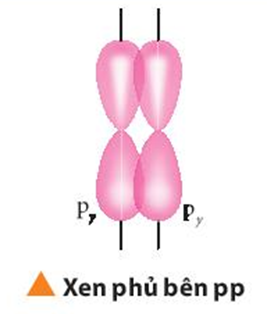
Quan sát Hình 10.8, hãy so sánh sự hình thành liên kết σ và liên kết π.
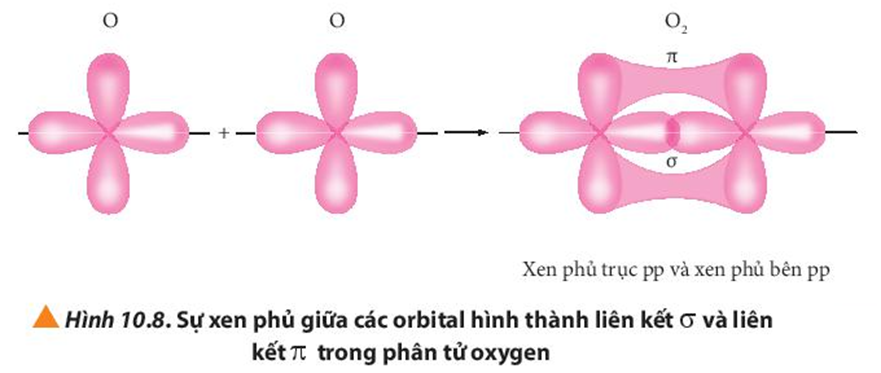
Theo em, thế nào là liên kết bội? Phân tử nào dưới đây có chứa liên kết bội: Cl2, HCl, O2 và N2?
Sự xen phủ có sự tham gia của orbital nào luôn là xen phủ trục?
Số liên kết σ và liên kết π trong mỗi liên kết đơn, liên kết đôi và liên kết ba lần lượt bằng bao nhiêu?
Vẽ sơ đồ xen phủ orbital giữa 2 nguyên tử carbon hình thành liên kết đôi trong phân tử ethylene (C2H4).
Căn cứ giá trị năng lượng liên kết H-H và N≡N đã cho, liên kết trong phân tử nào dễ bị phá vỡ hơn?
Theo em vì sao năng lượng liên kết luôn có giá trị dương?
Nitrogen chiếm khoảng 78% thể tích không khí nhưng chỉ hoạt động ở nhiệt độ cao. Vì sao nitrogen là một chất khí không hoạt động ở điều kiện thường?
Trong một số trường hợp đặc biệt, khí nitrogen được sử dụng để bơm lốp (vỏ) xe thay cho không khí là do khí oxygen có trong không khí có thể oxi hóa cao su theo thời gian. Khí nitrogen vì sao khắc phục được nhược điểm này?
Trình bày các bước trong quá trình lắp ráp mô hình phân tử NH3.
Mô hình sau biểu diễn phân tử CH4 hay phân tử CH3Cl?

Lắp ráp mô hình phân tử CH≡CH, biết toàn bộ các nguyên tử nằm trên cùng một đường thẳng.
Trong phân tử iodine (I2), mỗi nguyên tử iodine đã góp một electron để tạo cặp electron chung. Nhờ đó, mỗi nguyên tử iodine đã đạt cấu hình electron bền vững của khí hiếm nào dưới đây?
A. Xe
B. Ne
C. Ar
D. Kr
Hydrogen sulfide (H2S) và phosphine (PH3) đều là những chất có mùi khó ngửi và rất độc. Trình bày sự tạo thành liên kết cộng hóa trị trong phân tử các chất trên.
Viết công thức Lewis của các phân tử CS2, SCl2 và CCl4.
Trình bày sự hình thành liên kết cho – nhận trong phân tử sulfur dioxide (SO2).
Mô tả sự tạo thành liên kết trong phân tử chlorine bằng sự xen phủ của các AO.
Sự xen phủ giữa hai orbital p trong trường hợp nào sẽ tạo thành liên kết σ? Trong trường hợp nào sẽ tạo thành liên kết π? Cho ví dụ.
Cho biết số liên kết σ và liên kết п trong phân tử acetylene (C2H2).
Năng lượng liên kết của các hydrogen halide được liệt kê trong bảng sau:
Hydrogen halide | Năng lượng liên kết (kJ/mol) |
HF | 565 |
HCl | 427 |
HBr | 363 |
HI | 295 |
Sắp xếp theo chiều tăng dần độ bền liên kết trong các phân tử HF, HCl, HBr và HI
Gợi ý cho bạn
Xem tất cảNgân hàng đề thi

