Bài tập Enthalpy tạo thành và biến thiên enthalpy của phản ứng hóa học có đáp án
23 câu hỏi
Hầu như mọi phản ứng hóa học cũng như quá trình chuyển thể của chất luôn kèm theo sự thay đổi năng lượng.

Trong cả 2 ví dụ đều có phản ứng xảy ra với sự thay đổi năng lượng. Theo em, phản ứng có kèm theo sự thay đổi năng lượng dưới dạng nhiệt năng đóng vai trò gì trong đời sống?
Viết phương trình hóa học của phản ứng xảy ra ở Hình 13.1 và nêu nhận xét về sự thay đổi nhiệt của phản ứng đó

Thực hiện thí nghiệm 1. Nêu hiện tượng xảy ra. Rút ra kết luận về sự thay đổi nhiệt độ chất lỏng trong cốc. Giải thích.
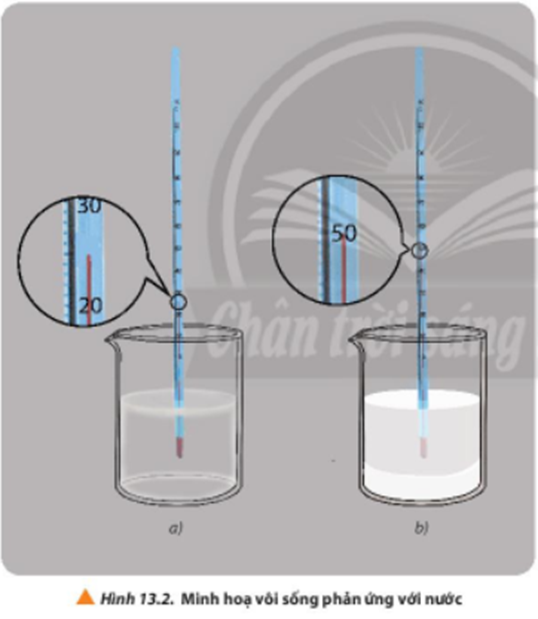
Thí nghiệm 1: Sự thay đổi nhiệt độ khi vôi sống phản ứng với nước.
Dụng cụ và thiết bị: Cốc chịu nhiệt 500 mL, cân, nhiệt kế, đũa thủy tinh, giá đỡ nhiệt kế.
Hóa chất: Vôi sống (CaO), nước cất.
Tiến hành:
Bước 1: Cho khoảng 25 mL nước cất vào cốc chịu nhiệt, đặt bầu nhiệt kế vào trong lòng chất lỏng (Hình 13.2a), ghi nhận giá trị nhiệt độ.
Bước 2: Cân khoảng 5g CaO. Cho nhanh CaO vào cốc, bắt đầu bấm giờ và ghi nhận nhiệt độ, đồng thời dùng đũa thủy tinh khuấy nhẹ (Hình 13.2b).
Bước 3: Ghi nhận giá trị nhiệt độ sau khoảng 2 phút.
Hãy nêu hiện tượng của các quá trình: đốt cháy than, ethanol trong không khí. Nhiệt độ môi trường xung quanh thay đổi như thế nào?
Khi thả viên vitamin C sủi vào cốc nước như Hình 13.3, em hãy dự đoán sự thay đổi nhiệt độ của nước trong cốc

Trong phản ứng nung đá vôi (CaCO3), nếu ngừng cung cấp nhiệt, phản ứng có tiếp tục xảy ra không?
Thực hiện thí nghiệm 2. Nêu hiện tượng trước và sau khi đốt nóng hỗn hợp. Nếu ngừng đốt nóng thì phản ứng có xảy ra không?
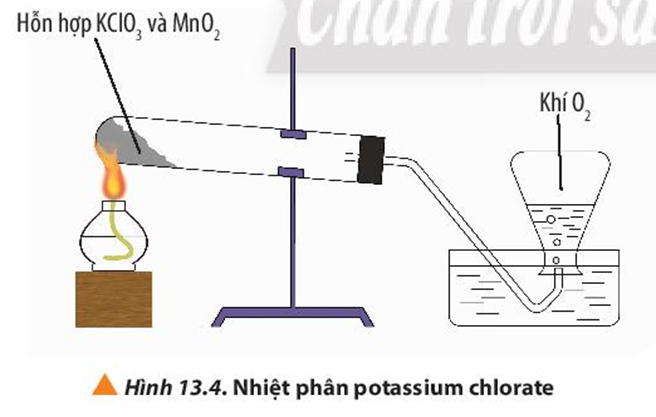
Thí nghiệm 2: Nhiệt phân potassium chlorate
Dụng cụ và thiết bị: Đèn cồn, ống nghiệm chịu nhiệt, nút cao su có gắn ống dẫn khí, chậu thủy tinh, bình tam giác, giá sắt.
Hóa chất: Potassium chlorate (KClO3), manganese dioxide (MnO2)
Tiến hành:
Bước 1: Trộn đều khoảng 4 g tinh thể KClO3 đã được nghiền nhỏ với 1 g MnO2. Cho hỗn hợp vào ống nghiệm chịu nhiệt, khô. Đậy ống nghiệm vào nút có gắn ống dẫn khí. Lắp hệ thống như Hình 13.4. Quan sát hiện tượng.
Bước 2: Dùng đèn cồn hơ nóng đều nửa đáy ống nghiệm, sau đó đun tập trung ở phần có chứa hóa chất. Quan sát hiện tượng.
Phương trình hóa học của phản ứng:
2KClO3(s) →t° 3O2(g) + 2KCl(s)
Biến thiên enthalpy chuẩn của một phản ứng hóa học được xác định trong điều kiện nào?
Phương trình nhiệt hóa học cho biết thông tin gì về phản ứng hóa học
Cho hai phương trình nhiệt hóa học sau:
C(s) + H2O(g) →t° CO(g) + H2(g) ∆ rH298o= +131,25 kJ (1)
CuSO4 (aq) + Zn(s) → ZnSO4(aq) + Cu(s) ∆ rH298o= -231,04 kJ (2)
Trong hai phản ứng trên, phản ứng nào là thu nhiệt, phản ứng nào là tỏa nhiệt?
Phân biệt enthalpy tạo thành của một chất và biến thiên enthalpy của phản ứng. Lấy ví dụ minh họa
Cho phản ứng sau:
S(s) + O2(g) →t° SO2(g)
∆ fH298o(SO2, g) = -296,80 kJ/mol
Cho biết ý nghĩa của giá trị ∆ fH298o(SO2, g)

Hợp chất SO2(g) bền hơn hay kém bền hơn về mặt năng lượng so với các đơn chất bền S(s) và O2(g)
Từ Bảng 13.1 hãy liệt kê các phản ứng có enthalpy tạo thành dương (lấy nhiệt từ môi trường)
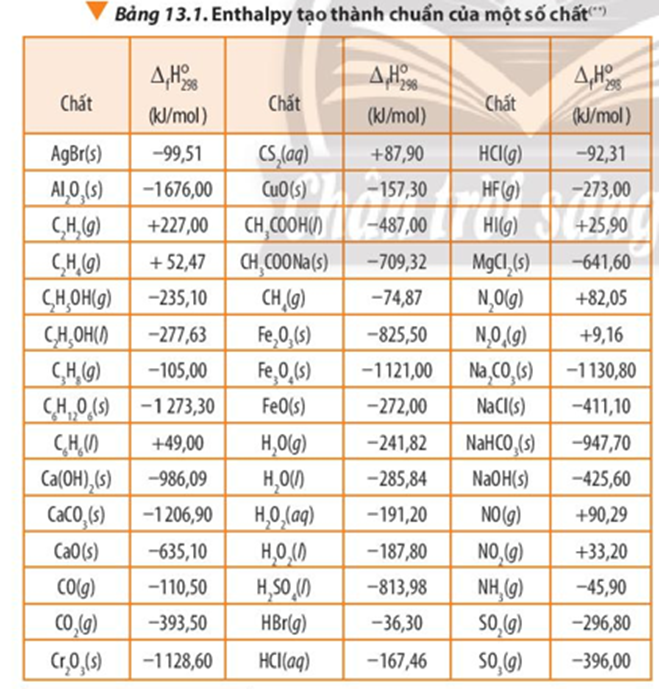
Em hãy xác định enthalpy tạo thành theo đơn vị (kcal) của các chất sau: Fe2O3(s), NO(g), H2O(g), C2H5OH(l). Cho biết 1J = 0,239 cal
Quan sát Hình 13.5, mô tả sơ đồ biểu diễn biến thiên enthalpy của phản ứng. Nhận xét về giá trị của ∆ fH298o(sp) so với ∆ fH298o(cđ)

Vận dụng để vẽ sơ đồ biểu diễn biến thiên enthalpy của phản ứng nhiệt phân CaCO3 ở Ví dụ 5.
Cho hai phương trình nhiệt hóa học sau:
CO(g) + 12O2(g) → CO2(g) ∆ r H298o= -283,00 kJ (1)
H2(g) + F2(g) → 2HF(g) ∆ rH298o = -546,00 kJ (2)
So sánh nhiệt giữa hai phản ứng (1) và (2). Phản ứng nào xảy ra thuận lợi hơn?
Hãy làm cho nhà em sạch bong với hỗn hợp baking soda (NaHCO3) và giấm (CH3COOH). Hỗn hợp này tạo ra một lượng lớn bọt. Phương trình nhiệt hóa học của phản ứng:
NaHCO3(s) + CH3COOH(aq) → CH3COONa(aq) + CO2(g) + H2O(l) ∆ rH298o= 94,30kJ
Phản ứng trên là tỏa nhiệt hay thu nhiệt? Vì sao? Tìm những ứng dụng khác của phản ứng trên.

Phương trình nhiệt hóa học giữa nitrogen và oxygen như sau:
N2(g) + O2(g) → 2NO(g) ∆ rH298o= +180 kJ
Kết luận nào sau đây đúng?
A. Nitrogen và oxygen phản ứng mạnh hơn khi ở nhiệt độ thấp.
B. Phản ứng tỏa nhiệt.
C. Phản ứng xảy ra thuận lợi ở điều kiện thường.
D. Phản ứng hóa học xảy ra có sự hấp thụ nhiệt năng từ môi trường.
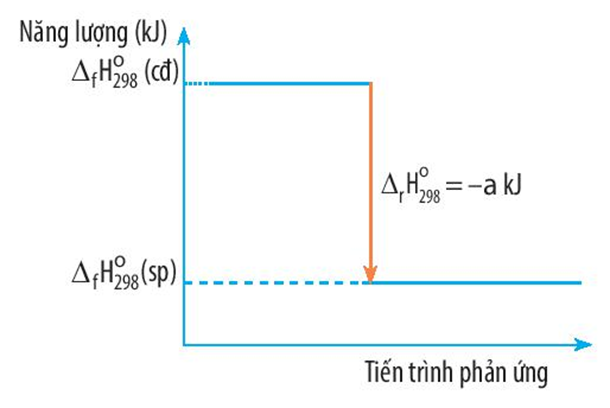
Biến thiên enthalpy của một phản ứng được ghi ở sơ đồ dưới. Kết luận nào sau đây là đúng?
A. Phản ứng tỏa nhiệt
B. Năng lượng chất tham gia phản ứng nhỏ hơn năng lượng chất sản phẩm
C. Biến thiên enthalpy của phản ứng là a kJ/mol
D. Phản ứng thu nhiệt
Đồ thị nào sau đây thể hiện đúng sự thay đổi nhiệt độ khi dung dịch hydrochloric acid được cho vào dung dịch sodium hydroxide tới dư?
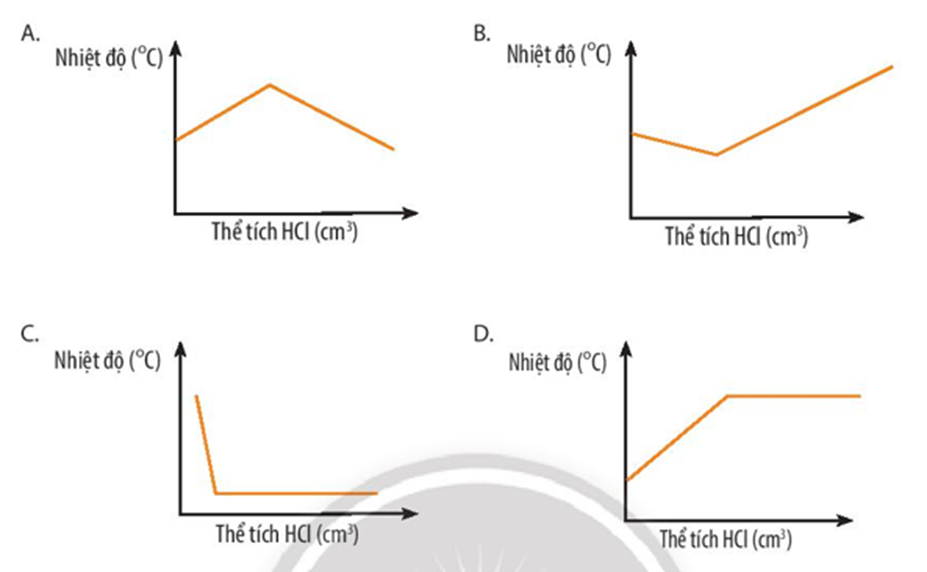
Cho phương trình nhiệt hóa học sau:
NaOH(aq) + HCl(aq) → NaCl(aq) + H2O(l) ∆ rH298o = -57,3 kJ
Vẽ sơ đồ biểu diễn biến thiên enthalpy của phản ứng
Gợi ý cho bạn
Xem tất cảNgân hàng đề thi

