Bài 13: Phản ứng oxi hóa – khử
21 câu hỏi
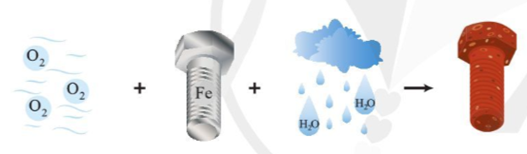
Quá trình bị gỉ của các đinh ốc ngoài không khí được mô tả như hình dưới đây:
Trong quá trình này hãy cho biết nguyên tử nguyên tố nào nhường electron, nguyên tử nguyên tố nào nhận electron. Giải thích.
Xác định số oxi hóa của mỗi nguyên tử nguyên tố trong các hợp chất ion Al2O3, CaF2.
Xác định số oxi hóa của mỗi nguyên tử trong hợp chất sau: NO, CH4
Dựa theo quy tắc octet, giải thích vì sao số oxi hóa của O là -2, của kim loại nhóm IA là +1, của kim loại nhóm IIA là +2 và của Al là +3.
Xác định số oxi hóa của mỗi nguyên tử trong các hợp chất: Fe2O3, Na2CO3, KAl(SO4)2
Xác định số oxi hóa của mỗi nguyên tử trong các ion NO3-, NH4+, MnO4-.
Xác định số oxi hóa của mỗi nguyên tử trong NH3 theo cách 2.
Dựa vào độ âm điện, giải thích vì sao công thức ion giả định của OF2 là F-O2+F- mà không phải là F+O2-F+
Xác định số oxi hóa của các nguyên tử trong phản ứng (1), (2). Cho biết nguyên tố nào có sự thay đổi số oxi hóa.
Nguyên tố Cl thể hiện bao nhiêu số oxi hóa trong phản ứng (3)?
Trong phản ứng ở ví dụ 1, hãy chỉ ra chất khử, chất oxi hóa, quá trình khử, quá trình oxi hóa.
Cân bằng các phản ứng oxi hóa – khử sau. Chỉ ra chất oxi hóa, chất khử, sự oxi hóa, sự khử.
a) Fe2O3 + CO → Fe + CO2
b) NH3 + O2 → NO + H2O
Các phản ứng trên thường gặp trong đời sống và trong sản xuất. Những phản ứng này thường diễn ra trong quá trình nào?
Cân bằng các phản ứng oxi hóa – khử sau:
a) HCl + PbO2 → PbCl2 + Cl2 + H2O
b) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
Sắt bị gỉ trong không khí ẩm. Đó có phải là phản ứng oxi hóa – khử không? Đề xuất một vài biện pháp hạn chế sự tạo gỉ kim loại nêu trên.
Hãy viết các quá trình thay đổi số oxi hóa của mỗi nguyên tử nguyên tố trong phản ứng oxi hóa hoàn toàn methane (thành phần chính của khí thiên nhiên)
Xác định số oxi hóa của mỗi nguyên tử trong phân tử và ion sau đây:
a) H2SO3
b) Al(OH)4-
c) NaAlH4
d) NO2-
Xác định chất oxi hóa, chất khử, viết quá trình oxi hóa, quá trình khử trong các phản ứng sau:
a) Ag+ + Fe2+ → Ag + Fe3+
b) 3Hg2+ + 2Fe → 3Hg + 2Fe3+
c) 2As + 3Cl2 → 2AsCl3
d*) Al + 6H+ + 3NO3- → Al3+ + 3NO2 + 3H2O
Cân bằng các phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron:
a) NaBr + Cl2 → NaCl + Br2
b) Fe2O3 + CO → Fe + CO2
c) CO + I2O5 → CO2 + I2
d) Cr(OH)3 + Br2 + OH- → CrO42- + Br- + H2O
e) H+ + MnO4- + HCOOH → Mn2+ + H2O + CO2
Nước oxi già có tính oxi hóa mạnh, do khả năng oxi hóa của hydrogen peroxide (H2O2).
a) Từ công thức cấu tạo H – O – O – H, hãy xác định số oxi hóa của mỗi nguyên tử.
b) Nguyên tử nguyên tố nào gây nên tính oxi hóa của H2O2. Viết quá trình khử minh họa cho nguyên tử nguyên tố đó.
Xăng E5 được tạo nên bởi sự pha trộn xăng A92 và ethanol (C2H5OH) theo tỉ lệ thể tích tương ứng là 95 : 5, giúp thay thế một phần nhiên liệu hóa thạch, phù hợp với xu thế phát triển chung trên thế giới và góp phần đảm bảo an ninh năng lượng quốc gia.
Viết phương trình của phản ứng hóa học đốt cháy ethanol thành CO2 và H2O. Phản ứng này có phải là phản ứng oxi hóa – khử hay không? Nó thuộc loại phản ứng cung cấp hay tích trữ năng lượng.
Gợi ý cho bạn
Xem tất cảNgân hàng đề thi

