30 câu hỏi
Orbital nguyên tử là
đám mây chứa electron có dạng hình cầu.
đám mây chứa electron có dạng hình số 8 nổi.
khu vực không gian xung quanh hạt nhân mà tại đó xác suất có mặt electron là lớn nhất.
quỹ đạo chuyển động của electron quay quanh hạt nhân có kích thước và năng lượng xác định.
Mỗi orbital nguyên tử chứa tối đa
1 electron.
2 electron.
3 electron.
4 electron.
Số orbital trong các phân lớp s, p, d lần lượt bằng
1, 3, 5.
1, 2, 4.
3, 5, 7.
1, 2, 3.
Lớp M có số orbital tối đa bằng
3.
4.
9.
18.
Hình dưới đây biểu diễn hình dạng orbital nguyên tử (AO) nào sau đây?
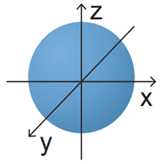
s.
px.
py.
pz.
Orbital nào sau đây có dạng hình cầu?
s.
px.
py.
pz.
Sự phân bố electron trong một orbital dựa vào nguyên lí hay quy tắc nào sau đây?
Nguyên lí vững bền.
Quy tắc Hund.
Nguyên lí Pauli.
Quy tắc Pauli.
Cách biểu diễn electron trong AO nào sau đây không tuân theo nguyên lí Pauli?
A. ![]() .
.
B. ![]() .
.
C. ![]() .
.
D. ![]() .
.
Theo mô hình nguyên tử hiện đại, xác suất tìm thấy electron lớn nhất là ở
bên ngoài các orbital nguyên tử.
trong các orbital nguyên tử.
bên trong hạt nhân nguyên tử.
bất kì vị trí nào trong không gian.
Vùng nào sau đây ứng với xác suất tìm thấy electron trong nguyên tử bằng 100%?
Bên ngoài các orbital nguyên tử.
Trong các orbital nguyên tử.
Trong toàn bộ khoảng không gian xung quanh hạt nhân.
Ở bên trong hạt nhân.
Chọn các phát biểu đúng về electron s.
Là electron chuyển động chủ yếu trong khu vực không gian hình cầu
Là electron chỉ chuyển động trên một mặt cầu.
Là electron chỉ chuyển động trên một đường tròn.
Là electron chỉ chuyển động trên một đường elip.
Hình ảnh dưới đây mô tả AO p với hai thùy.
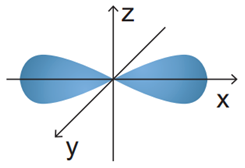
Cho các phát biểu sau:
(a) Xác suất tìm thấy electron ở mỗi thùy là khoảng 45%.
(b) Xác suất tìm thấy electron ở mỗi thùy là khoảng 90%.
(c) Xác suất tìm thấy electron trong AO p là khoảng 90%.
(d) Xác suất tìm thấy electron trong AO p là khoảng 45%.
Số phát biểu đúng là
3.
2.
4.
1.
Cho các phát biểu sau:
(a) Electron quay xung quanh hạt nhân theo những quỹ đạo giống như các hành tinh quay xung quanh Mặt trời.
(b) Electron không chuyển động theo quỹ đạo cố định mà trong cả khu vực không gian xung quanh hạt nhân.
(c) Electron không bị hút vào hạt nhân do còn chịu tác dụng của lực quán tính li tâm.
(d) Electron chuyển động rất nhanh xung quanh hạt nhân không theo một quỹ đạo xác định.
Số phát biểu đúng là
3.
2.
4.
1.
Sự phân bố electron vào các lớp và phân lớp căn cứ vào
nguyên tử khối tăng dần.
điện tích hạt nhân tăng dần.
số khối tăng dần.
mức năng lượng electron.
Ở trạng thái cơ bản, trong nguyên tử, electron chiếm các mức năng lượng
lần lượt từ cao đến thấp.
lần lượt từ thấp đến cao.
bất kì.
từ mức thứ hai trở đi.
Phân lớp 3d có số electron tối đa là
6.
18.
14.
10.
Phân lớp 2p có số electron tối đa là
6.
18.
14.
10.
Lớp electron thứ 3 có bao nhiêu phân lớp?
1.
2.
3.
4.
Lớp electron thứ 2 có bao nhiêu phân lớp?
1.
2.
3.
4.
Kí hiệu phân lớp electron nào sau đây sai?
3s.
3p.
3d.
3f.
Kí hiệu phân lớp electron nào sau đây sai?
1s.
3p.
3d.
2d.
Số lượng electron tối đa có thể chứa trong lớp electron thứ 3 là bao nhiêu?
2.
6.
10.
18.
Số lượng orbital ở lớp electron thứ 2 là bao nhiêu?
2.
3.
1.
4.
Số lượng orbital ở phân lớp electron 2p là
2.
3.
1.
4.
Số lượng electron tối đa có thể chứa trong lớp electron thứ 2 là bao nhiêu?
8.
6.
10.
18.
Phát biểu nào sau đây đúng?
Số phân lớp electron có trong lớp N là 4.
Số phân lớp electron có trong phân lớp M là 4.
Số orbital có trong lớp N là 9.
Số orbital có trong lớp M là 8.
Phát biểu nào sau đây không đúng?
Lớp M có 3 phân lớp.
Lớp L có 9 orbital.
Phân lớp p có 3 orbital.
Năng lượng của electron trên lớp K là thấp nhất.
Phát biểu nào sau đây đúng?
Những electron ở lớp K có mức năng lượng thấp nhất.
Những electron ở gần hạt nhân có mức năng lượng cao nhất.
Electron ở orbital 3p có mức năng lượng thấp hơn electron ở orbital 3s.
Các electron trong cùng một lớp có năng lượng bằng nhau.
Phát biểu nào đúng khi nói về các orbital trong một phân lớp electron?
Có cùng sự định hướng không gian.
Có cùng mức năng lượng.
Khác nhau về mức năng lượng.
Có hình dạng không phụ thuộc vào đặc điểm mỗi phân lớp.
Cho các phát biểu sau:
(a) Orbital 1s có dạng hình cầu, orbital 2s có dạng hình số tám nổi.
(b) Trong một nguyên tử, năng lượng của electron thuộc AO 1s thấp hơn năng lượng của electron thuộc AO 2s.
(c) Trong một nguyên tử, năng lượng của electron thuộc AO 2s thấp hơn năng lượng của electron thuộc AO 2p.
(d) Trong một nguyên tử, năng lượng của electron thuộc AO 2s gần năng lượng của electron thuộc AO 2p.
Số phát biểu đúng là
3.
2.
4.
1.
