Giải SBT Hóa học 12 KNTT Bài 17: Ôn tập chương 5 có đáp án
17 câu hỏi
Cặp oxi hoá - khử nào sau đây có giá trị thế điện cực chuẩn nhỏ hơn 0?
A. Ag+/Ag.
B. Na+/Na.
C. Hg2+/Hg.
D. Cu2+/Cu.
Kí hiệu cặp oxi hoá - khử tương ứng với quá trình khử: Fe(OH)3 + le ⇌ Fe(OH)2 + OH- là
A. Fe3+/Fe2+.
B. Fe2+/Fe.
C. Fe3+/Fe.
D. Fe(OH)3/Fe(OH)2.
Trong dãy điện hoá của kim loại, khi đi từ trái sang phải, tính oxi hoá của cảc ion kim loại biến đổi như thế nào?
A. Không đổi.
B. Tuần hoàn.
C. Giảm dần.
D. Tăng dần.
Trong pin điện hoá Zn - Cu, ở anode (cực âm) xảy ra quá trình
A. oxi hoá Zn thành ion Zn2+.
B. khử ion Cu2+ thành Cu.
C. khử Cu thành ion Cu2+.
D. oxi hoá ion Zn2+ thành Zn.
Khi điện phân dung dịch NaCl bằng dòng điện một chiều (với điện cực trơ, có màng ngăn xốp) thì ở cathode xảy ra quá trình
A. oxi hoá H2O thảnh H+ và O2.
B. khử Cl- thành Cl2.
C. oxi hoá Cl- thành Cl2.
D. khử H2O thành H2 và OH-.
Khi điện phân dung dịch CuSO4 bằng dòng điện một chiều (với điện cực anode bằng Cu) thì ở anode xảy ra quá trình
A. oxi hoá H2O thành H+ và O2.
B. khử Cu2+ thành Cu.
C. oxi hoá Cu thành Cu2+.
D. khử H2O thành H2 và OH-.
Trong nước, thế điện cực chuẩn của kim loại Mn+/M càng lớn thì dạng khử có tính khử ...(1)... và dạng oxi hoá có tính oxi hoá ...(2)... Cụm từ cần điền vào (1) và (2) lần lượt là
A. càng mạnh và càng yếu.
B. càng mạnh và càng mạnh.
C. càng yếu và càng yếu.
D. càng yếu và càng mạnh.
Cho thứ tự sắp xếp các cặp oxi hoá - khử trong dãy điện hoá: Mg2+/Mg; H2O/H2, OH-; 2H+/H2; Ag+/Ag.
Thí nghiệm nào sau đây không xảy ra phản ứng ở điều kiện chuẩn?
A. Cho sợi phoi bào Mg vào nước.
B. Cho lá Mg vào dung dịch HCl.
C. Cho lá Ag vào dung dịch H2SO4.
D. Cho sợi Mg vào dung dịch AgNO3.
Xét phản ứng hoá học giữa hai cặp oxi hoá - khử của kim loại:
R + 2M+ ® R2+ + 2M
Biết giá trị thế điện cực chuẩn các cặp oxi hoá - khử M+/M và R2+/R lần lượt là X (V) và y (V). Nhận xét nào sau đây đúng?
A. x < y.
B. x > y.
C. x - y.
D. 2x = y.
Cho phản ứng hoá học: Cu + 2Fe3+ ® Cu2+ + 2Fe2+
Phát biểu nào sau đây về phản ứng trên không đúng?
A. Cu bị Fe3+ oxi hoá thành Cu2+.
B. Cu2+ có tính oxi hoá mạnh hơn Fe3+.
C. Fe3+ bị Cu khử thành Fe2+.
D. Cu là chất khử, Fe3+ là chất oxi hoá.
Cho các cặp oxi hoá - khử và thế điện cực chuẩn tương ứng:
Cặp oxi hóa – khử | Na+/Na | Mg2+/Mg | Al3+/A1 | Cu2+/Cu |
Thể điện cực chuẩn (V) | -2,713 | -2,356 | -1,676 | +0,340 |
Ion kim loại nào sau đây bị khử tại cathode khi điện phân (với điện graphite) dung dịch muối sulfate tương ứng?
A. Mg2+.
B. Na+.
C. Cu2+.
D. Al3+.
Ở điều kiện chuẩn, cho bột Cu dư vào dung dịch Fe2(SO4)3 tới khi phản ứng hoàn toàn, thu được chất rắn X và dung dịch Y
Cho biết:
Cặp oxi hoá - khử | Fe2+/Fe | Cu2+/Cu | Fe3+/Fe2+ |
Thế điện cực chuẩn (V) | -0,44 | +0,340 | +0,771 |
a) X gồm hai kim loại.
b) Cu có tính khử mạnh hơn Fe2+ ở điều kiện chuẩn.
c) Y gồm hai chất tan là CuSO4 và FeSO4.
d) Trong điều kiện Fe2(SO4)3 dư thì Y gồm ba muối.
a) Kim loại càng mạnh thì thế điện cực chuẩn càng âm.
b) Khi tạo thành pin điện hoá, kim loại mạnh hơn sẽ đóng vai trò là cathode.
c) Điện phân dung dịch CuSO4, cứ thu được 1 moi Cu thì khối lượng dung dịch giảm 80 g.
d) Để bảo vệ đồ vật bằng kim loại, nên gắn chúng với những mảnh kim loại yếu hơn.
Xét quá trình hoạt động của một pin điện hoá Cu – Ag được thiết lập ở các điều kiện như hình vẽ bên.
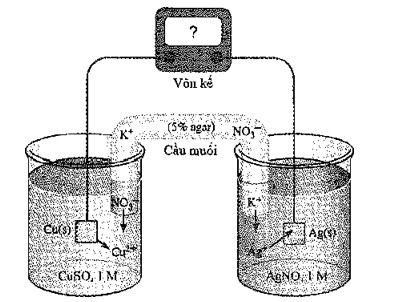
Cho thế điện cực chuẩn của các cặp Cu2+/Cu và Ag+/Ag lần lượt là +0,340 V và +0,799 V.
a) Giá trị sức điện động chuẩn của pin điện hoá trên là 0,459 V.
b) Ở anode xảy ra quá trình oxi hoá Cu, ở cathode xảy ra quá trình khử Ag+.
c) Điện cực Cu tăng khối lượng, điện cực Ag giảm khối lượng.
d) Phản ứng hoá học xảy ra trong pin: Cu + 2Ag+® Cu2+ + 2Ag.
Một pin Galvani được lắp ghép từ hai điện cực tạo bởi hai cặp oxi hoá - khử là Pb2+/Pb và Fe3+/Fe2+
Sức điện động chuẩn của pin Galvani trên là bao nhiêu vôn? (Làm tròn kết quả đến phần trăm).
Sức điện động chuẩn của một pin Galvani (được lắp ghép từ hai điện cực tạo bởi hai cặp oxi hoá - khử là 2H+/H2 và Ag+/Ag) đo được bằng vôn kế có điện trở vô cùng lớn là 0,771 V.
Từ kết quả trên, xác định được thế điện cực chuẩn của cặp Ag+/Ag là bao nhiêu vôn? (Làm tròn kết quả đến phần trăm).
Điện phân 2 lít dung dịch NaCl 0,5 M với điện cực trơ, màng ngăn xốp bằng dòng điện có cường độ không đổi 0,2 A. Sau 1 930 giây thì dừng điện phân, thu được dung dịch X (giả thiết thể tích dung dịch không đổi). Dung dịch X có pH bằng bao nhiêu?
Gợi ý cho bạn
Xem tất cảNgân hàng đề thi



