Giải SBT Hóa học 12 CTST Bài 17: Nguyên tố nhóm IA có đáp án
23 câu hỏi
Nguyên tử của các nguyên tố nhóm IA khác nhau về
A. số electron lớp ngoài cùng của nguyên tử.
B. cấu hình electron nguyên tử.
C. số oxi hóa của nguyên tử trong hợp chất.
D. kiểu mạng tinh thể của đơn chất.
Theo chiều tăng dần của điện tích hạt nhân nguyên tử, sự biến đổi tính chất của các nguyên tố nhóm IA nào sau đây đúng?
A. Bán kính nguyên tử giảm dần.
B. Nhiệt độ nóng chảy tăng dần.
C. Độ cứng giảm dần.
D. Khối lượng riêng của đơn chất giảm dần.
Công thức chung của oxide kim loại nguyên tố nhóm IA là
A. R2O3. B. RO2.
C. R2O. D. RO.
Cation M+ có cấu hình electron lớp ngoài cùng là 2s22p6. Biết Li (Z = 7); Na (Z = 11); K (Z = 19). Cation M+ là
A. Rb+. B. Na+.
C. Li+. D. K+.
Cho các dãy kim loại sau: Fe, Na, K, Cu và Li. Số kim loại trong dãy tác dụng được với nước ở nhiệt độ thường là
A. 1. B. 2. C. 3. D. 4.
Nước Javel là sản phẩm của quá trình
A. sục khí chlorine vào vôi sữa.
B. cho dung dịch NaOH loãng tác dụng với khí chlorine.
C. điện phân dung dịch NaOH có màng ngăn giữa hai điện cực.
D. điện phân nóng chảy NaOH không có màng ngăn.
Phương pháp điều chế NaOH trong công nghiệp là
A. Cho kim loại Na tác dụng với nước: 2Na + 2H2O → 2NaOH + H2↑
B. Cho Na2O tác dụng với nước: Na2O + H2O → 2NaOH
C. Điện phân dung dịch NaCl bão hòa có màng ngăn:
2NaCl + 2H2O →đpdd/ màng ngăn 2NaOH + H2↑ + Cl2↑
D. Điện phân dung dịch NaCl 20% không có màng ngăn:
2NaCl + 2H2O →đpdd 2NaOH + H2↑ + Cl2↑
Cho sơ đồ phản ứng: NaCl → X → NaHCO3 → Y → NaNO3
Chất X và Y phù hợp có thể là
A. NaOH và Na2CO3
B. NaOH và NaClO
C. Na2CO3 và NaClO
D. NaClO3 và Na2CO3
Cho a mol CO2 vào dung dịch chứa b mol NaOH, dung dịch thu được chứa muối Na2CO3 và NaHCO3. Giá trị của a và b trong trường hợp nào sau đây là đúng?
A. a > b. B. a < b < 2a. C. b > 2a. D. a = b.
Cho 0,53 gam muối carbonate của kim loại nhóm IA tác dụng với dung dịch HCl, thu được 123,95 mL khí CO2 (đkc). Công thức của muối là
A. Na2CO3 B. NaHCO3
C. KHCO3 D. K2CO3
Để xác định 3 hợp chất X, Y, Z đều là muối của Na (khi bị đốt cháy cho ngọn lửa màu vàng đặc trưng), tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho các mẫu thử tác dụng với dung dịch Ba(NO3)2, chỉ có X tạo kết tủa.
Thí nghiệm 2: Cho các mẫu thử tác dụng với dung dịch H2SO4 thì Y và Z tạo ra chất khí.
Thí nghiệm 3. Cho các mẫu thử tác dụng với dung dịch KMnO4 trong H2SO4, chỉ có Y làm nhạt màu dung dịch KMnO4.
Xác định X, Y, Z. Viết các phương trình hóa học xảy ra.
Viết phương trình hóa học dạng ion của các phản ứng trong thí nghiệm sau (các phản ứng xảy ra hoàn toàn): Đun nóng dung dịch NaHCO3, để nguội rồi đem tác dụng lần lượt với dung dịch Ba(NO3)2, dung dịch AlCl3.
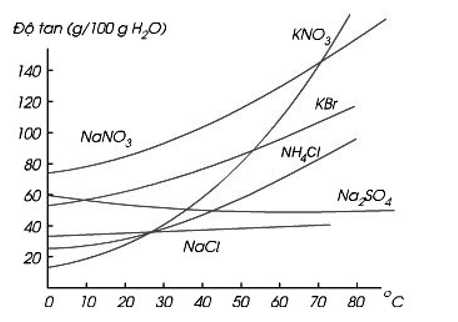
Dựa vào đồ thị về độ tan của các chất rắn trong nước ở hình bên, hãy cho biết độ tan của các muối NaNO3, KBr, KNO3, NaCl, Na2SO4 ở nhiệt độ 10oC và 60oC.
Viết phương trình hóa học cho các trường hợp phản ứng sau:
a. Sodium oxide tác dụng với nước.
b. Potassium hydroxide tác dụng với acetic acid.
c. Potassium superoxide tác dụng với nước.
d. Điện phân KBr nóng chảy.
e. Điện phân dung dịch NaCl có màng ngăn.
g. NaOH + SO2.
h. Na + (CH3)2CHOH
i. KOH + CO2
k. H2C2O4 + CsOH
Cho giá trị độ tan trong nước ở 298 K của một số chất trong bảng sau:
Chất | Li2CO3 | LiI | Na2CO3 | NaOH | Cs2CO3 | KNO3 |
Độ tan (g/100 g H2O) | 1,33 | 165 | 21,5 | 109 | 234 | 31,6 |
a. Hợp chất nào sau đây tan ít nhất trong nước ở 298 K: Li2CO3, LiI, Na2CO3, NaOH, Cs2CO3, KNO3?
b. Hợp chất nào sau đây xảy ra phản ứng khi thêm vào nước ở 298 K: RbOH, NaNO3, Na2O, Li2SO4, K2CO3, LiF?
Sơ đồ dưới đây mô tả quá trình Solvay để điều chế Na2CO3 trong công nghiệp.
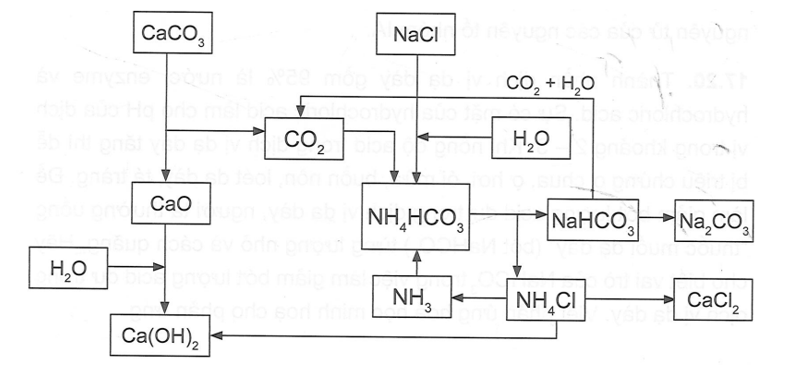
Dựa vào sơ đồ trên, hãy:
a. Viết phương trình của phản ứng tổng quát tạo Na2CO3.
b. Viết phương trình cân bằng của cặp muối NaCl/ NH4HCO3.
c. Viết phương trình hình thành NH4HCO3.
d. Nêu vai trò của Ca(OH)2 trong quá trình và viết phương trình phản ứng.
a. Có ba dung dịch NaCl, LiCl, KCl trong các lọ bị mất nhãn. Hãy nêu các phương pháp dùng để nhận biết các dung dịch trên.
b. Chỉ dùng quỳ tím, hãy nhận biết các dung dịch sau: Na2CO3, NaOH, HCl, NaNO3.
Hãy giải thích ứng dụng của Na2CO3 trong các trường hợp sau:
a. Bên cạnh việc phải lọc nước thường xuyên thì cần sử dụng hóa chất Na2CO3 trong xử lí nước bể bơi để đảm bảo được chất lượng loại bỏ vi khuẩn, giúp xử lí nước hồ bơi hiệu quả và nhanh chóng.
b. Soda chiếm 13% - 15% nguyên liệu sản xuất thủy tinh.
Dựa vào Bảng 17.12 về khối lượng riêng của các kim loại nhóm IA trong SGK để tính thể tích mol nguyên tử của chúng ở trạng thái rắn. Nhận xét về sự biến đổi thể tích mol nguyên tử với sự biến đổi bán kính nguyên tử của các nguyên tố nhóm IA.
Thành phần của dịch dạ dày gồm 95% là nước, enzyme và hydrochloric acid. Sự có mặt của hydrochloric acid làm cho pH của dịch vị trong khoảng 2 – 3. Khi nồng độ acid trong dịch vị dạ dày tăng thì dễ bị triệu chứng ợ chua, ợ hơi, ói mửa, buồn nôn, loét dạ dày, tá tràng. Đề làm giảm bớt lượng acid dư trong dịch vị dạ dày, người ta thường uống “thuốc muối dạ dày” (bột NaHCO3) từng lượng nhỏ và cách quãng. Hãy cho biết vai trò của NaHCO3 trong việc làm giảm bớt lượng acid dư trong dịch vị dạ dày. Viết phương trình hóa học minh họa cho phản ứng.
Sodium sulfate (Na2SO4) được ứng dụng trong sản xuất giấy, thủy tinh, chất tẩy rửa. Trong công nghiệp, Na2SO4 được sản xuất bằng cách đun H2SO4 với NaCl. Người ta dùng một lượng H2SO4 vừa đủ, nồng độ 75% đun với NaCl. Sau phản ứng thu được sản phẩm có tỉ lệ như sau: 91,48% Na2SO4; 4,79% NaHSO4; 1,98% NaCl; 1,35% H2O; 0,40% HCl.
a. Viết các phản ứng hóa học xảy ra. Tính tỉ lệ % NaCl đã chuyển hóa thành Na2SO4.
b. Tính khối lượng hỗn hợp rắn thu được nếu dùng một tấn NaCl.
c. Tính thành phần % khối lượng mỗi khí và hơi thoát ra khi sản xuất được 1 tấn hỗn hợp rắn.
a. Vì sao các kim loại nhóm IA rất dễ nóng chảy? Hãy nêu thêm hai xu hướng biến đổi có tính quy luật về tính chất vật lí khác của nhóm IA.
b. Một giá trị đo ở Bảng 17.2 trong SGK không phù hợp với xu hướng biến đổi có tính quy luật. Hãy nêu xu hướng không phù hợp đó.
Tiến hành điện phân với điện cực trơ có màng ngăn 200 mL dung dịch NaCl cho tới khi cathode thoát ra 0,2479 L khí (đkc) thì ngừng điện phân. Tính pH của dung dịch sau điện phân.
Gợi ý cho bạn
Xem tất cảNgân hàng đề thi



