40 câu hỏi
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Na (Z = 11) là
1s22s22p53s2.
1s22s22p63s1.
1s22s22p63s2.
1s22s22p43s1.
Nguyên tử nguyên tố X có tổng số electron ở các phân lớp p là 10. Nguyên tố X là
phi kim.
kim loại.
khí trơ.
kim loại hoặc phi kim.
Hợp chất nào sau đây ở dạng tinh thể, dễ tan trong nước và có nhiệt độ nóng chảy cao?
NaCl.
H2O.
HCl.
NH3.
Phản ứng nào dưới đây thuộc loại phản ứng oxi hóa - khử?
AgNO3 + NaCl → AgCl + NaNO3.
NaOH + HCl → NaCl + H2O.
2Na + 2H2O → 2NaOH + H2.
2 NaHCO3 → Na2CO3 + CO2 + H2O.
Cho phương trình phản ứng a Al + b HNO3 → c Al(NO3)3 + d N2O + e H2O. Tỉ lệ (a : e) là
4:1
1:4
15:8
8:15
Nitơ trong hợp chất nào sau đây vừa có tính oxi hoá vừa có tính khử?
NaNO3.
NaNO2.
HNO3.
NH3.
Dung dịch chất nào sau đây làm quỳ tím chuyển sang màu đỏ?
HCl.
NaOH.
NaCl.
NaNO3
Ozon là một dạng thù hình quan trọng của oxi. Trong tự nhiên có 1 lớp ozon mỏng hình thành ở tầng bình lưu, cách mặt đất khoảng 15-35 km – tùy địa điểm, nó có tác dụng ngăn các bức xạ nguy hại như tia cực tím, tia vũ trụ, bảo vệ các sinh vật trên Trái Đất. Hình ảnh bên dưới mô phỏng cho lỗ hổng tầng ozon. Em hãy cho biết công thức phân tử của ozon là

O3.
O2.
O4.
H2O2.
Dẫn mẫu khí thải của một nhà máy qua dung dịch Pb(NO3)2 dư thì thấy xuất hiện kết tủa màu đen. Hiện tượng đó chứng tỏ trong khí thải nhà máy có khí nào sau đây?
NH3.
CO2.
SO2.
H2S.
Thực hiện thí nghiệm như hình vẽ mô phỏng dưới đây. Em hãy cho biết, chất lỏng trong bình (c) có thể là chất nào sau đây?
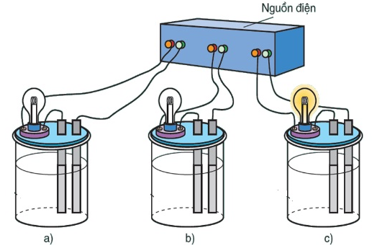
dung dịch muối ăn.
dung dịch saccarozơ.
dung dịch ancol etylic.
nước cất.
Chất nào sau đây thuộc loại chất điện li yếu?
KCl.
HF.
HNO3.
NH4Cl.
Chất nào dưới đây có tính lưỡng tính?
Ca(OH)2.
KOH.
Al(OH)3.
H2SO4.
Chất nào sau đây là muối axit?
KNO3.
NaHSO4.
NaCl.
Na2SO4.
Dung dịch chất nào sau đây (có cùng nồng độ) dẫn điện tốt nhất?
K2SO4.
KOH.
KCl.
KNO3.
Sau khi nhúng lần lượt từng giấy chỉ thị pH (có sự chuyển màu tương tự như quỳ tím) vào 4 cốc, mỗi cốc chứa 1 chất lỏng được đánh số như trên giấy chỉ thị. Khẳng định nào sau đây là đúng?

Cốc 1 chứa dung dịch NaOH.
Cốc 2 chứa nước cất.
Cốc 3 chứa dung dịch HCl.
Cốc 4 chứa axit axetic.
Phản ứng nào sau đây có phương trình ion rút gọn là H+ + OH- → H2O?
NaHCO3 + NaOH → Na2CO3 + H2O.
KOH + HCl → KCl + H2O.
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O.
Cu(OH)2 + 2HCl → CuCl2 + 2H2O.
Dãy gồm các ion cùng tồn tại trong một dung dịch là:
Al3+, PO43–, Cl–, Ba2+.
Ca2+, Cl–, Na+, CO32–.
K+, Ba2+, OH–, Cl–.
Na+, K+, OH–, HCO3–.
Cho các dung dịch riêng biệt: HCl, Ba(OH)2, KHSO4, H2SO4, KOH. Số chất tác dụng với dung dịch Ba(HCO3)2 tạo kết tủa là
5
3
2
4
Cho các dung dịch có cùng nồng độ: K2CO3 (1), H2SO4 (2), HCl (3), KNO3 (4). Giá trị pH của các dung dịch được sắp xếp theo chiều tăng từ trái sang phải là:
(3), (2), (4), (1).
(4), (1), (2), (3).
(1), (2), (3), (4).
(2), (3), (4), (1).
Hình ảnh bên dưới là sản phẩm một loại phân bón trên thị trường. Em hãy cho biết, nó được xếp vào loại nào sau đây

phân đạm.
Phân tổng hợp.
Phân phức hợp.
Phân vi lượng.
Loại phân bón hoá học mà độ dinh dưỡng được tính bằng thành phần % theo khối lượng của P2O5 là
phân đạm.
phân lân.
phân kali.
phân vi lượng.
Chất thường được dùng làm bột nở là
NaCl.
NH4HCO3.
HCl.
Na2CO3.
Kim loại bị thụ động trong HNO3 đặc, nguội là
Al, Fe.
Ag, Fe.
Pb, Ag.
Pt, Au.
Chất nào sau đây vừa phản ứng được với axit, vừa có thể phản ứng với bazơ?
Na2CO3.
H2SO4.
AlCl3.
NaHCO3.
Trong phản ứng nào sau đây, nitơ thể hiện tính khử?
N2 + 3H2 →.
N2 + 6Li →.
N2 + O2 →.
N2 + 3Mg →.
Trong phòng thí nghiệm, người ta thường thu khí bằng một trong ba cách như trong hình vẽ. Hãy cho biết khí nitơ có thể được thu bằng cách nào?
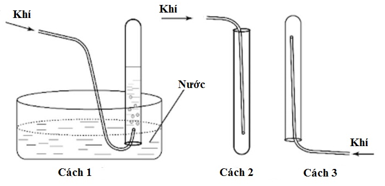
Cách 1 hoặc cách 3.
Cách 1 hoặc cách 2.
Cách 2 hoặc cách 3.
Cả ba cách.
Tính chất hóa học đặc trưng của amoniac là
tính bazơ yếu và tính khử.
tính axit yếu và tính khử.
tính bazơ yếu và tính oxi hóa.
tính axit yếu và tính oxi hóa.
Chất có thể dùng để làm khô khí NH3 là
H2SO4 đặc.
P2O5.
CuSO4 khan.
NaOH rắn.
Hình vẽ mô phỏng thí nghiệm dưới đây nhằm chứng minh điều gì?
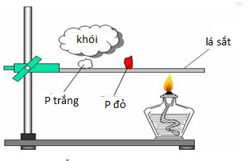
Tính oxi hóa rất mạnh của photpho đỏ.
Tính khử rất mạnh của photpho trắng.
Photpho trắng kém bền với nhiệt hơn photpho đỏ.
Khả năng phản ứng của photpho với kim loại sắt.
Trung hòa 100 ml dung dịch HCl 0,5 M cần dùng vừa đủ V ml dung dịch NaOH 1M. Giá trị của V là
50.
25.
100.
200.
Cho 35,84 gam kim loại X phản ứng vừa đủ với 21,504 lít khí Cl2 (đktc) tạo ra một muối clorua. Kim loại X là
Cu
Mg
Zn.
Fe.
Cho m gam kim loại Cu phản ứng hoàn toàn với dung dịch HNO3 loãng (dư), thu được 3,696 lít khí NO (đktc, sản phẩm khử duy nhất). Giá trị của m là
5,28.
10,56.
15,84.
31,68.
Trộn 500 ml dung dịch chứa hỗn hợp HNO3 0,08M và H2SO4 0,01M với 500 ml dung dịch KOH x M thu được 1 lít dung dịch có pH bằng 12. Giá trị của x là
0,13M.
0,12M.
0,14M.
0.10M.
Dung dịch X gồm 0,1 mol NH4+; 0,15 mol Mg2+; 0,1 mol Na+; 0,18 mol Cl− và x mol Y2-. Cô cạn dung dịch X, thu được m gam muối khan. Ion Y2− và giá trị của m là
CO32− và 33,29.
SO42− và 44,81.
CO32− và 23,69.
SO42− và 29,45.
Hòa tan 9,8 gam axit H3PO4 vào 130 ml dung dịch KOH 1M, sau phản ứng hoàn toàn thu được dung dịch chứa
KH2PO4 và K2HPO4.
KH2PO4 và K3PO4.
K3PO4 và K2HPO4.
K3PO4 và KOH dư.
Cho m gam P2O5 tác dụng với 507 ml dung dịch NaOH 2M, sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X. Cô cạn dung dịch X, thu được 3m gam chất rắn khan. Giá trị của m là
8,52.
12,78.
21,30.
17,04.
Hoà tan hoàn toàn 16,1 gam hỗn hợp gồm Na, K và Ca vào nước, thu được dung dịch X và 6,72 lít khí H2 (đktc). Dung dịch Y gồm HNO3 và H2SO4, tỉ lệ mol tương ứng là 2: 5. Trung hoà dung dịch X bởi dung dịch Y, tổng khối lượng các muối được tạo ra là
46,9 gam.
30,2 gam.
46,3 gam.
41,2 gam.
Nung hỗn hợp X gồm Cu(NO3)2, KNO3 và NaNO3 ở nhiệt độ cao đến phản ứng hoàn toàn thu được 13,44 lít hỗn hợp khí Y (ở đktc). Hấp thụ khí Y vào nước thu được 40 lít dung dịch Z và còn lại 2,24 lít khí thoát ra (ở đktc). Giá trị pH của dung dịch Z là
2
12
13
1
Cho hỗn hợp gồm 0,56 gam Fe và 0,96 gam Cu vào 200 ml dung dịch chứa hỗn hợp gồm H2SO4 0,5M và KNO3 0,2M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và khí NO (sản phẩm khử duy nhất). Cho V ml dung dịch NaOH 1M vào dung dịch X thì lượng kết tủa thu được là lớn nhất. Giá trị tối thiểu của V là
180
240
360
120
Hấp thụ hết 5,6 lít khí SO2 (đktc) vào dung dịch chứa x mol KOH và y mol K2SO3, thu được 250 ml dung dịch X. Cho từ từ đến hết 125 ml X vào 375 ml dung dịch HCl 0,5M, thu được 3,36 lít khí (đktc). Mặt khác, cho 125 ml X tác dụng với dung dịch Ba(OH)2 dư, thu được 54,25 gam kết tủa. Giá trị của x là
0,125.
0,205.
0,500.
0,225.
