29 câu hỏi
Công thức hóa học của nhôm là:
Al.
Cu.
Fe.
Zn.
Công thức hóa học của axit sunfuric là:
HCl.
H2SO3.
H2SO4.
HClO.
Tên gọi của Al2O3 và Al(OH)3 lần lượt là
Nhôm oxit và nhôm (III) hidroxit.
Nhôm (III) oxit và nhôm hidroxit.
Nhôm oxit và nhôm hidroxit.
Nhôm (III) oxit và nhôm (III) hidroxit.
Sản phẩm khi đốt cháy nhôm trong khí oxi (O2) là:
AlO.
Al2O3.
Al3O2.
Al2O2
Cho phản ứng: Al + Cl2 …. Tổng hệ số tối giản của phương trình là:
4.
3.
7.
9.
Nhôm không tác dụng được với:
HCl.
H2SO4 loãng.
NaOH.
NaCl.
Nhúng một thanh sắt vào dung dịch đồng (II) sunfat. Phản ứng hóa học xảy ra là:
Fe + CuSO4 15→"> FeSO4 + Cu
Fe + Cu2SO4 15→"> FeSO4 + 2Cu.
2Fe + 3CuSO4 15→"> Fe2(SO4)3 + 3Cu
2Fe + 3Cu2SO4 15→"> Fe2(SO4)3 + 6Cu.
Nhiệt phân sắt (III) hidroxit thu được sản phẩm là:
Fe2O3
Fe.
Fe2O3 và H2O.
Fe và H2O.
Thêm vài giọt kali hidroxit vào dung dịch đồng (II) clorua. Sản phẩm thu được là:
Cu(OH)2 và KCl.
Cu(OH)2 và NaCl.
CuOH và KCl
CuOH và NaCl.
Cho phản ứng hóa học: x… + H2SO4 → FeSO4 + y… . Tổng (x + y) có thể là:
1.
2.
3.
4.
Phản ứng hóa học nào sau đây không chính xác:
Fe + CuSO4 → FeSO4 + Cu.
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag.
Cu + MgSO4 → CuSO4 + Mg
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
Hiện tượng khi thêm vài giọt dung dịch H2SO4 vào dung dịch BaCl2 là:
Xuất hiện kết tủa hồng.
Xuất hiện kết tủa trắng.
Xuất hiện kết tủa nâu đỏ.
Xuất hiện kết tủa xanh lam.
Hiện tượng khi nhúng quỳ tím vào dung dịch NaOH là:
Quỳ chuyển đỏ
Quỳ chuyển xanh
Quỳ chuyển đen
Quỳ không chuyển màu.
Có thể phân biệt Fe và Al bằng dung dịch:
NaOH.
HCl.
H2SO4 (loãng).
CuSO4.
Có thể phân biệt BaCl2 và NaCl bằng dung dịch:
KNO3.
H2SO4.
KOH.
NaOH.
Quặng nào sau đây chứa thành phần chính là Al2O3:
Boxit.
Pirit.
Dolomit.
Apatit
Cho hỗn hợp bột gồm: Al, Fe, Mg và Cu vào dung dịch HCl dư, sau phản ứng thu được chất rắn T không tan. Vậy T là:
Al
Fe.
Mg.
Cu.
Khí X là nguyên nhân gây hiệu ứng nhà kính, đồng thời khí X cũng một nguyên nhân gây mưa axit. Vậy công thức hóa học của X là:
CO2
N2.
O2.
SO2.
Ăn mòn kim loại do ma sát được gọi là:
Ăn mòn vật lý.
Ăn mòn hóa học.
Ăn mòn sinh học.
Ăn mòn toán học
Kim loại có nhiệt độ nóng chảy thấp nhất là:
HCl.
H2O.
HClO.
HCl và HClO
Mô hình điều chế khí clo trong phòng thí nghiệm được cho như hình vẽ bên (Hình 1). Quy trình thí nghiệm xảy ra như sau: Nhỏ từ từ dung dịch (1) xuống bình cầu có chứa chất rắn màu đen (2). Đun nóng hỗn hợp thì thoát ra khí clo (màu vàng lục). Khí clo sinh ra di chuyển theo hệ thống bình (3); (4); (5). Tại bình số (5), khí clo được giữ lại. Để tránh việc clo thoát ra ngoài không khí, người ta tẩm vào (6) dung dịch T. Vậy (1) là:
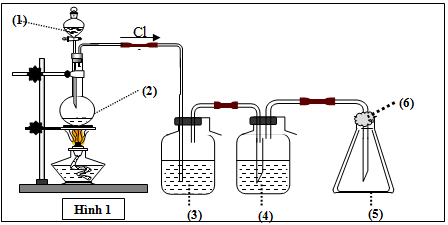
HCl.
NaOH.
H2SO4.
NaCl.
Kim loại có nhiệt độ nóng chảy thấp nhất là:
Hg.
Al.
Fe.
W.
Hòa tan hoàn toàn 5,6 gam Fe bằng dung dịch HCl, sau phản ứng thu được V lít H2 (đktc). Giá trị của V là:
1,12 lít.
2,24 lít.
3,36 lít.
4,48 lít.
Hòa tan hoàn toàn 14,4 gam FeO cần vừa đủ V ml dung dịch HCl 2M. Giá trị của V là:
100.
200.
300.
400.
Nhúng một thanh sắt vào dung dịch CuSO4, sau một thời gian thấy khối lượng chất rắn tăng 1,6 gam. Số mol CuSO4 đã tham gia phản ứng là:
0,1 mol
0,2 mol.
0,3 mol.
0,4 mol.
Hỗn hợp X gồm Fe và Al (với tỉ lệ mol 1 : 1). Hòa tan hoàn toàn m gam X bằng dung dịch HCl dư, sau phản ứng thu được 5,6 lít H2 (đktc). Giá trị của m là:
10,2 gam.
8,3 gam
2,7 gam
16,6 gam.
Để trung hòa hoàn toàn 100ml dung dịch NaOH 1M cần vừa đủ V ml dung dịch H2SO4 2M. Giá trị của V là:
25ml.
50ml.
100ml.
200ml.
Hòa tan 5,6 gam Fe bằng 250ml dung dịch HCl 1M, sau phản ứng thu được dung dịch X có chứa chất tan T. Chất T có khả thể tác dụng với Na2CO3 tạo khí. Coi thể tích dung dịch thay đổi không đáng kể. Nồng độ mol của T là:
0,2M.
0,4M.
0,6M.
0,8M
Hòa tan hoàn toàn một kim loại R có hóa trị II bằng dung dịch H2SO4 9,8% (loãng) vừa đủ, sau phản ứng thu được dung dịch X chứa muối Y với nồng độ phần trăm là 14,394%. Kim loại R là:
Mg.
Fe.
Zn.
Cu.
