Bài tập Tính chất vật lí và hóa học các đơn chất nhóm VIIA có đáp án
26 câu hỏi
Trong đèn halogen, bao quanh dây tóc làm bằng wolfram là các khí hiếm như krypton, xenon và một lượng nhỏ halogen như bromine hoặc iodine, giúp tăng tuổi thọ và duy trì độ trong suốt của vỏ bóng đèn. Đèn halogen được sử dụng trong các máy sưởi, lò nướng, bếp halogen hồng ngoại,… do đặc điểm tỏa nhiều nhiệt.
Nhu cầu về nước sạch là thiết yếu và cấp bách của con người, nước sạch được dùng cho sinh hoạt, ăn uống và sản xuất. Cách xử lí nước phổ biến hiện nay là sử dụng nước chlorine hoặc các chất có chứa chlorine để khử trùng nước
Nhóm halogen gồm những nguyên tố nào? Halogen có những tính chất và ứng dụng trong lĩnh vực nào?

Quan sát Hình 17.1, cho biết vị trí nhóm halogen trong bảng tuần hoàn.
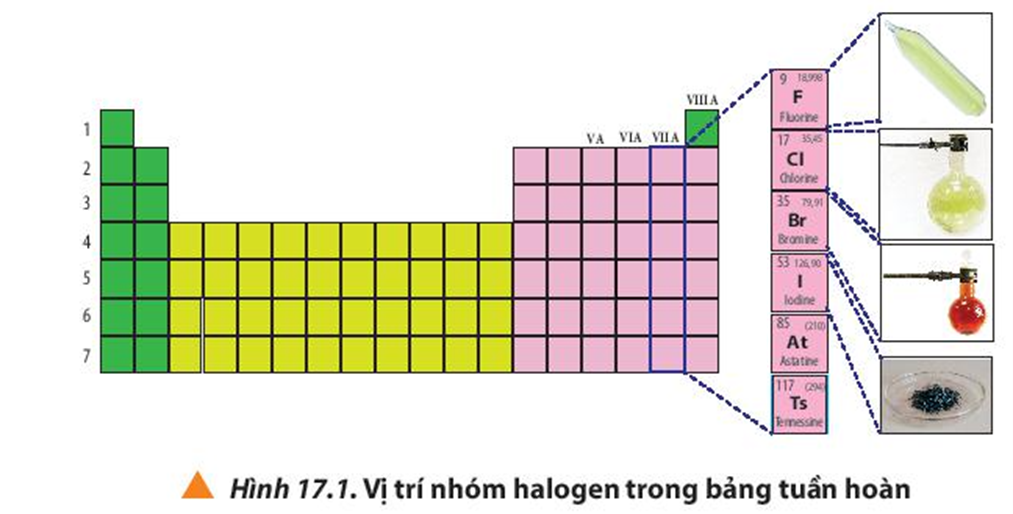
Hãy kể tên một số chất chứa nguyên tố halogen
Từ các thông tin và quan sát Hình 17.2, nhận xét dạng tồn tại của các nguyên tố halogen trong tự nhiên

Khoảng 71% bề mặt Trái Đất được bao phủ bởi biển và đại dương, phần còn lại là các lục địa và đảo. Theo em, hàm lượng nguyên tố halogen nào nhiều nhất trong tự nhiên?
Viết cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố halogen
Từ đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, nhận xét xu hướng hình thành liên kết trong phân tử halogen
Dựa vào Bảng 17.1, nhận xét sự biến đổi về màu sắc, thể các chất ở điều kiện thường, nhiệt độ nóng chảy, nhiệt độ sôi của các đơn chất halogen
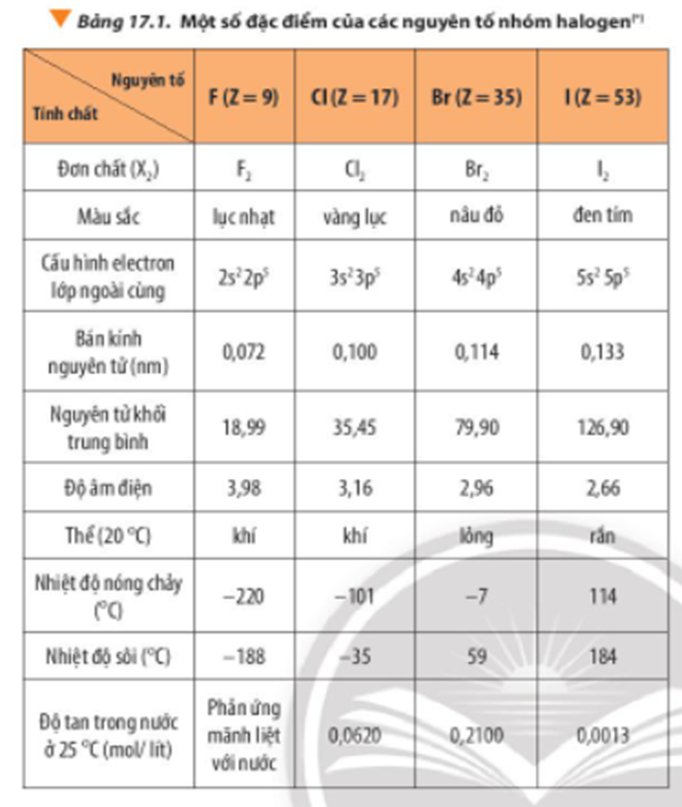
Giải thích sự biến đổi nhiệt độ nóng chảy, nhiệt độ sôi từ fluorine đến iodine.
Ở điều kiện thường, hãy dự đoán astatine tồn tại ở thể khí, thể lỏng hay thể rắn. Giải thích
Từ cấu tạo phân tử halogen và đặc điểm cấu hình electron lớp ngoài cùng của nguyên tử, nhận xét xu hướng hình thành liên kết của nguyên tử halogen trong các phản ứng hóa học
Trong phản ứng với kim loại, nhận xét sự biến đổi số oxi hóa của nguyên tử các nguyên tố halogen và viết các quá trình khử xảy ra
Dựa vào điều kiện phản ứng với hydrogen và giá trị năng lượng liên kết của phân tử H – X, giải thích khả năng phản ứng của các halogen với hydrogen.

Trong phản ứng với dung dịch kiềm, nhận xét sự biến đổi số oxi hóa của chlorine và cho biết phản ứng này thuộc loại phản ứng gì?
Tiến hành thí nghiệm 1, quan sát và ghi nhận hiện tượng.
Thí nghiệm 1: So sánh tính chất hóa học của halogen
Hóa chất: dung dịch NaBr, NaI, nước chlorine, nước bromine và dung dịch hồ tinh bột.
Dụng cụ: ống nghiệm, ống hút nhỏ giọt, kẹp gỗ, giá để ống nghiệm.
Tiến hành: Thực hiện các bước theo Bảng 17.3
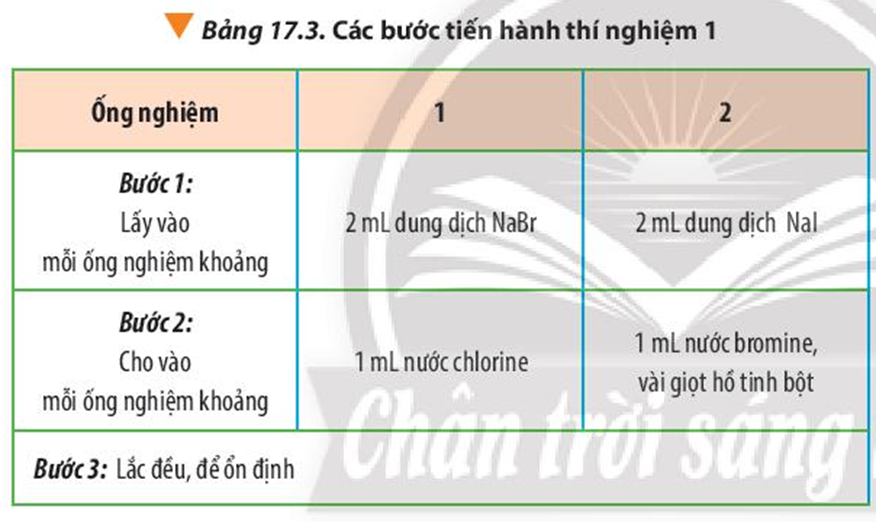
Dựa vào phương trình hóa học của các phản ứng, giải thích kết quả thí nghiệm 1.
Tiến hành thí nghiệm 2, quan sát và ghi nhận hiện tượng.
Thí nghiệm 2: Tính tẩy màu của khí chlorine ẩm
Hóa chất: tinh thể potassium permanganate (KMnO4), dung dịch HCl đặc, giấy màu, nước cất.
Dụng cụ: ống nghiệm 2 nhánh, nút cao su, giá đỡ, thìa thủy tinh, ống hút nhỏ giọt.
Tiến hành:
Bước 1: Dùng thìa thủy tinh lấy một ít tinh thể KMnO4, cho vào nhánh dài của ống nghiệm. Dùng ống hút nhỏ giọt lấy khoảng 1 mL dung dịch HCl đặc cho vào nhánh ngắn của ống nghiệm. Lắp dụng cụ để điều chế khí Cl2 ẩm như Hình 17.4.
Lưu ý: Kiểm tra nút cao su phải được đậy kín trước khi thực hiện bước 2.
Bước 2: Nghiêng ống nghiệm sao cho dung dịch HCl tiếp xúc với KMnO4.
Phương trình hóa học của phản ứng điều chế khí Cl2:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
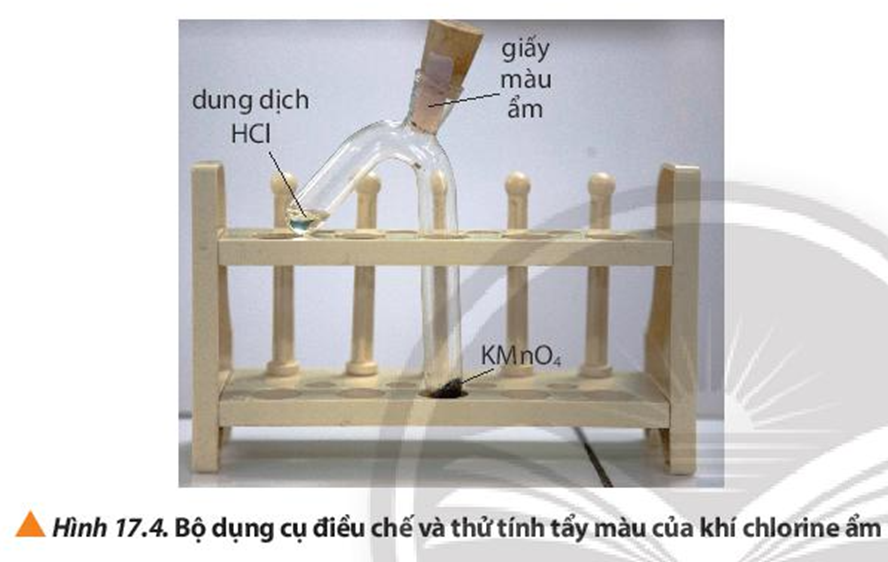
Dựa vào phương trình hóa học của các phản ứng, giải thích kết quả thí nghiệm 2.
Viết phương trình hóa học của các phản ứng sau:
Cu + Cl2 → (1)
Al + Br2 → (2)
Ca(OH)2 + Cl2 → (3)
KOH + Br2 →>70oC (4)
Cl2 + KBr → (5)
Br2 + NaI → (6)
Tính tẩy màu của khí chlorine ẩm được ứng dụng vào lĩnh vực nào trong đời sống?
Nhận xét vai trò của halogen trong đời sống, sản xuất và y tế
Tìm hiểu thêm những ứng dụng khác của halogen trong thực tế.
Tại sao có thể sử dụng nước Javel để tẩy những vết mực trên áo trắng, nhưng lại không nên sử dụng trên vải quần, áo có màu?
Hoàn thành các phương trình minh họa tính chất hóa học của các nguyên tố halogen
a) Cl2 + H2 →
b) F2 + Cu →
c) I2 + Na →
d) Cl2 + Fe →
e) Br2 + Ca(OH)2 →
f) Cl2 + KOH
g) Br2 + KI →
Giải thích vì sao các nguyên tố halogen không tồn tại ở dạng đơn chất trong tự nhiên.
Chlorine B (C6H5ClNNaO2S) là chất thường được sử dụng để sát khuẩn trên các bề mặt, vật dụng hoặc dùng để khử trùng, sát khuẩn, xử lí nước sinh hoạt. Ở nồng độ cao, chloramine B có tác dụng diệt nấm mốc, vi khuẩn, virus gây bệnh cho người. Chloramine B có dạng viên nén (mỗi viên có khối lượng 0,3 – 2,0 gam) và dạng bột. Chloramine B 25% (250 mg chlorine hoạt tính trong một viên nén như hình bên) được dùng phổ biến, vì tiện dụng khi pha chế và bảo quản.
a) Nồng độ chloramine B khi hòa tan vào nước đạt 0,001% có tác dụng sát khuẩn dùng trong xử lí nước sinh hoạt. Cần dùng bao nhiêu viên nén chloramine B 25% (loại viên 1 gam) để xử lí bình chứa 200 lít nước?
b) Chloramine B nồng độ 2% dùng để xịt trên các bề mặt vật dụng nhằm sát khuẩn, virus gây bệnh. Để pha chế dung dịch này, sử dụng chloramine B 25% dạng bột, vậy cần bao nhiêu gam bột chloramine B 25% pha với 1 lít nước để được dung dịch sát khuẩn 2%

Gợi ý cho bạn
Xem tất cảNgân hàng đề thi

