Bài tập Phản ứng oxi hóa – khử và ứng dụng trong cuộc sống có đáp án
22 câu hỏi
Đom đóm có thể phát ra ánh sáng đặc biệt, không tỏa nhiệt như ánh sáng nhân tạo. Cấu tạo bên trong lớp da bụng của đom đóm là dãy các tế bào phát quang có chứa luciferin. Luciferin tác dụng với oxygen, cùng xúc tác enzyme, để tạo ra ánh sáng. Đây là phản ứng oxi hóa – khử.
Trong cuộc sống cũng như trong tự nhiên có nhiều hiện tượng mà nguyên nhân chính là do phản ứng oxi hóa – khử gây ra. Phản ứng oxi hóa – khử là gì? Vai trò quan trọng của chúng trong cuộc sống như thế nào? 
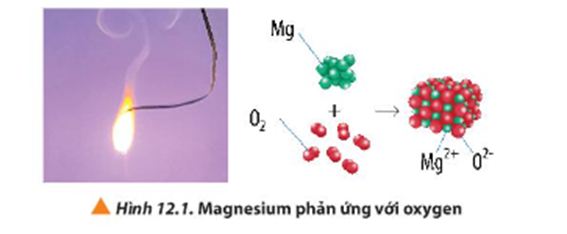
Quan sát Hình 12.1, hãy viết quá trình nhường và nhận electron trong phản ứng giữa magnesium và oxygen
Quan sát Hình 12.2a hydrogen cháy trong chlorine với ngọn lửa sáng, tạo hợp chất hydrogen chloride (HCl). Nếu cặp electron chung trong hợp chất cộng hóa trị HCl lệch hẳn về phía nguyên tử Cl (Hình 12.2b), hãy xác định điện tích của các nguyên tử trong phân tử HCl

Nêu điểm khác nhau giữa kí hiệu oxi hóa và kí hiệu điện tích của ion M trong hình sau:
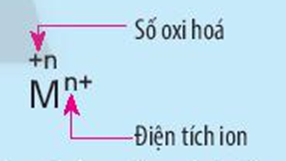
Dự đoán số oxi hóa của các nguyên tử trong nhóm IA, IIA, IIIA trong các hợp chất. Giải thích
Hãy xác định số oxi hóa của các nguyên tử trong các đơn chất, hợp chất và ion sau: Zn, H2, Cl‑, O2-, S2-, HSO4-, Na2S2O3, KNO3
Magnetite là khoáng vật sắt từ có hàm lượng sắt cao nhất được dùng trong ngành luyện gang, thép, với công thức hóa học là Fe3O4. Hãy xác định số oxi hóa của nguyên tử Fe trong hợp chất trên.

Hãy nhận xét và giải thích sự thay đổi số oxi hóa của các nguyên tử trong chất oxi hóa và chất khử trước và sau phản ứng.
Cho phương trình hóa học của các phản ứng sau:
H2S + Br2 → 2HBr + S↓ (1)
2KClO3 →t° 2KCl + 3O2↑ (2)
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O (3)
Phản ứng nào là phản ứng oxi hóa – khử? Vì sao? Hãy xác định quá trình oxi hóa và quá trình khử của các phản ứng đó
Làm thế nào để biết một phản ứng là phản ứng oxi hóa – khử?
Hãy nêu 3 ví dụ về phản ứng có sự thay đổi số oxi hóa của nguyên tử và 3 ví dụ về phản ứng không có sự thay đổi số oxi hóa của nguyên tử
Lập phương trình hóa học của các phản ứng oxi hóa - khử sau, xác định vai trò của các chất tham gia phản ứng.
KMnO4 + HCl → KCl + MnCl2 + Cl↑ + H2O (1)
NH3 + Br2 → N2 + HBr (2)
NH3 + CuO →t° Cu + N2 + H2O (3)
FeS2 + O2 →t° Fe2O3 + SO2 (4)
KClO3 →t° KCl + O2↑ (5)
Lập phương trình hóa học của phản ứng đốt cháy gas trong không khí và phản ứng kích nổ hỗn hợp nhiên liệu của tàu con thoi. Xác định vai trò của các chất trong mỗi phản ứng
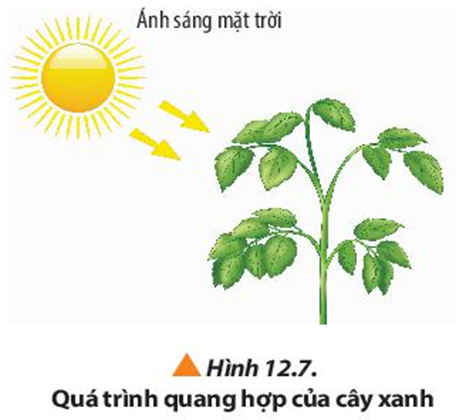
Quan sát Hình 12.7 và đọc thông tin, hãy lập phương trình hóa học của phản ứng quang hợp ở cây xanh. Quá trình quang hợp của thực vật có vai trò quan trọng như thế nào đối với cuộc sống?
Từ thông tin về “Luyện kim”, viết phản ứng của khí carbon monoxide khử iron(III) oxide ở nhiệt độ cao. Lập phương trình hóa học của phản ứng theo phương pháp thăng bằng electron, xác định vai trò của các chất trong phản ứng
Đọc thông tin về “Điện hóa” để biết được phản ứng oxi hóa – khử gắn liền với cuộc sống. Lập phương trình hóa học của phản ứng sinh ra dòng điện trong pin khi zinc phản ứng với manganese dioxide.
Hãy nêu thêm một số phản ứng oxi hóa – khử quan trọng gắn với đời sống hằng ngày
Tính số oxi hóa của nguyên tử có đánh dấu ∗ trong các chất và ion dưới đây:
a) K2Cr∗2O7; KMn∗O4; KCl∗O4; N∗H4NO3
b) Al∗O2−; P∗O43−; Cl∗O3−; S∗O42−
Lập phương trình hóa học của các phản ứng sau bằng phương pháp thăng bằng electron, nêu rõ chất oxi hóa, chất khử trong mỗi trường hợp
a) HCl + MnO2 →t° MnCl2 + Cl2↑ + H2O
b) KMnO4 + KNO2 + H2SO4 → MnSO4 + KNO3 + K2SO4 + H2O
c) Fe3O4 + HNO3 → Fe(NO3)3 + NO↑ + H2O
d) H2C2O2 + KMnO4 + H2SO4 → CO2↑ + MnSO4 + K2SO4 + H2O
Có nhiều hiện tượng xảy ra xung quanh ta, em hãy nêu hai phản ứng oxi hóa - khử gắn liền với cuộc sống hàng ngày và lập phương trình hóa học của các phản ứng đó bằng phương pháp thăng bằng electron.
Viết phương trình hóa học của phản ứng điều chế muối zinc chloride (ZnCl2) bằng một phản ứng oxi hóa - khử và một phản ứng không phải là phản ứng oxi hóa - khử.
Nhiên liệu rắn dành cho tên lửa tăng tốc của tàu vũ trụ con thoi là hỗn hợp gồm ammonium perchlorate (NH4ClO4) và bột nhôm. Khi được đốt đến trên 200oC, ammonium perchlorate nổ theo phản ứng sau:
NH4ClO4 →200oC N2↑ + Cl2↑ + O2↑ + H2O↑
Lập phương trình hóa học của phản ứng bằng phương pháp thăng bằng electron.
Gợi ý cho bạn
Xem tất cảNgân hàng đề thi

