Bài tập ôn tập Hóa 10 Cánh diều Chủ đề 7 có đáp án
50 câu hỏi
Nguyên tố nào sau đây là nguyên tố halogen?
Nitrogen.
Bromine.
Oxygen.
Carbon.
Ở điều kiện thường, đơn chất halogen nào sau đây tồn tại ở thể khí màu lục nhạt?
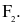
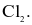
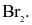
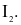
Cấu hình electron lớp ngoài cùng của các nguyên tử halogen có dạng
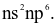
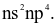
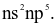
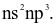
Khi đun nóng, chất thăng hoa chuyển từ thể rắn sang thể hơi màu tím là
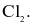
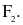
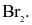
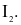
Đơn chất halogen nào sau đây là chất rắn ở điều kiện thường?
Iodine.
Bromine.
Chlorine.
Fluorine.
Liên kết trong đơn chất halogen là liên kết
cộng hóa trị khôngphân cực.
hydrogen.
ion.
cộng hóa trị phân cực.
Hòa tan khí 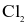 vào dung dịch KOH loãng, dư ở nhiệt độ phòng thu được dung dịch chứa các chất
vào dung dịch KOH loãng, dư ở nhiệt độ phòng thu được dung dịch chứa các chất
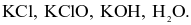
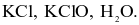
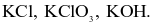
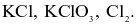
Trường hợp nào sau đây không xảy ra phản ứng?
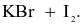
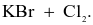
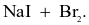
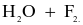
Cho phản ứng tổng quát sau: 
X có thể là chất nào sau đây?
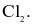
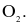
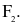
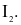
Dẫn 2 luồng khí chlorine đi qua 2 ống nghiệm đựng dung dịch KOH. Ống nghiệm thứ nhất đựng dung dịch KOH loãng và nguội, ống nghiệm thứ 2 đựng dung dịch KOH đậm đặc và đun nóng ở 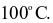 Sau khi phản ứng xảy ra hoàn toàn,nếu lượng muối KCl sinh ra trong 2 dung dịch bằng nhau thì tỉ lệ thể tích khí Cl2 qua dung dịch thứ nhất và dung dịch thứ 2 tương ứng là
Sau khi phản ứng xảy ra hoàn toàn,nếu lượng muối KCl sinh ra trong 2 dung dịch bằng nhau thì tỉ lệ thể tích khí Cl2 qua dung dịch thứ nhất và dung dịch thứ 2 tương ứng là
1 : 3.
5 : 3.
4 : 4.
2 : 4.
Quá trình sản xuất khí chlorine trong công nghiệp hiện nay dựa trên phản ứng là

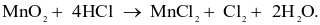
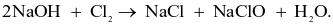
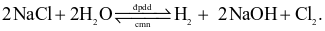
Phát biểu nào sau đây không đúng về tính chất vật lý của đơn chất halogen?
Fluorine là chất khí màu lục nhạt.
Chlorine là chất khí màu vàng lục.
Iodine dễ bị thăng hoa.
Bromine là chất lỏng không màu.
Trong tự nhiên, halogen
chỉ tồn tại ở dạng hợp chất.
chỉ tồn tại ở dạng đơn chất.
tồn tại ở dạng đơn chất hoặc hợp chất.
chỉ tồn tại trong cơ thể người và động vật.
Điều chế chlorine trong phòng thí nghiệm qua phương trình:
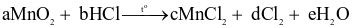
Với a, b, c, d, e là các số nguyên tối giản, giá trị a + b là
4.
9
5.
8.
Trong các hình vẽ mô tả cách thu khí chlorine sau đây, hình vẽ nào mô tả đúng cách thu khí chlorine trong phòng thí nghiệm?
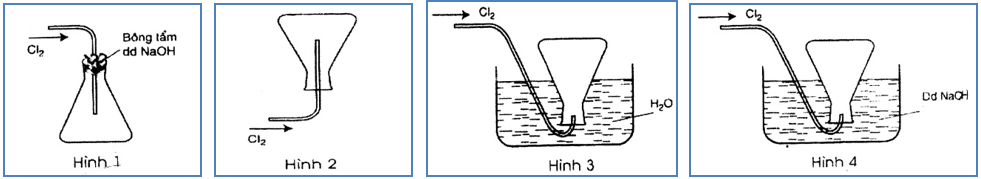
Hình 1.
Hình 2.
Hình 3.
Hình 4.
Để khắc chữ lên thủy tinh người ta dùng chất nào?
HF đặc.
HBr đặc.
HI đặc.
HCl đặc.
Dung dịch dùng để nhận biết các ion halide là
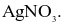
Quỳ tím.
NaOH.
HCl.
Nước Javel là hỗn hợp của các chất tan nào sau đây?
NaCl, NaClO.
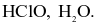
HCl, HClO.
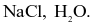
Phản ứng được dùng để điều chế khí hydrogen chloride trong phòng thí nghiệm là
2 + Cl2 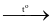 2HCl.
2HCl.
Cl2 + H2O  HCl + HClO .
HCl + HClO .
Cl2 + SO2 + 2H2O  2HCl + H2SO4.
2HCl + H2SO4.
NaClrắn + H2SO4 đặc 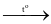 NaHSO4 + HCl.
NaHSO4 + HCl.
Ở áp suất thường, hydrogen halide (HX) nào sau đây có nhiệt độ sôi cao nhất?
HF.
HCl.
HBr.
HI.
Phát biểu nào sau đây liên quan đến halogen halide (HX) là không đúng?
Các halogen halide dễ tan trong nước phân li hoàn toàn thanh 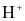 và
và 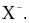
Liên kết H – I kém bền nhất trong các liên kết H – X.
Tính acid của các hydrogen halide tăng dần từ HF đến HI.
Liên kết trong phân tử hydrogen halide là liên kết công hóa trị không phân cực.
Trong dãy hydrogen halide, từ HCl đến HI, nhiệt độ sôi tăng dần chủ yếu do
tương tác vander Waals tăng dần.
phân tử khối tăng dần.
độ bền liên kết giảm dần.
độ phân cực liên kết giảm dần.
Cho muối halide nào sau đây tác dụng với dung dịch 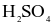 đặc, nóng thì chỉ xảy ra phản ứng trao đổi?
đặc, nóng thì chỉ xảy ra phản ứng trao đổi?
KBr.
KI.
NaCl.
NaBr.
Ion halide được sắp xếp theo chiều giảm dần tính khử:
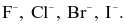
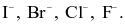
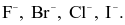
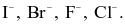
Ở cùng điều kiện áp suất, hydrogen fluoride (HF) có nhiệt độ sôi cao vượt trội so với các hydrogen halide còn lại là do
fluorine có nguyên tử khối nhỏ nhất.
năng lượng liên kết H – F bền vững làm cho HF khó bay hơi.
các nhóm phân tử HF được tạo thành do có liên kết hydrogen giữa các phân tử.
fluorine là phi kim mạnh nhất.
Cho phản ứng hóa học: 3Cl2 + 6KOH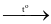 5KCl + KClO3 + H2O
5KCl + KClO3 + H2O
Tỉ lệ giữa số nguyên tử chlorine đóng vai trò chất oxi hóa và số nguyên tử chlorine đóng vai trò chất khử trong phương trình hóa học của phản ứng đã cho tương ứng là
3: 1.
1: 3.
5: 1.
1: 5.
Có hai ống nghiệm, mỗi ống chứa 2 mL dung dịch muối của sodium. Cho vài giọt dung dịch 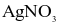 vào ống thứ nhất, thu được kết tủa. Nhỏ vài giọt nước
vào ống thứ nhất, thu được kết tủa. Nhỏ vài giọt nước 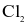 vào ống thứ hai, lắc nhẹ, thêm 1 mL benzene và lắc đều, lớp benzene từ không màu chuyển sang màu nâu đỏ. Công thức của muối sodium là
vào ống thứ hai, lắc nhẹ, thêm 1 mL benzene và lắc đều, lớp benzene từ không màu chuyển sang màu nâu đỏ. Công thức của muối sodium là
NaBr.
NaF.
NaCl.
NaI.
Dung dịch nào sau đây có thể phân biệt hai dung dịch NaF và NaCl?
HCl.
HF.
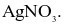
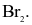
Hydrochloric acid thể hiện tính oxi hoá khi tác dụng với chất nào sau đây?
Fe.
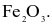
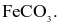
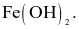
Các nguyên tố phổ biến thuộc nhóm halogen (VIIA) trong bảng tuần hoàn các nguyên tố hóa học gồm: F (Z = 9), Cl (Z = 17), Br (Z = 35) và I (Z = 53). Đơn chất halogen tồn tạo dạng phân tử 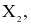 giữa các phân tử
giữa các phân tử 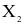 thường có tương tác với nhau. Cho giá trị năng lượng liên kết
thường có tương tác với nhau. Cho giá trị năng lượng liên kết 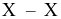 ở bảng sau:
ở bảng sau:
| Liên kết | F - F | Cl - Cl | Br - Br | I - I |
Năng lượng liên kết (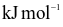 ) )ở | 159 | 243 | 193 | 151 |
Năng lượng liên kết X – X càng lớn thì liên kết càng bền.
(a) Cấu hình electron lớp ngoài cùng của nguyên tử X có dạng 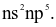
(b) Liên kết giữa các nguyên tử trong 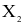 là liên kết cộng hóa trị không phân cực.
là liên kết cộng hóa trị không phân cực.
(c) Tương tác giữa các phân tử 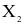 là tương tác van der Waals.
là tương tác van der Waals.
(d) Năng lượng liên kết Cl – Cl lớn nhất trong dãy trên vì Cl có bán kính nguyên tử nhỏ nhất.
Cho các nhận định về các nguyên tố halogen như sau:
(a)Màu các đơn chất đậm dần theo thứ tự 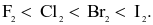
(b)Nếu chẳng may làm đổ bromine lỏng xuống bàn làm thí nghiệm, có thể dùng nước vôi để loại bỏ hoàn toàn lượng bromine này.
(c)Trong phản ứng với hydrogen, khả năng phản ứng của halogen tăng dần từ 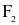 đến
đến 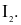
(d)Liên kết trong phân tử halogen là liên kết cộng hóa trị không phân cực.
Cho hình vẽ mô tả thí nghiệm điều chế chlorine từ MnO2 và dung dịch HCl:
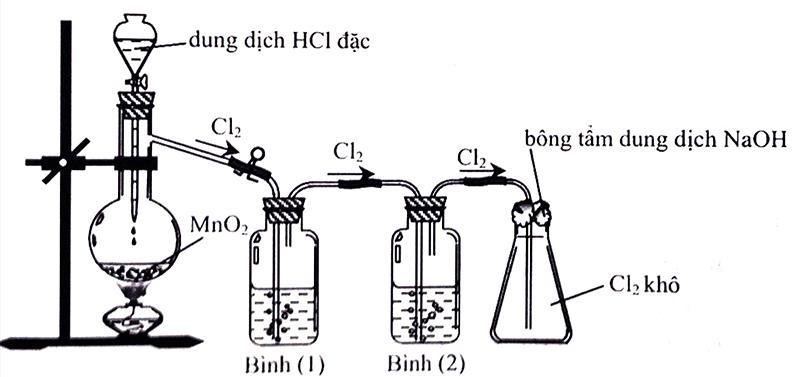
(a) Để thu được khí chlorine khô thì bình (1) và bình (2) lần lượt đựng dung dịch NaCl bão hòa và dung dịch H2SO4 đặc.
(b) Bông tẩm dung dịch NaOH dùng để ngăn không cho khí chlorine thoát ra ngoài.
(c) Có thể thay acid HCl đặc bằng acid H2SO4 đặc.
(d) Có thể thu khí chlorine bằng phương pháp đẩy nước.
Javel là chất oxi hóa mạnh nên nó có khả năng phân hủy phân tử hữu cơ hiệu quả, tất cả các loại vi trùng nguy hại và chất có mùi khó ngửi như urea, ammonia. Chính vì vậy, Javel thường được dùng trong việc tẩy quần áo, vệ sinh nhà cửa ... Trong công nghiệp, nước Javel được sản xuất bằng cách điện phân dung dịch sodium chloride bão hòa trong thùng điện phân không có màng ngăn. Giai đoạn 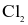 tác dụng với dung dịch NaOH tạo nước Javel theo phương trình sau:
tác dụng với dung dịch NaOH tạo nước Javel theo phương trình sau:
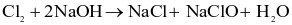
(a) NaClO là chất giúp nước Javel có tính oxi hóa.
(b) Số oxi hóa của Cl trong NaClO là +2
(c) Ứng dụng của nước Javel dùng để tẩy trùng, tẩy trắng...
(d) Trong phản ứng trên 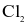 vừa là chất oxi hóa, vừa là chất khử.
vừa là chất oxi hóa, vừa là chất khử.
Theo nghiên cứu của Đại học Harvard vào năm 2013, trẻ em sinh sống tại những khu vực có nguồn nước bị nhiễmfluorine có chỉ số IQ trung bình sẽ thấp hơn so với những trẻ em sống tại vùng khác. Anion F− (fluoride) có độc tính mạnh với hệ thần kinh. Với lượng tương đối thấp: 0,2 gam ion F− trên cơ thể có trọng lượng 70 kg có thể gây tử vong. Tuy nhiên, sự có mặt của anion fluoride lại giúp men răng chắc khỏe và chống chọi các bệnh về sâu răng, vì vậy anion fluoride được thêm vào nước uống đóng chai với nồng độ 1mg ion F− trên 1L nước và bổ sung một lượng nhỏ dưới dạng muối sodium fluoride (NaF) trong kem đánh răng.
(a) NaF là hợp chất cộng hóa trị phân cực và tan tốt trong nước.
(b) Trong tinh thể NaF, mỗi ion Na+ được bao quanh bởi 6 ion F− gần nhất.
(c) Muối sodium fluoride giúp bảo vệ răng chắc khỏe và chống sâu răng.
(d) Theo hiệp hội nha khoa Hoa Kỳ, một người trưởng thành nên bổ sung 3,0 mg 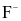 mỗi ngày dưới dạng muối sodium fluoride (NaF) để ngăn ngừa sâu răng. Lượng NaF không gây độc cho cơ thể khi ở mức
mỗi ngày dưới dạng muối sodium fluoride (NaF) để ngăn ngừa sâu răng. Lượng NaF không gây độc cho cơ thể khi ở mức 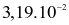 gam/1kg cơ thể. Một mẫu kem đánh răng chứa 0,28% NaF, một người nặng 75 kg nếu vô tình nuốt phải 50 gam kem đánh răng có thể bị ngộ độc.
gam/1kg cơ thể. Một mẫu kem đánh răng chứa 0,28% NaF, một người nặng 75 kg nếu vô tình nuốt phải 50 gam kem đánh răng có thể bị ngộ độc.
Phản ứng giữa chlorine và hydrogencần điều kiện ánh sáng hoặc nhiệt độ xảy theo phương trình:

(a)Chlorine là chất khí có màu nâu đỏ.
(b)Chlorine đóng vai trò là chất oxi hóa.
(c) Dung dịch HCl khi tác dụng với 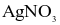 sản phẩm xuất hiện kết tủa màu trắng.
sản phẩm xuất hiện kết tủa màu trắng.
(d) Liên kết giữa H với Cl trong HCl là liên kết cộng hóa trị phân cực.
Trong dịch vị dạ dày của người có hydrohalic acid X với nồng độ khoảng 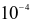 đến
đến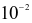 mol/L, đóng vai trò quan trọng trong quá trình tiêu hoá, cùng với enzyme và sự co bóp của cơ dạ dày nhằm chuyển hoá thức ăn thành chất dinh dưỡng cho cơ thể dễ hấp thụ.
mol/L, đóng vai trò quan trọng trong quá trình tiêu hoá, cùng với enzyme và sự co bóp của cơ dạ dày nhằm chuyển hoá thức ăn thành chất dinh dưỡng cho cơ thể dễ hấp thụ.
(a) X là hydrochloric acid.
(b) Dung dịch hydrohalic acid X làm quỳ tím chuyển màu đỏ.
(c) Hydrohalic acid X được dùng để tẩy rửa gỉ sét trên bề mặt gang, thép.
(d) Hydrohalic acid X là một acid yếu.
Thuỷ tinh vốn cứng, trơn và khá trơ về mặt hoá học nênviệc chạm khắc là điều không đơn giản. Muốn khắc cáchoa văn, cần phủ lên bề mặt thuỷ tinh một lớp paraffin, thực hiện chạm khắc các hoa văn lên lớp paraffin, để phầnthuỷ tinh cần khắc lộ ra. Nhỏ dung dịch hydrofluoric acid hoặc hỗn hợp 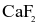 và
và 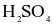 đặc lên lớp paraffin đó, phầnthuỷtinh cần chạm khắc sẽ bị ăn mòn, tạo nên những hoavăn trên vật dụng cần trang trí.
đặc lên lớp paraffin đó, phầnthuỷtinh cần chạm khắc sẽ bị ăn mòn, tạo nên những hoavăn trên vật dụng cần trang trí.
(a) HF là là acid mạnh và có tính chất đặc biệt là ăn mòn thuỷ tinh.
(b) Phương trình hoá học của phản ứng ăn mòn thủy tinh là: 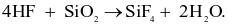
(c) Để bảo quản hydrofluoric acid, người ta chứa trong bình bằng nhựa.
(d) Tất cả các hydrohalic acid đều có khả năng ăn mòn thủy tinh.
Nhiệt độ sôi của các hydrogen halide được biểu diễn qua đồ thị sau:
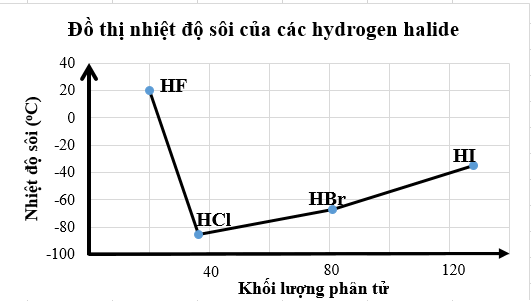
(a) Các phân tử hydrogen fluoride hình thành liên kết hydrogen liên phân tử nên nhiệt độ sôi của hydrogen fluoride cao bất thường so với các hydrogen halide còn lại.
(b) Nhiệt độ sôi của hydrogen fluoride cao bất thường so với các hydrogen halide còn lại là do lực tương tác van der Waals của HF lớn hơn.
(c) Nhiệt độ sôi tăng dần từ HF đến HI do khối lượng phân tử tăng dẫn đến tương tác van der Waals tăng.
(d) Nhiệt độ sôi của các hydrogen halide tăng dần từ HCl đến HI là do khối lượng phân tử tăng dẫn đến liên kết hydrogen liên phân tử tăng dần.
“Natri clorid 0,9%” là nước muối sinh lí chứa sodium chloride (NaCl), nồng độ 0,9% tương đương các dịch trong cơ thể người như máu, nước mắt, … thường được sử dụng để súc miệng, sát khuẩn, …
(a)Rót nước sạch vào cốc đến vạch thể tích mong muốn, cho muối vào, khuấy đều đến khi nếm thấy độ mặn vừa phải thì dừng lại, thu được nước muối sinh lí 0,9%.
(b) Natri chlorid 0,9% được lấy từ nước biển ngoài khơi xa ở độ sâu 500 m để đảm bảo độ tinh khiết.
(c) NaCl là hợp chất ion, dễ tan trong nước.
(d)Cách pha chế 500 mL nước muối sinh lí trên: cân 0,9 g tinh thể NaCl sạch, cho vào cốc có vạch chia thể tích 500 mL, thêm nước vào cốc đến đủ thể tích 500 mL, khuấy đều (biết 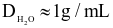 ).
).
Thực hiện các thí nghiệm sau:
(a) 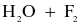

(b) Dung dịch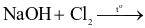
(c) Dung dịch 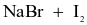

(d) Dung dịch 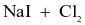

Ở điều kiện thích hợp, có bao nhiêu phản ứng tạo ra đơn chất?
Hydrochloric acid (HCl) là một acid mạnh được sử dụng trong các ngành công nghiệp sản xuất phân bón, thuốc nhuộm, ... Nó cũng được sử dụng trong các ngành công nghiệp mạ điện, chiết xuất ảnh, cao su và dệt may. Cho dung dịch acid HCl tác dụng với các chất sau: Zn, Cu, 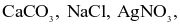 FeO. Số chất phản ứng được với dung dịch HCl là bao nhiêu?
FeO. Số chất phản ứng được với dung dịch HCl là bao nhiêu?
Cho các phương trình phản ứng sau:
(a) 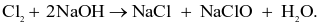
(b) 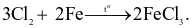
(c) 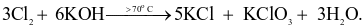
(d) 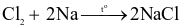
(e) 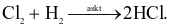
Số phản ứng trong đó Cl2 chỉ đóng vai trò chất oxi hóa là bao nhiêu?
Cho 13,05 gam 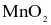 tác dụng với acid HCl đặc, dư. Khí chlorine sinh ra tác dụng vừa đủ với bao nhiêu gam sắt?
tác dụng với acid HCl đặc, dư. Khí chlorine sinh ra tác dụng vừa đủ với bao nhiêu gam sắt?
“Muối i-ốt” có thành phần chính là sodium chloride (NaCl) có bổ sung một lượng nhỏ potassium iodide (KI) nhằm bổ sung nguyên tố vi lượng iodine cho cơ thể, nhằm ngăn bệnh bướu cổ, phòng ngừa khuyết tật trí tuệ và phát triển, … Trong 100 g “muối i-ốt” có chứa hàm lượng ion iodide 2 200 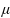 g; lượng iodide cần thiết cho một người trưởng thành khoảng 88
g; lượng iodide cần thiết cho một người trưởng thành khoảng 88 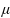 g/ngày. Trung bình, một người trưởng thành cần bao nhiêu gam “muối i-ốt” trong một ngày?
g/ngày. Trung bình, một người trưởng thành cần bao nhiêu gam “muối i-ốt” trong một ngày?
Trong công nghiệp, nước Javel được sản xuất bằng cách điện phân dung dịch muối ăn (nồng độ từ 15 – 20%) trong thùng điện phân không có màng ngăn. Loại nước Javel dùng để tẩy vết bẩn quần áo trên thị trường thường được đóng vào chai dung tích 1 lít có nồng độ NaClO và NaCl lần lượt là 6% và 5% (khối lượng riêng của dung dịch nước Javel D = 1,1 g/mL). Cần bao nhiêu kg NaCl nguyên chất để sản xuất 1000 chai nước Javel nói trên. (Kết quả làm tròn đến hàng phần mười)
Trong công nghiệp, xút (sodium hydroxide) được sản xuất bằng phương pháp điện phân dung dịch sodium chloride có màng ngăn xốp. Bằng phương pháp này, người ta cũng thu được khí chlorine (sơ đồ minh hoạ). Chất khí này được làm khô (loại hơi nước) rồi hoá lỏng để làm nguyên liệu quan trọng cho nhiều ngành công nghiệp chế biến và sản xuất hoá chất.
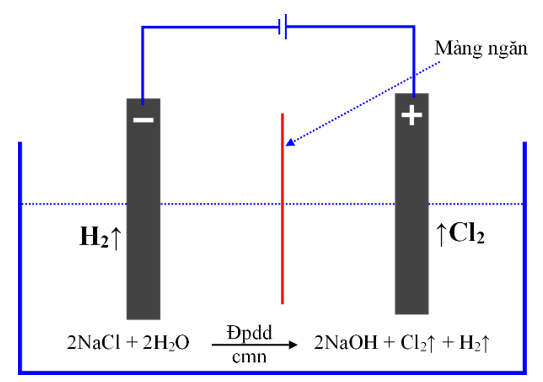
Từ quá trình điện phân nêu trên, một lượng chlorine và hydrogen sinh ra được tận dụng để sản xuất hydrochloric acid đặc thương phẩm (32%, D = 1,153 g mL-1 ở 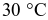 ). Một nhà máy với quy mô sản xuất 200 tấn xút mỗi ngày thì đồng thời sản xuất được bao nhiêu m3 acid thương phẩm trên. Biết rằng, tại nhà máy này, 60% khối lượng chlorine sinh ra được dùng tổng hợp hydrochloric acid và hiệu suất của toàn bộ quá trình từ chlorine đến acid thương phẩm đạt 80% về khối lượng. (Kết quả làm tròn đến hàng phần mười)
). Một nhà máy với quy mô sản xuất 200 tấn xút mỗi ngày thì đồng thời sản xuất được bao nhiêu m3 acid thương phẩm trên. Biết rằng, tại nhà máy này, 60% khối lượng chlorine sinh ra được dùng tổng hợp hydrochloric acid và hiệu suất của toàn bộ quá trình từ chlorine đến acid thương phẩm đạt 80% về khối lượng. (Kết quả làm tròn đến hàng phần mười)
Một nhà máy nước sử dụng 4 mg Cl2 để khử trùng 1 L nước sinh hoạt. Tính khối lượng (kg) Cl2 nhà máy cần dùng để khử trùng 60000 m3 nước sinh hoạt.
Đốt 2,88 gam kim loại R (hóa trị II) trong khí Cl2 (dư). Sau khi phản ứng xảy ra hoàn toàn, thu được 11,4 gam muối chloride của kim loại R. Khối lượng mol của R có giá trị bằng bao nhiêu? (Biết nguyên tử khối của Cl = 35,5)
Dựa vào độ âm điện, liên kết nào sau đây có độ phân cực lớn nhất?
H – F.
H – Cl.
H – Br.
H – I.
Người ta thường tách bromine trong rong biển bằng quá trình sục khí chlorine vào dung dịch chiết chứa ion bromide. Phương trình hoá học của phản ứng có thể được mô tả dạng thu gọn như sau:

Cho các số liệu enthalpy tạo thành chuẩn 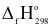 (kJ mol-1) trong bảng dưới đây:
(kJ mol-1) trong bảng dưới đây:
| Br - (aq) | Cl - (aq) | Br 2 (aq) | Cl 2 (aq) |
| -121,55 | -167,16 | -2,16 | -17,30 |
Tính biến thiên enthalpy chuẩn phản ứng trên (đơn vị: kJ).

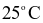 và 1 bar
và 1 bar