Bài tập Liên kết hóa học có đáp án
14 câu hỏi
Dạng hình học phân tử ảnh hưởng đến khả năng phản ứng, hoạt tính sinh học, tính phân cực, … của phân tử. Dựa trên cơ sở nào để dự đoán dạng hình học của một phân tử?
Công thức Lewis của CS2 là
A. 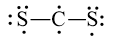
B.
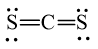
C.
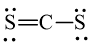
D. S = C = S
Trình bày các bước để viết công thức Lewis của phân tử NH3.
Viết các công thức Lewis cho mỗi phân tử sau:
a) Cl2; N2.
b) SO2; SO3.
c) H2O; H2S; HOCl.
Công thức Lewis biểu diễn cấu tạo của NO2 là
A. O = N = O
B.
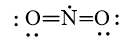
C.
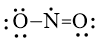
D.
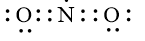
Công thức của PCl3 theo mô hình VSEPR là
A. AX3.
B. AXE2.
C. AX3E.
D. AX2E.
Viết công thức của một số phân tử sau theo mô hình VSEPR: CCl4, H2S, CO2, SO3 và PH3. Nêu số cặp electron hóa trị liên kết và chưa liên kết trong mỗi phân tử.
Viết công thức theo mô hình VSEPR và cho biết dạng hình học của phân tử OF2. Phân tử này có phân cực không?
Dạng hình học của ion NH4+ là
A. tứ diện đều.
B. tháp tam giác.
C. tam giác phẳng.
D. đường thẳng.
Dự đoán dạng hình học của một số phân tử sau: CO2, CS2, BF3, SCl2.
Các nguyên tử carbon (1), (2), (3) trong hình bên ở những trạng thái lai hóa nào?
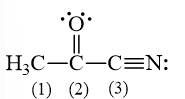
Mô tả sự tạo thành các phân tử sau theo khái niệm lai hóa orbital.
a) Phân tử BeH2.
b) Phân tử SO2.
c) Phân tử NH3.
Cho các phân tử NCl3, SO3, CO2.
a) Nguyên tử trung tâm trong các phân tử trên ở trạng thái lai hóa nào?
b) Phân tử nào không phân cực, phân tử nào phân cực? Vì sao?
Vận dụng công thức phân tử theo mô hình VSEPR đề dự đoán dạng hình học và vận dụng khái niệm lai hoá orbital để giải thích dạng hình học đã dự đoán theo công thức phân tử theo mô hình VSEPR.
