45 câu hỏi
Xét hệ cân bằng gồm ba chất có mặt trong phản ứng sau: NH4Cl(r) ⇌ HCl(k) + NH3(k).
(1) Hệ có số cấu tử là 3, số pha là 2, số bậc tự do là 2.
(2) Hệ có số cấu tử là 2, số pha là 2, số bậc tự do là 2.
(3) Nếu nồng độ HCl và NH3 bằng nhau thì số cấu tử của hệ là 1, số pha là 2, số bậc tự do là 1.
(4) Nếu nồng độ HCl và NH3 bằng nhau thì số cấu tử của hệ là 2, số pha là 2, số bậc tự do là 2.
1, 4
2, 4
2, 3
1, 3
Chọn phương án đúng: Đối với một hệ hơi nước: (1) Có thể thay đổi cả nhiệt độ và áp suất của hệ trong phạm vi cho phép để hệ vẫn ở trạng thái hơi. (2) Phải giữ nhiệt độ của hệ trên 100°C để hệ vẫn ở trạng thái hơi. (3) Nếu nhiệt độ của hệ bị hạ xuống dưới 100°C, hệ sẽ chuyển sang trạng thái lỏng.
Chỉ 2 đúng
Chỉ 3 đúng
Chỉ 1 đúng
1, 2, 3 đúng
Trong giản đồ sau, đường biểu diễn cân bằng Rắn ⇌ Khí là:
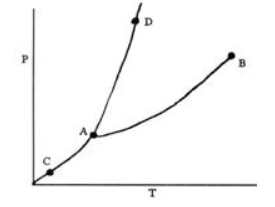
AC
AB
CD
AD
Chọn phát biểu đúng: Đối với phản ứng một chiều, tốc độ phản ứng sẽ:
Không đổi theo thời gian.
Giảm dần theo thời gian cho đến khi bằng không.
Giảm dần theo thời gian cho đến khi bằng một hằng số khác không.
Tăng dần theo thời gian.
Chọn câu sai. Hằng số tốc độ phản ứng:
Không phụ thuộc chất xúc tác.
Không phụ thuộc nồng độ chất phản ứng.
Phụ thuộc nhiệt độ.
Phụ thuộc năng lượng hoạt hóa của phản ứng.
Chọn câu sai: Hằng số tốc độ của phản ứng nA + mB = AnBm
Phụ thuộc vào nồng độ CA và CB.
Biến đổi khi nhiệt độ thay đổi.
Là tốc độ riêng của phản ứng khi CA = CB = 1 mol/l.
Biến đổi khi có mặt chất xúc tác.
Chọn đáp án đúng: Cho phản ứng: 2A(k) + B(k) ® C(k). Biểu thức tốc độ phản ứng phải là:
v = k.CA2.CB
v = k. Cc
v = k.CAm.CBn, với m và n là những giá trị tìm được từ thực nghiệm
v = k.CAm.CBn, với m và n là những giá trị tìm được từ phương trình phản ứng
Phản ứng phân hủy oxit dinitơ có sơ đồ tổng quát: 2N2O(k) ® 2N2(k) + O2(k), với v = k[N2O]. Người ta cho rằng phản ứng trải qua hai bước sơ cấp: Bước 1: N2O ® N2 + O. Bước 2: N2O + O ® N2 + O2. Vậy, phát biểu nào dưới đây phù hợp với các dữ liệu trên:
Phản ứng phân hủy dinitơ oxit có bậc động học bằng 2
Oxi nguyên tử là xúc tác của phản ứng
Bước 2 là bước quyết định tốc độ phản ứng
Bước 1 có phân tử số là đơn phân tử
Chọn ý sai: Cho phản ứng aA + bB = cC + dD có \[{\rm{v = kC}}_{\rm{A}}^{\rm{m}}{\rm{C}}_{\rm{B}}^{\rm{n}}\]. Bậc của phản ứng: (1) Luôn bằng (n + m) ; (2) Ít khi lớn hơn 3 ; (3) Bằng (c+d) – (a+b) ; (4) Có thể là phân số ; (5) Bằng (a + b).
3 và 5
2 và 3
3 và 4
2, 3 và 5
Cho phản ứng: 2H2 (k) + O2 (k) ® 2H2O (k). Tốc độ trung bình của phản ứng được xác định theo [O2] là \[{\rm{\bar v = }}\frac{{ - {\rm{\Delta }}\left[ {{{\rm{O}}_{\rm{2}}}} \right]}}{{{\rm{\Delta \tau }}}}\]. Chọn biểu thức đúng của \[{\rm{\bar v}}\]nếu biểu diễn theo [H2O].
\[{\rm{\bar v = }}\frac{{{\rm{\Delta }}\left[ {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right]}}{{{\rm{\Delta \tau }}}}\]
\[{\rm{\bar v = }}\frac{{{\rm{2\Delta }}\left[ {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right]}}{{{\rm{\Delta \tau }}}}\]
\[{\rm{\bar v = }}\frac{{ - {\rm{2\Delta }}\left[ {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right]}}{{{\rm{\Delta \tau }}}}\]
\[{\rm{\bar v = }}\frac{{{\rm{\Delta }}\left[ {{{\rm{H}}_{\rm{2}}}{\rm{O}}} \right]}}{{{\rm{2}}{\rm{.\Delta \tau }}}}\]
Đại lượng nào sau đây của phản ứng sẽ thay đổi khi được thêm xúc tác:
∆H
∆G
E*
Kcb
Chọn đáp án đúng: Một phản ứng có năng lượng hoạt hóa là 4,82 × 102 cal/mol. Nếu ở 275K phản ứng có hằng số tốc độ là 8,82 × 10-5, thì ở 567K hằng số tốc độ là:
6,25
1,39 ×10-4
5,17 ×102
36 ×10-3
Chọn đáp án đúng: Một phản ứng bậc nhất có chu kỳ bán hủy là 45 phút 30 giây. Xác định hằng số tốc độ của phản ứng trên.
2,54×10-4s-1
3,66×10-4s-1
1,89×103s-1
1,78×102s-1
Chọn phương án đúng: Phản ứng 2A + 2B + C ® D + E có các đặc điểm sau:
* [A], [B] không đổi, [C] tăng gấp đôi, vận tốc v không đổi.
* [A], [C] không đổi, [B] tăng gấp đôi, vận tốc v tăng gấp đôi.
* [A], [B] đều tăng gấp đôi, vận tốc V tăng gấp 8 lần.
Cả ba thí nghiệm đều ở cùng một nhiệt độ. Biểu thức của vận tốc v theo các nồng độ A, B, C là:
v = k[A][B][C]
v = k[A]2[B]
v = k[A][B]2
v = k[A]2[B][C]
Chọn phương án đúng: Một phản ứng A + 2B = C bậc 1 đối với [A] và bậc 1 đối với [B], được thực hiện ở nhiệt độ không đổi.
Nếu [A], [B] và [C] đều gấp đôi, vận tốc phản ứng tăng gấp 8 lần và phản ứng là phản ứng đơn giản.
Nếu [A] và [B] đều tăng gấp đôi, vận tốc phản ứng tăng lên gấp 4 lần và phản ứng này là phản ứng đơn giản.
Nếu [A] tăng gấp đôi, [B] tăng gấp ba, vận tốc phản ứng tăng lên gấp 6 lần và phản ứng này là phản ứng phức tạp.
Nếu [A] và [B] đều tăng gấp ba, vận tốc phản ứng tăng lên gấp 6 lần và phản ứng này là phản ứng đơn giản.
Chọn phương án đúng: Phản ứng CO(k) + Cl2(k) ® COCl2(k) là phản ứng đơn giản. Nếu nồng độ CO tăng từ 0,1M lên 0,4M; nồng độ Cl2 tăng từ 0,3M lên 0,9M thì tốc độ phản ứng thay đổi như thế nào?
Tăng 3 lần
Tăng 4 lần
Tăng 7 lần
Tăng 12 lần
Chọn phương án đúng: Trong các phương trình sau đây, phương trình nào chắc chắn không thể biểu thị cho một tác dụng cơ bản (phản ứng sơ cấp)?
1) N2 + 3H2 ® 2NH3
2) \[\frac{{\rm{1}}}{{\rm{2}}}{{\rm{N}}_{\rm{2}}}{\rm{ + }}\frac{{\rm{3}}}{{\rm{2}}}{{\rm{H}}_{\rm{2}}} \to {\rm{N}}{{\rm{H}}_{\rm{3}}}\]
3) 8NO + 4O2 ® 8NO2
4) \[{{\rm{H}}_{\rm{2}}}{\rm{ + }}\frac{{\rm{1}}}{{\rm{2}}}{{\rm{O}}_{\rm{2}}} \to {{\rm{H}}_{\rm{2}}}{\rm{O}}\]
1, 3
2, 4
2, 3, 4
1, 2, 3, 4
Chọn đáp án đúng: Đối với phản ứng: 4NH3 + 3O2 ® 2N2 + 6H2O. Tốc độ tạo ra N2 là 0,270 mol/lít.s. Ta có: (1) Tốc độ tạo thành H2O là 0,540 mol/lít.s. (2) Tốc độ mất đi của NH3 là 0,810 mol/lít.s. (3) Tốc độ mất đi của O2 là 0,405 mol/lít.s. (4) Tốc độ của phản ứng là 0,135 mol/lít.s.
3
3, 4
1, 4
1, 2
Chọn phát biểu đúng: Tốc độ phản ứng đồng thể khí tăng khi tăng nồng độ là do:
Tăng entropi của phản ứng.
Giảm năng lượng hoạt hóa của phản ứng.
Tăng số va chạm của các tiểu phân hoạt động.
Tăng hằng số tốc độ của phản ứng.
Chọn phát biểu đúng: Sự tăng nhiệt độ có tác động đến một phản ứng thuận nghịch:
Làm tăng vận tốc cả chiều thu và tỏa nhiệt, làm cho hệ mau đạt đến trạng thái cân bằng mới.
Chỉ làm tăng vận tốc chiều thu nhiệt.
Chỉ làm tăng vận tốc chiều tỏa nhiệt.
Tăng đồng đều vận tốc cả chiều thu và tỏa nhiệt nên cân bằng không thay đổi.
Khi tăng nhiệt độ, tốc độ phản ứng tăng vì sự tăng nhiệt độ đó:
Làm cho DG < 0.>
Làm giảm năng lượng hoạt hóa.
Chủ yếu là làm tăng số lần va chạm giữa các phân tử.
Làm tăng số phân tử có năng lượng lớn hơn năng lượng hoạt hóa.
Chọn phát biểu đúng: Chất xúc tác có ảnh hưởng như thế nào đến trạng thái cân bằng của phản ứng tỏa nhiệt?
Làm tăng năng lượng của các tiểu phân.
Làm cho phản ứng nhanh đạt tới cân bằng.
Làm cho phản ứng xảy ra hoàn toàn.
Làm tăng hiệu suất của phản ứng theo chiều thuận.
Chọn đáp án đúng: Khi có mặt chất xúc tác, DH° của phản ứng:
Thay đổi vì chất xúc tác tham gia vào quá trình phản ứng.
Thay đổi vì chất xúc tác làm giảm nhiệt độ cần có để phản ứng xảy ra.
Không thay đổi vì chất xúc tác chỉ tham gia vào giai đoạn trung gian của phản ứng và được phục hồi sau phản ứng. Sản phẩm và tác chất vẫn giống như khi không có chất xúc tác.
Thay đổi vì chất xúc tác làm giảm năng lượng hoạt hóa của phản ứng.
Chọn các đặc tính đúng của chất xúc tác. Chất xúc tác làm cho tốc độ phản ứng tăng lên nhờ các đặc tính sau: (1) Làm cho DG của phản ứng âm hơn. (2) Làm tăng vận tốc phản ứng nhờ làm giảm năng lượng hoạt hóa của phản ứng. (3) Làm tăng vận tốc của phản ứng nhờ làm tăng vận tốc chuyển động của các tiểu phân. (4) Làm cho DG của phản ứng đổi dấu từ dương sang âm.
2
1, 2 và 3
1 và 2
2 và 4
Chọn câu sai trong các câu sau. Chất xúc tác:
Không làm thay đổi các đặc trưng nhiệt động của phản ứng.
Chỉ có tác dụng xúc tác với một phản ứng nhất định.
Làm thay đổi hằng số cân bằng của phản ứng.
Làm giảm năng lượng hoạt hóa của phản ứng.
Chọn ý sai: Tốc độ phản ứng càng lớn khi:
Entropi hoạt hóa càng lớn.
Năng lượng hoạt hóa của phản ứng càng lớn.
Số va chạm có hiệu quả giữa các tiểu phân càng lớn.
Nhiệt độ càng cao.
Chọn câu đúng: Tốc độ của phản ứng dị thể:
Của bất kỳ phản ứng nào cũng tăng lên khi khuấy trộn
Chỉ được quyết định bởi tương tác hóa học của bản thân chất phản ứng
Phụ thuộc vào bề mặt tiếp xúc pha mà không phụ thuộc vào nồng độ chất phản ứng
Tăng lên khi tăng bề mặt tiếp xúc pha
Chọn câu đúng. Tốc độ của phản ứng hòa tan kim loại rắn trong dung dịch acid sẽ: (1) Giảm xuống khi giảm nhiệt độ phản ứng. (2) Tăng lên khi tăng kích thước các hạt kim loại. (3) Giảm xuống khi giảm áp suất phản ứng. (4) Tăng lên khi tăng nồng độ acid.
1 và 4
1, 2 và 4
1, 3 và 4
1, 2 và 3
Chọn đáp án đúng và đầy đủ nhất: Có một số phản ứng tuy có DG < 0 song trong thực tế phản ứng vẫn không xảy ra. Vậy có thể áp dụng những biện pháp nào trong các cách sau để phản ứng xảy ra: (1) Dùng xúc tác ; (2) Thay đổi nhiệt độ ; (3) Tăng nồng độ tác chất ; (4) Nghiền nhỏ các tác chất rắn.
>
1 và 3
1 và 2
1, 2 và 4
2, 3 và 4
Chọn phương án đúng: Phản ứng N2(k) + O2(k) ® 2NO(k) tỏa nhiệt. Tốc độ của phản ứng này sẽ tăng lên khi áp dụng các biện pháp sau: (1) Dùng xúc tác ; (2) Nén hệ; (3) Tăng nhiệt độ ; (4) Giảm áp suất hệ phản ứng.
1, 3, 4
2, 3, 4
1, 2, 3
1, 2
Chọn đáp án đúng: Một phản ứng kết thúc sau 3 giờ ở 20°C. Ở nhiệt độ nào phản ứng sẽ kết thúc sau 20 phút, biết hệ số nhiệt độ của phản ứng là 3.
ở 30°C
ở 40°C
ở 50°C
ở 60°C
Chọn đáp án đúng: Phản ứng thuận nghịch A2 (k) + B2 (k) ⇄ 2AB (k). Có hệ số nhiệt độ g của phản ứng thuận và phản ứng nghịch lần lượt là 2 và 3. Hỏi khi tăng nhiệt độ cân bằng dịch chuyển theo chiều nào và từ đó suy ra dấu của DH° của phản ứng thuận.
Nghịch, DH° > 0
Thuận, DH° < 0>
Thuận, DH° > 0
Nghịch, DH° < 0>
Chọn đáp án đúng: Quá trình phân hủy phóng xạ Radi: \[_{{\rm{88}}}^{{\rm{226}}}{\rm{Ra}} \to _{{\rm{86}}}^{{\rm{222}}}{\rm{Ra + }}_{\rm{2}}^{\rm{4}}{\rm{He}}\]
được xem là phản ứng bậc nhất, đơn giản. Hãy xác định thời gian để 3g Radi giảm xuống còn 0,375g. Biết thời gian bán phân hủy của Radi là 1260 năm.
3780 năm
3915 năm
4012 năm
Đáp án khác
Chọn đáp án đúng: Đương lượng của HNO3 (Phân tử lượng M) bằng:
M/1
M/3
M/5
Tùy thuộc vào phản ứng
Cho phản ứng: Al2(SO4)3 + 4NaOH = 2Na2SO4 + [Al(OH)2]2SO4. Đương lượng gam của Al2(SO4)3 và NaOH lần lượt bằng: (Cho biết phân tử gam của Al2(SO4)3 bằng 342g và của NaOH bằng 40g)
342g; 40g
171g; 40g
85,5g; 40g
114g; 40g
Chọn đáp án đúng: Cho phản ứng: 2KAl(SO4)2.12H2O + 4NaOH = 2Na2SO4 + [Al(OH)2]2SO4 + K2SO4 + 24H2O. Đương lượng gam của KAl(SO4)2.24H2O và NaOH lần lượt bằng: (Cho biết phân tử gam của KAl(SO4)2.12H2O bằng 474g và của NaOH bằng 40g)
474g; 40g
237g; 40g
118,5g; 20g
237g; 40g
Chọn đáp án đúng: Cho phản ứng: MnO2 + 4HClđặc, nóng = MnCl2 + Cl2 + 2H2O. Đương lượng gam của MnO2 và HCl lần lượt bằng: (cho biết phân tử gam của MnO2 bằng 87g và của HCl bằng 36,5g)
43,5g; 36,5g
21,75g; 18,25g
87g; 35,5g
21,75g; 35,5g
Tính nồng độ mol của KMnO4 trong phản ứng với acid citric trong môi trường H+, biết \[{{\rm{C}}_{{\rm{NKMn}}{{\rm{O}}_{\rm{4}}}}} = 0.1{\rm{N}}\]. 2KMnO4 + 5H2C2O4 + 3H2SO4 = 2MnSO4 + 10CO2 + K2SO4 + 8H2O.
0,1M
0,02M
0,025M
Không xác định được
Chọn đáp án đúng: Tính thể tích dung dịch HCl 4M cần thiết để có thể pha thành 1 lít dung dịch HCl 0,5M.
0,0125 lit
0,125 lit
0,875 lit
12,5 lit
Chọn phát biểu đúng: (1) Chỉ tồn tại các dung dịch ở thể lỏng và thể khí. (2) Các dung dịch là những hệ phân tán và tất cả các hệ phân tán đều là dung dịch. (3) Dung dịch phân tử - ion là những dung dịch thực. (4) Dung dịch là những hệ phân tán mà trong đó các hạt phân tán có kích thước cỡ phân tử hay ion. (5) Không khí được xem là dung dịch.
1, 2, 4
1, 2, 5
3, 4, 5
Tất cả đều đúng
Chọn một phát biểu đúng trong các phát biểu dưới đây:
Tính chất các hệ phân tán phụ thuộc rất lớn vào kích thước hạt phân tán.
Kích thước các hạt phân tán trong hệ huyền phù nhỏ hơn rất nhiều so với kích thước các hạt phân tán trong hệ keo.
Hệ keo là hệ phân tán rất bền.
Trong thực tế chỉ tồn dung dịch rắn thay thế, không tồn tại dung dịch rắn xen kẽ.
Chọn phát biểu đúng: (1) Dung dịch là những hệ đồng thể gồm hai hay nhiều chất mà thành phần của chúng thay đổi trong giới hạn rộng. (2) Trong dung dịch dung môi là chất có lượng nhiều hơn và là môi trường phân tán. (3) Hằng số điện môi là đại lượng quan trọng trong việc lựa chọn dung môi, hằng số điện môi phụ thuộc vào độ có cực, cấu tạo và kích thước phân tử dung môi.
Chỉ 2, 3 đúng.
1, 2, 3 đều đúng.
Chỉ 1 đúng.
Không có phát biểu nào đúng.
Chọn phát biểu đúng về dung dịch rắn:
Dung dịch rắn thay thế và dung dịch rắn xen kẽ được xác định dựa vào cách bố trí các tiểu phân trong mạng tinh thể.
Dung dịch rắn xen kẽ và dung dịch rắn thay thế đều là các dung dịch rắn hạn chế.
Tất cả các chất đều tạo được dung dịch rắn với nhau khi chúng có kiểu mạng tinh thể gần nhau.
Trong thực tế, không tồn tại dung dịch rắn liên tục.
Chọn phát biểu đúng: (1) Nồng độ dung dịch đồng nhất trong toàn bộ dung dịch được giải thích bằng sự khuyếch tán các tiểu phân chất tan vào trong dung môi. (2) Bản chất của lực tương tác giữa các tiểu phân chất tan và dung môi là các tương tác vật lý. (3) Trong quá trình tạo thành dung dịch, các quá trình vật lý bao gồm sự phá vỡ mạng tinh thể, sự khuyếch tan chất tan vào dung môi được gọi chung là sự chuyển pha. (4) Sự tương tác giữa dung môi và các tiểu phân chất tan là yếu tố quan trọng hàng đầu quyết định sự tạo thành dung dịch.
1, 4 đúng
2, 3 đúng
1, 3, 4 đúng
Tất cả đều đúng
Chọn phát biểu đúng trong các ý sau:
Cân bằng hòa tan là một trạng thái cân bằng động, trạng thái cân bằng này là cố định trong mọi trường hợp.
Cân bằng hòa tan là cân bằng động và dung dịch ở trạng thái này được gọi là dung dịch bão hòa.
Cân bằng hòa tan được thiết lập cho bất kỳ lượng chất tan nào.
Khi đã đạt đến trạng thái cân bằng hòa tan, chất tan vẫn có thể tan thêm vào trong dung dịch.
