78 bài tập Khoa học tự nhiên 8 Chân trời sáng tạo Bài 6 có đáp án
78 câu hỏi
Khối lượng nước tạo thành khi đốt cháy hết 65 gam khí hydrogen là:
585 gam.
600 gam.
450 gam.
820 gam.
Cho 8,45g Zn tác dụng với 5,95 lít khí Cl2 (đkc). Hỏi chất nào sau phản ứng còn dư
Zn.
Cl2.
Cả 2 chất.
Không có chất dư.
Nhiệt phân 2,45g KClO3 thu được O2. Cho Zn tác dụng với O2 vừa thu được. Tính khối lượng chất thu được sau phản ứng?
2,45 g.
5,4 g.
4,86 g.
6,35 g.
Cho thanh Mg cháy trong không khí thu được hợp chất MgO. Biết mMg = 7,2 g. Tính khối lượng hợp chất tạo thành?
2,4 g.
9,6 g.
4,8 g.
12 g.
Trộn 10,8 gam bột nhôm với bột lưu huỳnh dư. Cho hỗn hợp vào ống nghiệm và đun nóng để phản ứng xảy ra thu được 25,5 gam Al2S3. Tính hiệu suất phản ứng ?
85%.
80%.
90%.
92%.
Cho luồng khí H2 đi qua ống thủy tinh chứa 20 gam bột CuO ở nhiệt độ cao. Sau phản ứng thu được 16,8 gam chất rắn. Hiệu suất của phản ứng là
Biết phương trình hóa học của phản ứng như sau: CuO + H2 Cu + H2O
70%.
75%.
80%
85%.
Người ta nung 4,9 gam KClO3 có xúc tác thu được 2,5 gam KCl và một lượng khí oxygen. Tính hiệu suất của phản ứng.
83,9%.
80%.
90%.
92%.
Một cơ sở sản xuất vôi tiến hành nung 4 tấn đá vôi (CaCO3) thì thu được 1,68 tấn vôi sống(CaO) và một lượng khí CO2. Tính hiệu suất của quá trình nung vôi.
70%.
75%.
80%.
85%.
Để điều chế được 8,775 gam muối Sodium chloride (NaCl) thì cần bao nhiêu gam Na? Biết hiệu suất phản ứng đạt 75%.
2,3 gam.
4,6 gam.
3,2 gam.
6,4 gam.
Cho phương trình:CaCO3 CaO + CO2
Số mol CaCO3 cần dùng để điều chế được 11,2 gam CaO là
0,2 mol.
0,3 mol.
0,4 mol.
0,1 mol.
Cho phản ứng hóa học sau: Al + H2SO4 Al2(SO4)3 + H2
Số mol H2SO4 phản ứng hết với 6 mol Al là
6 mol.
9 mol.
3 mol.
5 mol.
Cho phương trình sau: 2KClO3 2KCl + 3O2 Giả sử phản ứng hoàn toàn, từ 0,6 mol KClO3 sẽ thu được bao nhiêu mol khí oxygen?
0,9 mol.
0,45 mol.
0,2 mol.
0,4 mol.
Mg phản ứng với HCl theo phản ứng: Mg + 2HCl MgCl2 + H2 Sau phản ứng thu được 2,479 lít (đkc) khí hydrogen thì khối lượng của Mg đã tham gia phản ứng là
2,4 gam.
12 gam.
2,3 gam.
7,2 gam.
Cho 112 kg vôi sống (CaO) tác dụng với nước, biết rằng vôi sống có 10% tạp chất không tác dụng với nước. Khối lượng Ca(OH)2 thu được sau phản ứng là
131 kg.
133 kg.
133,2 kg.
143,2 kg.
Người ta điều chế vôi sống bằng cách nung đá vôi. Lượng vôi sống thu được từ 1 tấn đá vôi có chứa 10% tạp chất là
0,252 tấn.
0,378 tấn.
0,504 tấn.
0,606 tấn.
Đốt cháy hoàn toàn 7,5 gam than đá có chứa 4% tạp chất không cháy. Thể tích khí oxygen cần dùng (đktc) để đốt cháy hết lượng than đá trên là
14,33 lít.
13,44 lít.
14,478 lít.
14,874 lít.
Đốt cháy 12,395 lít CH4 (đkc) trong không khí, thu được khí X và nước. Khí và cho biết số mol của X là
CO và 0,5 mol.
CO2 và 0,5 mol.
C và 0,2 mol.
CO2 và 0,054 mol.
Cho cùng một khối lượng các kim loại là Mg, Al, Zn, Fe lần lượt vào dung dịch H2SO4 loãng, dư thì thể tích khí H2 lớn nhất thoát ra là của kim loại nào sau đây?
Mg.
Al.
Zn.
Fe.
Có một hỗn hợp chứa 2,3 gam sodium và 1,95 gam potassium tác dụng với nước. Thể tích khí hydrogen thu được (đkc) là
1,68 lít.
1,7 lít.
1,6 lít.
2,68 lít.
Trộn 4 gam bột sulfur với 14 gam bột iron rồi đun nóng. Khối lượng FeS thu được là
18 gam.
11 gam.
16 gam.
13 gam.
Nhiệt phân 2,45 gam KClO3 thu được O2. Cho Zn tác dụng với O2 vừa thu được. Tính khối lượng chất thu được sau phản ứng
2,45 gam.
5,4 gam.
4,86 gam.
6,35 gam.
Nung nóng m gam hỗn hợp chứa Fe2O3 và CuO trong bình kín với khí hydrogen để khử hoàn toàn lượng oxide trên, thu được 13,4 gam hỗn hợp Fe và Cu, trong đó số mol của sắt là 0,125 mol. Giá trị m và thể tích khí H2 (đkc) tham gia là
18; 7,9.
18; 8,9.
18; 2,24.
18, 5,6.
Khi cho luồng khí CO (dư) đi qua ống sứ có chứa 5,36 gam hỗn hợp FeO và Fe2O3 nung nóng thì thu được m gam chất rắn và hỗn hợp khí X. Cho X lội vào dung dịch Ca(OH)2 dư thấy có 9 gam kết tủa. Giá trị m là
9,32.
2,39.
9,23.
3,92.
Cho dòng khí CO dư qua hỗn hợp 2 oxide CuO và Fe3O4 nung nóng thu được 29,6 gam hỗn hợp 2 kim loại trong đó sắt nhiều hơn đồng 4 gam. Thể tích khí CO cần dùng (đkc) là
14,874 lít.
20,16 lít.
17,92 lít.
13,44 lít.
Cho 12,8 gam một kim loại R hóa trị II tác dụng với khí chlorine (Cl2) vừa đủ, thu được 27 gam muối chloride (RCl2). R là kim loại
Fe.
Ca.
Cu.
Mg.
Cho 3,6 gam một FexOy vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được 6,35 gam một muối iron(II) chloride. Công thức phân tử FexOy là
Fe2O3.
Fe3O4.
FeO.
Fe2O.
Cho 4,8 gam kim loại X (có hóa trị II) tác dụng hết với dung dịch hydrochloric acid. Sau phản ứng thu được dung dịch Y chứa 19 gam muối. Kim loại X là
Ca.
Ba.
Mg.
Zn.
Cho 3,2 gam một FexOy vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được 6,5 gam một muối iron(III) chloride. Công thức phân tử oxit sắt là
Fe2O3.
Fe3O4.
FeO.
Fe2O.
Người ta dùng 490 kg than để đốt lò chạy máy. Sau khi lò nguội, thấy còn 49 kg than chưa cháy. Hiệu suất của sự cháy trên là
95%.
75%.
90%.
80%.
Cho 19,5 gam Zn tác dụng với khí Cl2 dư, thu được 36,72 gam ZnCl2. Hiệu suất phản ứng là
95%.
75%.
90%.
80%.
Nung 1 kg đá vôi chứa 80% CaCO3, thu được 123,95 lít CO2 (đkc). Hiệu suất phân huỷ CaCO3 là
80%.
62,5%.
50%.
75,5%.
Người ta điều chế vôi sống (CaO) bằng cách nung đá vôi (CaCO3). Lượng vôi sống thu được từ 1 tấn đá vôi có chứa 10% tạp chất là 0,45 tấn. Hiệu suất của phản ứng điều chế vôi sống là
90%.
73,62%.
89,29%.
81,65%.
Từ 320 tấn quặng pyrite sắt có chứa 45% lưu huỳnh đã sản xuất được 506,25 tấn dung dịch H2SO4 80%. Hiệu suất của quá trình là
91,84%.
75%.
90%.
80,36%.
Khi cho khí SO3 hợp nước, thu được dung dịch H2SO4. Biết hiệu suất phản ứng là 95%. Khối lượng H2SO4 điều chế được khi cho 40 kg SO3 hợp nước là
44,1 kg.
41,65%.
36,75%.
46,55 kg.
Người ta điều chế vôi sống (CaO) bằng cách nung đá vôi CaCO3 với hiệu suất 85%. Lượng vôi sống thu được từ 1 tấn đá vôi có chứa 10% tạp chất là
0,4284 tấn.
0,478 tấn.
0,504 tấn.
0,4536 tấn.
Có thể điều chế bao nhiêu kg nhôm từ 1 tấn quặng bauxite có chứa 95% aluminium oxide (Al2O3), biết hiệu suất phản ứng là 98%?
0,493 tấn.
0,501 tấn.
0,453 tấn.
0,475 tấn.
Nung 500 gam đá vôi chứa 80% CaCO3, sau một thời gian thu được rắn X và khí Y. Biết hiệu suất phản ứng phân huỷ đá vôi là 57%. Khối lượng chất rắn X và thể tích khí Y (đkc) là
133,4 gam và 53,76 lít.
156,8 gam và 62,72 lít.
224 gam 89,6 lít.
127,68 gam và 56,5212 lít.
Đốt cháy 6,0 gam hỗn hợp Y gồm các kim loại Al, Fe, Zn trong khí oxygen, sau một thời gian thu được 8,08 gam chất rắn Z gồm các oxide kim loại và kim loại còn dư. Thể tích khí oxygen đã phản ứng (đkc) là
1,4874.
1,61135.
1,568.
1,792.
Trong phản ứng hóa học, chất phản ứng hết là chất
còn lại sau khi phản ứng kết thúc.
còn lại một nửa sau khi phản ứng kết thúc.
không còn sau khi phản ứng kết thúc.
tạo thành sau phản ứng.
Phản ứng không hoàn toàn là phản ứng có
các chất phản ứng đều còn sau phản ứng kết thúc.
các chất phản ứng đều hết sau phản ứng kết thúc.
ít nhất một chất tham gia phản ứng đết sau phản ứng kết thúc.
các chất sản phẩm đều là chất khí.
Phản ứng vừa đủ là phản ứng có
các chất phản ứng đều còn sau phản ứng kết thúc.
các chất phản ứng đều hết sau phản ứng kết thúc.
ít nhất một chất tham gia phản ứng đết sau phản ứng kết thúc.
các chất sản phẩm đều là chất khí.
Cho phản ứng hóa học sau: Al + H2SO4 Al2(SO4)3 + H2. Số mol H2SO4 phản ứng hết với 6 mol Al là
A. 6 mol.B. 9 mol.C. 3 mol.D. 5 mol.
6 mol.
9 mol.
3 mol.
5 mol.
Fe phản ứng với HCl theo phản ứng: Fe + HCl FeCl2 + H2.Hòa tan hoàn toàn 8,4 gam Fe vào dung dịch HCl dư, thu được dung dịch X và khí Y. Cô cạn dung dịch X thu được m gam muối khan (FeCl2). Giá trị của m là
24,375.
19,05.
12,70.
16,25.
Ba tác dụng với H2O theo phản ứng : Ba + H2O Ba(OH)2 + H2.Cho 13,7 gam Ba tác dụng với nước dư, sau phản ứng thu được V lít H2 (ở đkc). Giá trị của V là
1,2395 lít.
2,479 lít.
1,792 lít.
3,7185 lít.
Để tác dụng vừa đủ với 0,5 gam khí hydrogen thì cần dùng thể tích O2 (đkc) là
1,2395 lít.
3,09875 lít.
7,437 lít.
6,1975 lít.
Phản ứng hoàn toàn có
H = 100%
H = 90%.
H = 0%.
H = 50%.
Phản ứng không hoàn toàn có
H = 100%.
H < 100%.
H = 0%.
H < 50%.
Cho 9,916 lít N2 (đkc) tác dụng với 22,311 lít H2 (đkc), thu được 3,4 gam NH3. Hiệu suất của phản ứng là
20%.
34%.
33,3%.
50%.
Nung 316 gam KMnO4 sau một thời gian thấy còn lại 300 gam chất rắn. Hiệu suất phản ứng nhiệt phân là
25%.
30%.
40%.
50%.
Cho 30 lít khí nitrogen tác dụng với 30 lít H2 trong điều kiện thích hợp và tạo ra một thể tích NH3 là (các thể tích đo ở cùng điều kiện và hiệu suất phản ứng đạt 30%)
6 lít.
18 lít.
20 lít.
60 lít.
Đốt cháy 3,2g sulfur (lưu huỳnh) trong một bình chứa 1,2395 lít khí O2 (đkc). Thể tích khí SO2 thu được là:
4,958 lít.
2,479 lít.
1,2395 lít.
3,7185 lít.
Cho 13 gam kẽm (zinc) vào dung dịch chứa 16,425 gam HCl đến khi phản ứng hoàn toàn thu được zinc chloride (ZnCl2) và V lít khí H2 (đkc). Giá trị của V là
4,958.
3,7185.
5,57775.
11,1555.
Hiệu suất phản ứng là
là tổng giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lí thuyết.
là hiệu giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lí thuyết.
là tích giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lí thuyết.
là tỉ số giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lí thuyết.
Hiệu suất phản ứng có kí hiệu là
M.
H.
N.
S.
Để điều chế ra 2 lít NH3 từ N2 và H2 với hiệu suất 25% thì cần thể tích N2 ở cùng điều kiện là:
8 lít.
4 lít.
2 lít.
1 lít.
Đốt cháy 3,1 gam phosphorus trong lọ chứa 2,479 lít khí O2 (đkc) đến khi phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là
5,68.
7,10.
6,30.
4,97.
Phản ứng hoàn toàn là phản ứng có
các chất phản ứng đều còn sau phản ứng kết thúc.
các chất phản ứng đều hết sau phản ứng kết thúc
ít nhất một chất tham gia phản ứng đết sau phản ứng kết thúc.
các chất sản phẩm đều là chất khí.
Trong phản ứng hóa học, chất phản ứng dư là chất
còn lại sau khi phản ứng kết thúc.
không còn khi phản ứng xảy ra được một thời gian.
không còn sau khi phản ứng kết thúc.
tạo thành sau phản ứng.
Mg phản ứng với HCl theo phản ứng: Mg + HCl MgCl2 + H2. Sau phản ứng thu được 2,479 lít (đkc) khí hydrogen thì khối lượng của Mg đã tham gia phản ứng là
2,4 gam.
12 gam.
2,3 gam.
7,2 gam.
Zn phản ứng với H2SO4 loãng theo phản ứng: Zn + H2SO4 ZnSO4 + H2. Hòa tan hoàn toàn 6,5 gam Zn bằng dung dịch H2SO4 loãng, thu được V lít H2 (đkc). Giá trị của V là
2,479.
1,2395.
4,958.
3,7185.
Đốt cháy hết 0,54 gam Al trong không khí thu được aluminium oxide theo sơ đồ phản ứng: Al + O2 Al2O3. Lập phương trình hóa học của phản ứng rồi tính:
a) Khối lượng aluminium oxide tạo ra.
b) Thể tích khí oxygen tham gia phản ứng ở điều kiện chuẩn.
Hòa tan hoàn toàn 2,8 gam Fe trong dung dịch hydrochloric acid (HCl) dư, thu được muối iron (II) chloride (FeCl2) và khí hydrogen.
a) Viết phương trình hóa học xảy ra.
b) Tính khối lượng muối iron (II) chloride thu được.
c) Tính thể tích khí hydrogen thu được ở điều kiện chuẩn.
Có phương trình hóa học sau: CaCO3 CaO + CO2
a) Cần dùng bao nhiêu mol CaCO3 để điều chế được 11,2 g CaO?
b) Muốn điều chế được 7 gam CaO cần dùng bao nhiêu gam CaCO3?
c) Nếu có 3,5 mol CaCO3 tham gia phản ứng sẽ sinh ra bao nhiêu lít CO2 (đkc)?
Khi cho Mg tác dụng với dung dịch H2SO4 loãng thì xảy ra phản ứng hóa học như sau: Mg + H2SO4 MgSO4 + H2 . Sau phản ứng thu được 0,02 mol MgSO4. Tính thể tích khí H2 thu được ở 25 oC, 1 bar.
Đốt cháy hoàn toàn 6,2 gam phosphorus trong khí oxygen. Hãy tính thể tích khí oxygen (đkc) và khối lượng sản phẩm tạo thành theo phản ứng: 4P + 5O2 2P2O
Xét phản ứng xảy ra hoàn toàn: H2 + Cl2 2HCl. Tiến hành 3 thí nghiệm với các tỉ lệ mol khác nhau của khí hydrogen và khí chlorine, kết quả thu được như sau: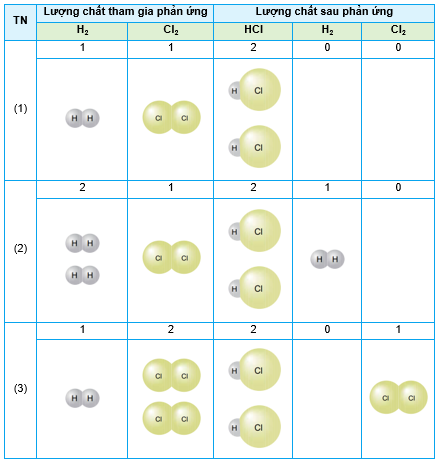
a) Các chất sau phản ứng trong các thí nghiệm (1), (2) và (3) gồm những chất nào?
b) Trong thí nghiệm (2) và (3), chất nào là chất hết và chất nào là chất dư?
c) Phản ứng nào xảy ra vừa đủ trong các thí nghiệm (1), (2), (3)?
d) Sản phẩm tạo thành trong 3 thí nghiệm là chất nào? Để xác định lượng sản phẩm tạo thành cần dựa vào lượng chất hết hay chất dư?
Cho 5,4 gam nhôm (aluminium) tác dụng với 14,6 gam hydrochloric acid, sau phản ứng thu được muối aluminium chloride (AlCl3) và khí H2.
a) Viết phương trình hóa học xảy ra.
b) Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
c) Sau phản ứng thu được bao nhiêu lít khí H2 (ở đkc).
Đốt cháy 1 mol khí hydrogen trong 0,4 mol khí oxygen đến khi phản ứng xảy ra hoàn toàn. Cho biết chất nào còn dư sau phản ứng.
Đốt cháy 4,65 gam phosphorus trong bình chứa 3,7185 lít oxygen (đkc), sản phẩm tạo thành là diphosphorus pentoxide (P2O5).
a) Viết phương trình hóa học của phản ứng xảy ra.
b) Sau phản ứng chất nào còn dư và dư bao nhiêu gam?
c) Tính khối lượng của chất rắn thu được sau phản ứng.
Dẫn 2,479 lít khí H2 (ở đkc) vào một ống có chứa 12 gam copper (II) oxide (CuO) đã nung nóng tới nhiệt độ thích hợp, sau phản ứng thu được a gam chất rắn và hơi nước.
a) Viết phương trình hóa học xảy ra.
b) Tính khối lượng nước tạo thành sau phản ứng.
c) Tính a.
Khi nung nóng KClO3 xảy ra phản ứng hóa học sau (phản ứng nhiệt phân):
2KClO3 2KCl + 3O2
Biết rằng hiệu suất phản ứng nhỏ hơn 100%. Hãy chọn các cụm từ (lớn hơn, nhỏ hơn, bằng) phù hợp với nội dung còn thiếu trong các câu sau đây:
- Khi nhiệt phân 1 mol KClO3 thì thu được số mol O2 (1) …………. 1,5 mol
- Để thu được 0,3 mol O2 thì cần số mol KClO3 (2) ………………… 0,2 mol.
Trong công nghiệp, aluminium (Al) được sản xuất từ aluminium oxide (Al2O3) theo phương trình hóa học sau: 2Al2O3 4Al + 3O2↑
a) Tính hiệu suất phản ứng khi điện phân 102 kg Al2O3, biết khối lượng aluminium thu được sau phản ứng là 51,3 kg.
b) Biết khối lượng aluminium thu được sau điện phân là 54 kg và hiệu suất phản ứng là 92%, tính khối lượng Al2O3 đã dùng.
Nung 10 gam calcium carbonate (thành phần chính của đá vôi), thu được khí carbon dioxide và m gam vôi sống. Giả thiết hiệu suất phản ứng là 80%, xác định m.
Cho 0,5 mol khí hydrogen tác dụng với 0,45 mol hơi iodine thu được 0,6 mol khí hydrogen iodide (HI). Tính hiệu suất phản ứng.
Ammonia (NH3) được tổng hợp từ nitrogen và hydrogen theo phản ứng:
N2 + H2 NH3.
Cho vào bình kín 0,2 mol N2 và 0,8 mol H2 với xúc tác thích hợp, sau một thời gian thu được 0,12 mol NH3. Tính hiệu suất của phản ứng tổng hợp NH3 ở trên.
Khi nung nóng potassium pemanganate (thuốc tím) KMnO4 xảy ra phản ứng hóa học sau (phản ứng nhiệt phân): KMnO4 K2MnO4 + MnO2 + O2
Biết rằng khi nung 39,5 gam KMnO4 sau một thời gian thì thu được 2,479 lít khí oxygen (đkc). Tính hiệu suất phản ứng.
Nung nóng 50 g KClO3 một thời gian thấy khối lượng hỗn hợp chất rắn còn lại là 38 gam.
a) Tính hiệu suất của phản ứng nhiệt phân.
b) Hãy tính khối lượng mỗi chất trong hỗn hợp rắn sau phản ứng.
Ammonia (NH3) được tổng hợp từ nitrogen và hydrogen theo phản ứng:
N2 + H2 NH3.Cho 2,479 lít N2 tác dụng với lượng dư H2, sau một thời gian thu được 1,2395 lít khí NH3 (các thể tích khí đều đo ở đkc). Tính hiệu suất của phản ứng tổng hợp NH3 ở trên.
