28 câu trắc nghiệm Hóa 12 Kết nối tri thức Bài 25: Nguyên tố nhóm IIA (Đúng sai - Trả lời ngắn) có đáp án
28 câu hỏi
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Mỗi câu hỏi học sinh chỉ chọn một phương án.
Nước cứng không gây tác hại nào sau đây?
Làm giảm khả năng tẩy rửa của xà phòng, làm cho quần áo mau mục nát.
Gây lãng phí nhiên liệu và mất an toàn cho các nồi hơi, làm tắc các đường ống nước nóng.
Gây ngộ độc cho nước uống.
Làm hỏng dung dịch pha chế, làm thực phẩm lâu chín và giảm mùi vị của thực phẩm.
Số electron lớp ngoài cùng của các nguyên tử kim loại thuộc nhóm IIA là
3.
2.
4.
1.
Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của các kim loại nhóm IIA có dạng chung là
A. ns1.
ns2.
ns2np3.
ns2np5.
Trong nhóm IIA, nguyên tố phổ biến trong vỏ Trái Đất là
Rb và Sr.
Mg và Ba.
Mg và Ca.
Be và Ca.
Kim loại không phản ứng với nước là
Mg.
Ba.
Be.
Ca.
Khi đun nóng nước tự nhiên, muối nào sau đây bị phân huỷ tạo thành cặn đá vôi trong phích nước, ấm đun nước?
C. CaSO4.
Ca3(PO4)2.
CaCl2.
Ca(HCO3)2.
Trong chế độ dinh dưỡng hàng ngày, khi cơ thể không hấp thu được hoặc thiếu nguyên tố nào dưới đây sẽ dẫn đến nguy cơ loãng xương?
Ba.
Mg.
Be.
Ca.
Ở nơi tồn ứ rác thải, chất nào sau đây được các công nhân vệ sinh môi trường dùng để xử lí tạm thời nhằm sát trùng, diệt khuẩn, phòng chống dịch bệnh?
Cát vàng.
Than đá.
Đá vôi.
Vôi bột.
Cho sơ đồ chuyển hoá sau:
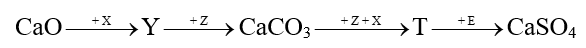
Biết: X, Y, Z, T, E là các hợp chất khác nhau; mỗi mũi tên ứng với một phương trình hoá học. Các chất Z, E thoả mãn sơ đồ trên lần lượt là
Na2CO3, H2SO4.
CO2, KHSO4.
NaHCO3, Na2SO4.
CO2, BaSO4.
Khi đun nóng đến 60 °C, thạch cao sống mất một phần nước trở thành thạch cao nung, được dùng để đúc khuôn trong điêu khắc, bó bột trong y học. Thành phần chính của thạch cao nung là
CaSO4.0,5H2O.
Ca(H2PO4)2.
CaCO3.
Ca(OH)2.
Trong các mẫu nước cứng sau đây, nước cứng tạm thời là
dung dịch Ca(HCO3)2.
dung dịch MgSO4.
dung dịch CaCl2.
dung dịch Mg(NO3)2 .
Trong tự nhiên, magnesium có nhiều ở khoáng vật nào sau đây?
Dolomite.
Calcite.
Phosphorite.
Halite.
Trong đời sống, người ta dùng sữa vôi để quét lên tường, tạo lớp rắn, mịn, màu trắng trên bức tường. Hiện tượng này được giải thích bằng phản ứng nào dưới đây?
\({\rm{Ca}}{({\rm{OH}})_2} + {\rm{C}}{{\rm{O}}_2} \to {\rm{CaC}}{{\rm{O}}_3} + {{\rm{H}}_2}{\rm{O}}.\)
\({\rm{CaO}} + {\rm{C}}{{\rm{O}}_2} \to {\rm{CaC}}{{\rm{O}}_3}.\)
\({\rm{Ca}}{({\rm{OH}})_2} + 2{\rm{C}}{{\rm{O}}_2} \to {\rm{Ca}}{\left( {{\rm{HC}}{{\rm{O}}_3}} \right)_2}.\)
\({\rm{CaO}} + {{\rm{H}}_2}{\rm{O}} \to {\rm{Ca}}{({\rm{OH}})_2}.\)
Có thể nhận biết dung dịch BaCl2 bằng dung dịch chất nào sau đây?
NaOH.
Na2CO3.
NaCl.
NaNO3.
Muối nào sau đây chỉ tồn tại trong dung dịch và bị phân huỷ khi đun nóng?
Ca(NO3)2.
Ca(HCO3)2.
CaCl2.
CaSO4.
Bình thuỷ dùng để đun nước lâu ngày bị đóng cặn, có thể dùng dung dịch nào sau đây để hoà tan lớp cặn?
Nước vôi.
Rượu uống.
Giấm ăn.
Muối ăn.
Trong tự nhiên, calcium sulfate tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
vôi sống.
vôi tôi.
thạch cao sống.
đá vôi.
Độ tan trong dãy muối sulfate từ MgSO4 đến BaSO4 biến đổi như thế nào?
Tăng dần.
Giảm dần.
Không có quy luật.
Không đổi.
PHẦN II. Câu trắc nghiệm đúng sai. Trong mỗi ý a), b), c), d) ở mỗi câu, học sinh chọn đúng hoặc sai.
Magnesium \(({\rm{Mg}})\) là kim loại được ứng dụng để tạo các hợp kim nhẹ, bền, đặc biệt là cho ngành công nghiệp sản xuất ô tô và hàng không vũ trụ. Magnesium được sản xuất trong công nghiệp theo quá trình Pidgeon với nguyên liệu ban đầu là quặng dolomite. Quá trình được thực hiện qua các giai đoạn sau:

a) Quá trình Pidgeon là quá trình thu nhiệt.
b) Phản ứng ở giai đoạn (2) thuộc phương pháp nhiệt luyện.
c) Phản ứng ở giai đoạn (2) chứng tỏ MgO có tính oxi hoá mạnh hơn CaO.
d) Nếu hiệu suất của quá trình là 90% thì cứ 1 tấn quặng dolomite sẽ điều chế được 120 kg kim loại magnesium.
Giá trị biến thiên enthalpy chuẩn của phản ứng nhiệt phân muối nitrate của kim loại nhóm IIA (R) (R(NO3)2(s) RO(s) + 2NO2(g) + \(\frac{1}{2}\)O2(g)) theo bảng sau:
Muối R(NO3)2(s) | Mg(NO3)2 | Ca(NO3)2 | Sr(NO3)2 | Ba(NO3)2 |
\({\Delta _r}H_{298}^o(kJ)\) | 255,2 | 369,5 | 452,4 | 506,2 |
a) Độ bền nhiệt của các muối nitrate của kim loại nhóm IIA có xu hướng tăng dần từ \[Mg{\left( {N{O_3}} \right)_2}\]tới\[Ba{\left( {N{O_3}} \right)_2}.\]
b) Dựa vào bảng giá trị biến thiên enthalpy chuẩn ở trên có thể dự đoán xu hướng biến đổi độ bền nhiệt của\[R{\left( {N{O_3}} \right)_2}.\]
c) Phản ứng nhiệt phân muối nitrate của kim loại nhóm IIA \[\left( {R{{\left( {N{O_3}} \right)}_2}} \right)\] là phản ứng oxi hoá – khử, trong đó vai trò chất oxi hoá là\[{R^{2 + }}.\;\]
d) Nhiệt độ phân huỷ theo thứ tự sau: \[Mg{\left( {N{O_3}} \right)_2} < {\rm{ }}Ca{\left( {N{O_3}} \right)_2} < {\rm{ }}Sr{\left( {N{O_3}} \right)_2} < {\rm{ }}Ba{\left( {N{O_3}} \right)_2}.\;\]
Một loại nước cứng có thành phần ion như sau:
Ion | Nồng độ (M) |
Calcium (Ca2+) | 0,02 |
Sodium (Na+) | 0,03 |
Hydrogen carbonate (\(HCO_3^ - \)) | x |
a) Nước cứng đã nêu có tính cứng vĩnh cửu.
b) Giá trị của x là 0,05.
c) Có làm mềm mẫu nước cứng trên bằng cách đun nóng.
d) Để làm mềm 1 lít nước cứng trên, cần dùng ít nhất 40 mL dung dịch NaOH 0,5 M.
Xét các phản ứng phân hủy sau:
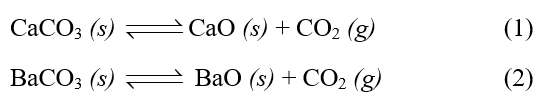
Biến thiên enthalpy chuẩn (\({{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{{\rm{298}}}^{\rm{0}}\)) của phản ứng thuận ở mỗi cân bằng (1) và (2) khi phân hủy 1 mol mỗi chất lần lượt có giá trị là 108,7 kJ và 271,5 kJ.
a) Nhiệt lượng tỏa ra khi phân hủy 1 mol BaCO3 lớn hơn nhiệt lượng tỏa ra khi phân hủy 1 mol CaCO3.
b) BaCO3 bị phân hủy ở nhiệt độ cao hơn CaCO3.
c) Khi tăng nhiệt độ, cả hai phản ứng đều dịch chuyển theo chiều thuận.
d) CO2 cần được lấy ra khỏi lò nung để tăng hiệu suất của phản ứng.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn
Ion Ca2+ cần thiết cho máu của người hoạt động bình thường. Nồng độ ion calcium không bình thường là dấu hiệu của bệnh. Để xác định nồng độ ion calcium, người ta lấy mẫu máu, sau đó kết tủa ion calcium dưới dạng calcium oxalate (CaC2O4) rồi cho calcium oxalate tác dụng với dung dịch potassium permanganate trong môi trường acid theo phản ứng sau:
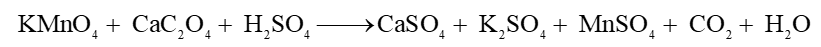
Giả sử calcium oxalate kết tủa từ 1 mL máu một người tác dụng vừa hết với 2 mL dung dịch potassium permanganate \[\left( {KMn{O_4}} \right){\rm{ }}{5.10^{ - 4}}M.\] Xác định nồng độ ion calcium trong máu người đó bằng đơn vị \[mg{\rm{ }}C{a^{2 + }}/100{\rm{ }}mL\]máu.
Để đánh giá mức độ tự diễn biến của một phản ứng tại nhiệt độ T, người ta dựa vào đại lượng biến thiên năng lượng tự do Gibbs \[({\Delta _r}G_T^o).\] Nếu \[{\Delta _r}G_T^o > 0\]: phản ứng không tự xảy ra; \[{\Delta _r}G_T^o < 0\]: phản ứng tự xảy ra.
Giá trị của đại lượng này được tính theo biểu thức:
\[{\Delta _r}G_T^o = {\rm{ }}{\Delta _r}H_T^o - {\rm{ }}T{\Delta _r}S_T^o.\] Trong đó
- T: nhiệt độ tính theo thang Kelvin (K);
- \[{\Delta _r}H_T^o\]: Biến thiên enthalpy của phản ứng;
- \[{\Delta _r}S_T^o\]: Biến thiên entropy của phản ứng (đại lượng đặc trưng cho độ mất trật tự của hệ ở một trạng thái và điều kiện xác định).
Tính giá trị thấp nhất của T (làm tròn đến hàng đơn vị) để phản ứng sau tự xảy ra:
CaCO₃(s) → CaO(s) + CO₂(g)
Cho biết: \[{\Delta _r}S_T^o = 159,26{\rm{ }}J/mo{l^{ - 1}}.{K^{ - 1}}\]và nhiệt tạo thành chuẩn của các chất như sau:
Chất | CaCO₃(s) | CaO(s) | CO₂(g) |
\[{\Delta _f}H_{298}^o(kJ.mo{l^{ - 1}})\] | -1207,0 | -635,0 | -393,5 |
Giả sử \[{\Delta _r}H_T^o\] và \[{\Delta _r}S_T^o\] của quá trình không phụ thuộc vào nhiệt độ.
Ở điều kiện thường, tinh thể Ca có D = 1,55 g/cm3. Giả thiết các nguyên tử Ca là những hình cầu chiếm 74% thể tích tinh thể, phần còn lại là khe rỗng.
Cho biết:
- Công thức tính thể tích hình cầu: V = \[\frac{4}{3}\].π.r3
- Số Avogadro NA= 6,023.1023 và số pi π = 3,1416.
Bán kính nguyên tử Ca là bao nhiêu pm? (Làm tròn kết quả đến hàng đơn vị).
Làm mềm \(10\;{{\rm{m}}^3}\) nước cứng có tổng nồng độ \({\rm{M}}{{\rm{g}}^{2 + }}\) và \({\rm{C}}{{\rm{a}}^{2 + }}\) là \(5,5{\rm{mmol}}/{\rm{L}}\) bằng \({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\), thu được nước có tổng nồng độ \({\rm{M}}{{\rm{g}}^{2 + }}\) và \({\rm{C}}{{\rm{a}}^{2 + }}\) là \(1,5{\rm{mmol}}/{\rm{L}}\). Coi toàn bộ lượng \({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\) cho vào đều chuyển hết thành kết tủa \({\rm{CaC}}{{\rm{O}}_3}\) và \({\rm{MgC}}{{\rm{O}}_3}\). Khối lượng \({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\) đã dùng là bao nhiêu kg? (Làm tròn kết quả đến hàng phần trăm)
Vôi sống có nhiều ứng dụng như: sản xuất vật liệu xây dựng, vật liệu chịu nhiệt, khử chua đất trồng, tẩy uế, sát trùng, xử lí nước thải,... Hiện nay, nhiều lò nung vôi thủ công hoạt động tự phát, gây ảnh hưởng xấu đến môi trường xung quanh. Ở các lò nung vôi công nghiệp, quá trình kiểm soát phát thải ô nhiễm được thực hiện chặt chẽ hơn.
Xét một lò nung vôi công nghiệp sử dụng than đá làm nhiên liệu.
Giả thiết:
+ Đá vôi chỉ chứa CaCO3 và để phân hủy 1 kg đá vôi cần cung cấp một lượng nhiệt là 1800 kJ.
+ Đốt cháy 1 kg than đá giải phóng ra một lượng nhiệt là 27000 kJ và có 50% lượng nhiệt này được hấp thụ ở quá trình phân hủy đá vôi.
+ Công suất của lò nung vôi là 420 tấn vôi sống/ngày.
Tổng khối lượng (tấn) đá vôi và than đá mà lò nung vôi trên sử dụng mỗi ngày là bao nhiêu?
Nhiệt phân hoàn toàn 40 g một loại quặng dolomite có lẫn tạp chất trơ sinh ra 9,916 lít khí CO2 (điều kiện chuẩn). Thành phần phần trăm về khối lượng của CaCO3.MgCO3 trong loại quặng nêu trên là bao nhiêu?

