28 câu trắc nghiệm Hóa 12 Cánh diều Bài 12: Điện phân (Đúng sai - Trả lời ngắn) có đáp án
28 câu hỏi
Khi điện phân dung dịch NaCl có màng ngăn, các chất được tạo ra ở anode (cực dương) và cathode (cực âm) lần lượt là
Cl2 và NaOH, H2.
Na và Cl2.
Cl2 và Na.
NaOH và H2.
Khi điện phân dung dịch gồm NaCl 1,0 M và CuSO4 0,5 M, thứ tự điện phân ở anode là
H2O, Cl–.
Cl–, H2O.
\[{\rm{SO}}_4^{2 - }\], Cl–, H2O.
Cl–, \[{\rm{SO}}_4^{2 - }\], H2O.
Quá trình xảy ra đầu tiên tại cực âm khi điện phân dung dịch gồm NaCl và CuCl2 là
khử ion Cl–.
oxi hóa ion Cl–.
khử ion Cu2+.
khử H2O.
Trong quá trình điện phân KCl nóng chảy với các điện cực trơ, ở cathode xảy ra quá trình
oxi hóa ion K+.
khử ion K+.
oxi hóa ion Cl–.
khử ion Cl–.
Phản ứng hóa học chính xảy ra trong quá trình điện phân nóng chảy Al2O3 trong 3NaF.AlF3 là
2AlF3 → 2Al + 3F2.
2NaF → Na + F2.
2H2O → 2H2 + O.
2Al2O3 → 4Al + 3O2.
Phương trình hóa học nào sau đây biểu diễn quá trình điều chế kim loại bằng phương pháp điện nóng chảy?
2Al2O3 → 4Al + 3O2.
2Al + Cr2O3 → Al2O3 + 2Cr.
Zn + CuSO4 → ZnSO4 + Cu.
2NaCl + 2H2O → 2NaOH + Cl2 + H2.
Khi điện phân dung dịch gồm Cu(NO3)2 0,1 M và AgNO3 0,1 M, quá trình oxi hóa xảy ra ở anode là
2H2O → 4H++ O2 + 4e.
2H2O + 2e → H2 + 2OH–.
Cu2+ + 2e → Cu.
Ag+ + 1e → Ag.
Dung dịch X chứa hỗn hợp các muối: MgCl2, CuCl2, FeCl2 và KCl. Kim loại tách ra đầu tiên ở cathode khi điện phân dung dịch là
Cu..
Mg.
K.
Fe.
Sodium được sản xuất trong công nghiệp bằng phương pháp nào?
Phương pháp thủy luyện.
Phương pháp nhiệt luyện.
Phương pháp điện phân.
Phương pháp điện phân nóng chảy.
Khi điện phân dung dịch gồm Zn(NO3)2 1 M và AgNO3 1 M, thứ tự điện phân ở cathode là
Zn2+, Ag+, H2O.
Ag+, Zn2+, H2O.
H2O, Zn2+, Ag+.
Zn2+, H2O, Ag+.
Ion halide hầu như không bị điện phân trong dung dịch là
\[{\rm{B}}{{\rm{r}}^{\rm{ - }}}\].
\[{{\rm{I}}^{\rm{ - }}}\].
\[{{\rm{F}}^{\rm{ - }}}\].
\[{\rm{C}}{{\rm{l}}^{\rm{ - }}}\].
Trong công nghiệp, quá trình điện phân dung dịch NaCl bão hòa (điện cực trơ, có màng ngăn xốp) tạo ra khí nào sau đây ở cathode?
Hydrogen.
Chlorine.
Oxygen.
Hydrogen chloride.
Khi điện phân dung dịch gồm NaCl 1 M và NaBr 1 M, quá trình oxi hóa đầu tiên xảy ra ở anode là
2H2O → 4\[{{\rm{H}}^{\rm{ + }}}\]+ O2 + 4e.
2\[{\rm{C}}{{\rm{l}}^{\rm{ - }}}\]→ Cl2 + 2e.
2\[{\rm{B}}{{\rm{r}}^{\rm{ - }}}\]→ Br2 + 2e.
Na → \[{\rm{N}}{{\rm{a}}^{\rm{ + }}}\] + 1e.
Trong quá trình điện phân dung dịch CuSO4 với anode bằng graphite, ở anode xảy ra quá trình
2H2O → 4\[{{\rm{H}}^{\rm{ + }}}\]+ O2 + 4e.
2H2O → 4\[{{\rm{H}}^{\rm{ + }}}\]+ O2 + 4e.
\[{\rm{C}}{{\rm{u}}^{{\rm{2 + }}}}\]+ 2e → Cu.
Cu → \[{\rm{C}}{{\rm{u}}^{{\rm{2 + }}}}\]+ 2e.
Khi điện phân dung dịch gồm Cu(NO3)2 0,1 M và AgNO3 0,1 M, quá trình khử đầu tiên xảy ra ở cathode là
\[{\rm{A}}{{\rm{g}}^{\rm{ + }}}\]+ 1e → Ag
\[{\rm{C}}{{\rm{u}}^{{\rm{2 + }}}}\]+ 2e → Cu.
2H2O + 2e → H2 + 2\[{\rm{O}}{{\rm{H}}^{\rm{ - }}}\].
2\[{{\rm{H}}^{\rm{ + }}}\]+ 2e → H2.
Trong công nghiệp, việc tinh chế đồng từ đồng thô được thực hiện bằng phương pháp điện phân dung dịch với anode làm bằng
graphite.
platinum.
thép.
đồng thô.
Điện phân dung dịch chất nào sau đây (dùng điện cực trơ), thu được dung dịch có khả năng làm quỳ tím chuyển sang màu đỏ?
NaBr.
NaCl.
CuSO4.
CuCl2.
Trong quá trình mạ bạc cho một chiếc vòng bằng thép thì ở anode xảy ra quá trình
Ag → \[{\rm{A}}{{\rm{g}}^{\rm{ + }}}\]+ 1e.
Fe → \[{\rm{F}}{{\rm{e}}^{{\rm{2 + }}}}\]+ 2e.
2H2O → 4\[{{\rm{H}}^{\rm{ + }}}\]+ O2 + 4e.
C → \[{{\rm{C}}^{{\rm{4 + }}}}\]+ 4e.
Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Trong công nghiệp, từ nguồn kim loại thô có thể tinh chế kim loại bằng phương pháp điện phân.
a. Nguyên tắc chung để điều chế kim loại là oxi hóa ion kim loại thành kim loại.
b. Trong sự điện phân ở anode xảy ra sự oxi hóa, ở cathode xảy ra sự khử.
c. Các kim loại mạnh như Na, K, Mg, Ca, K… được sản xuất bằng phương pháp điện phân nóng chảy hợp chất ion của chúng.
d. Trong công nghiệp nhôm được sản xuất bằng cách điện phân aluminium oxide nóng chảy.
Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Trong công nghiệp, Al được sản xuất bằng phương pháp điện phân nóng chảy Al2O3. Các phát biểu sau đúng hay sai?
a. Trong thực tế trong quá trình điện phân người ta thêm cryolite để giảm nhiệt độ nóng chảy, tiết kiệm năng lượng.
b. Ở cực âm, xảy ra quá trình: H2O + 2e \[ \to \]2OH–+H2
c. Ở cực dương, xảy ra quá trình: 2O2–\[ \to \] O2 + 4e
d. Phương trình hóa học của phản ứng điện phân:
Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Do \[A{l_2}{O_3}\] có nhiệt độ nóng chảy rất cao \[\left( {2050^\circ C} \right)\] nên \[A{l_2}{O_3}\]được trộn cùng với cryolite \[\left( {N{a_3}Al{F_6}} \right)\] để tạo thành hỗn hợp nóng chảy ở gần \[1000^\circ C.\] Giải pháp này giúp tiết kiệm nhiều năng lượng, đồng thời tạo ra chất lỏng vừa có tính dẫn điện tốt, vừa nổi lên trên Al lỏng để ngăn cách Al lỏng với không khí. Sơ đồ thùng điện phân được biểu diễn như hình dưới đây:
![Do \[A{l_2}{O_3}\] có nhiệt độ nóng chảy rất cao \[\left( {2050^\circ C} \right)\] nên \[A{l_2}{O_3}\]được trộn cùng với cryolite \[\left( {N{a_3}Al{F_6}} \right)\] để tạo thành hỗn hợp nóng chảy ở gần \[1000^\circ C.\] Giải pháp này giúp tiết kiệm nhiều năng lượng, đồng thời tạo ra chất lỏng vừa có tính dẫn điện tốt, vừa nổi lên trên Al lỏng để ngăn cách Al lỏng với không khí. Sơ đồ thùng điện phân được biểu diễn như hình dưới đây: Quá trình điện phân được tiến hành với dòng điện có hiệu điện thế thấp (khoảng 5 V) và cường độ dòng điện 100 – 300 kA. Cho biết: Năng lượng điện tiêu thụ theo lí thuyết: \({{\rm{A}}_{{\rm{lt}}}} = \frac{{{\rm{U}}{\rm{.}}{{\rm{m}}_{{\rm{Al}}}}{\rm{.F}}}}{{{{9.3,6.10}^6}}}{\rm{(kWh) }}\) Trong đó: • mAl: khối lượng Al được điều chế (gam); • F: hằng số Faraday, \[F = 96485{\rm{ }}Cmo{l^{ - 1}};\] • U: hiệu điện thế áp đặt vào hai cực của bình điện phân (V). Hiệu suất tiêu thụ điện năng là 95%. a. Ở anode chỉ có khí \[{O_2}\] thoát ra. b. Năng lượng điện tiêu thụ thực tế để sản xuất được 1 kg Al là 15 kWh. c. Tại cathode xảy ra quá trình khử cation \[A{l^{3 + }}.\] d. Cryolite làm hạ nhiệt độ nóng chảy của \[A{l_2}{O_3},\]do đó giúp tiết kiệm năng lượng tiêu thụ. (ảnh 1)](https://video.vietjack.com/upload2/quiz_source1/2025/07/blobid0-1752416725.png)
Quá trình điện phân được tiến hành với dòng điện có hiệu điện thế thấp (khoảng 5 V) và cường độ dòng điện 100 – 300 kA.
Cho biết: Năng lượng điện tiêu thụ theo lí thuyết:
\({{\rm{A}}_{{\rm{lt}}}} = \frac{{{\rm{U}}{\rm{.}}{{\rm{m}}_{{\rm{Al}}}}{\rm{.F}}}}{{{{9.3,6.10}^6}}}{\rm{(kWh) }}\)
Trong đó:
• mAl: khối lượng Al được điều chế (gam);
• F: hằng số Faraday, \[F = 96485{\rm{ }}Cmo{l^{ - 1}};\]
• U: hiệu điện thế áp đặt vào hai cực của bình điện phân (V).
Hiệu suất tiêu thụ điện năng là 95%.
a. Ở anode chỉ có khí \[{O_2}\] thoát ra.
b. Năng lượng điện tiêu thụ thực tế để sản xuất được 1 kg Al là 15 kWh.
c. Tại cathode xảy ra quá trình khử cation \[A{l^{3 + }}.\]
d. Cryolite làm hạ nhiệt độ nóng chảy của \[A{l_2}{O_3},\]do đó giúp tiết kiệm năng lượng tiêu thụ.
Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. (Đ – S)
Hai nhóm học sinh tiến hành thí nghiệm điện phân dung dịch CuSO4 với một điện cực than chì và một điện cực bằng đồng (bỏ qua sự thay đổi thể tích của dung dịch khi điện phân).
Nhóm 1: Nối điện cực than chì với cực dương và điện cực đồng với cực âm của nguồn điện.
Nhóm 2: Nối điện cực than chì với cực âm và điện cực đồng với cực dương của nguồn điện.
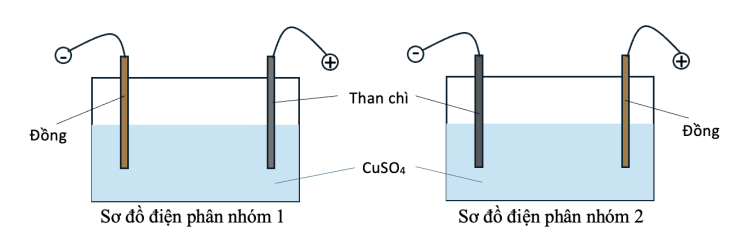
Hai nhóm đều đưa ra giả thuyết sau: trong quá trình điện phân, nồng độ ion Cu2+ giảm dần ứng với màu xanh của dung dịch nhạt dần.
a. Ở nhóm thứ hai, tại anode xảy ra quá trình oxi hoá đồng.
b. Đối với cả hai nhóm đều có kim loại đồng bám vào cathode.
c. Ở nhóm thứ nhất, pH của dung dịch điện phân giảm dần.
d. Giả thuyết đúng với nhóm thứ nhất và sai với nhóm thứ hai.
Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Cho các kim loại sau: Na, Ca, Fe, Al, Zn, Cu, Ag. Có bao nhiêu kim loại được điều chế trong công nghiệp bằng phương pháp điện phân hợp chất nóng chảy của chúng?
Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Điện phân dung dịch CuCl2 trong 1 giờ với dòng điện 5A. Sau điện phân, dung dịch còn CuCl2 dư. Khối lượng Cu đã sinh ra tại cathode của bình điện phân là bao nhiêu gam? (Cho Cu = 64).
Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Cho 2 phản ứng sau:
(1)
(2) \(Z + X \to T + H \uparrow \)
Cho các phát biểu sau về 2 phản ứng trên:
a. Khí H sinh ra nhẹ hơn khí Y.
b. T là một oxide.
c. Y là khí duy trì sự sống.
d. Z là dung dịch chuyển quỳ tím sang màu xanh.
Có bao nhiêu phát biểu là đúng?
Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Để mạ 5,0 g bạc lên một đĩa sắt khi điện phân dung dịch chứa \[{{\rm{[Ag(N}}{{\rm{H}}_{\rm{3}}}{{\rm{)}}_{\rm{2}}}{\rm{]}}^{\rm{ + }}}\]với dòng điện có cường độ 1,5 A không đổi cần thời gian t phút.
Cho biết:
- Quá trình khử tại cathode: + 1e → Ag + 2NH3.
- Điện lượng q = It = ne. F, F = 96 500 C/mol.
Giá trị của t là bao n\[{{\rm{[Ag(N}}{{\rm{H}}_{\rm{3}}}{{\rm{)}}_{\rm{2}}}{\rm{]}}^{\rm{ + }}}\]hiêu? (Làm tròn kết quả đến phần mười).
Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Tiến hành điện phân dung dịch CuSO4 với anode bằng đồng. Để hòa tan 100 g đồng ở anode trong 8 giờ thì cần cường độ dòng điện bằng bao nhiêu ampe? (Làm tròn kết quả đến phần mười).
Câu hỏi trắc nghiệm yêu cầu trả lời ngắn.
Điện phân dung dịch M(NO3)n (điện cực trơ, cường độ dòng điện không đổi), ở cathode chỉ thu được 5,4 g kim loại M và ở anode thu được 0,31 lít khí (đkc). Kim loại M là?

