28 câu trắc nghiệm Hóa 10 Kết nối tri thức Bài 16: Ôn tập chương 4 (Đúng sai - Trả lời ngắn) có đáp án
36 câu hỏi
Số oxi hóa là một số đại số đặc trưng cho đại lượng nào sau đây của nguyên tử trong phân tử?
Hóa trị.
Điện tích.
Khối lượng.
Số hiệu nguyên tử.
Trong hợp chất SO3, số oxi hóa của sulfur (S) là
+2.
+3.
+5.
+6.
Chromium(VI) oxide là chất rắn, màu đỏ thẫm, vừa là acidic oxide, vừa là chất oxi hóa mạnh. Số oxi hóa của chromium (Cr) trong oxide trên là
0.
+6.
+2.
+3.
Ammonia (NH3) là nguyên liệu để sản xuất nitric acid và nhiều loại phân bón. Số oxi hóa của nitrogen (N) trong ammonia là
+3.
–3.
+1.
–1.
Thuốc tím chứa ion permanganate (MnO4–) có tính oxi hóa mạnh, được sử dụng để sát trùng, diệt khuẩn trong y học, đời sống và nuôi trồng thủy sản. Số oxi hóa của manganse trong ion permanganate là
+2.
+3.
+7.
+6.
Trong thiên nhiên manganese (Mn) là nguyên tố tương đối phổ biến, đứng thứ ba trong các kim loại chuyển tiếp, chỉ sau Fe và Ti. Các khoáng vật chính của manganese là hausmanite (Mn3O4), pyrolusite (MnO2), braunite (Mn2O3) và manganite (MnOOH). Manganese tồn tại ở rất nhiều trạng thái số oxi hóa khác nhau từ +2 tới +7.
Cho các chất sau: Mn, MnO2, MnCl2, KMnO4. Số oxi hóa của nguyên tố Mn trong các chất lần lượt là
+2, –2, –4, +8.
0, +4, +2, +7.
0, +4, –2, +7.
0, +2, –4, –7.
Cho một số hợp chất: H2S, H2SO3, H2SO4, NaHS, Na2SO3, SO3, K2S, SO2. Dãy các chất trong đó sulfur (S) có cùng số oxi hóa là
H2S, H2SO3, H2SO4.
H2SO3, H2SO4, Na2SO3, SO3.
H2SO3, H2SO4, Na2SO3, SO2.
H2S, NaHS, K2S.
Dấu hiệu để nhận ra phản ứng là phản ứng oxi hóa – khử dựa trên sự thay đổi đại lượng nào sau đây của nguyên tử?
Số mol.
Số oxi hóa.
Số khối.
Số proton.
Trong phản ứng oxi hóa – khử, chất oxi hóa là chất
nhường electron.
nhận electron.
nhận proton.
nhường proton.
Phản ứng nào sau đây là phản ứng oxi hóa – khử?
2Ca + O2 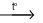 2CaO.
2CaO.
CaCO3 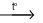 CaO + CO2.
CaO + CO2.
CaO + H2O  Ca(OH)2.
Ca(OH)2.
Ca(OH)2 + CO2  CaCO3 + H2O.
CaCO3 + H2O.
Trong thiên nhiên manganese (Mn) là nguyên tố tương đối phổ biến, đứng thứ ba trong các kim loại chuyển tiếp, chỉ sau Fe và Ti. Các khoáng vật chính của manganese là hausmanite (Mn3O4), pyrolusite (MnO2), braunite (Mn2O3) và manganite (MnOOH). Manganese tồn tại ở rất nhiều trạng thái số oxi hóa khác nhau từ +2 tới +7.
Phản ứng nào sau đây không có sự thay đổi số oxi hóa của nguyên tố Mn?
MnO2 + 4HCl 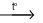 MnCl2 + Cl2 + 2H2O.
MnCl2 + Cl2 + 2H2O.
Mn + O2  MnO2.
MnO2.
2HCl + MnO  MnCl2 + H2O.
MnCl2 + H2O.
6KI + 2KMnO4 + 4H2O  3I2 + 2MnO2 + 8KOH.
3I2 + 2MnO2 + 8KOH.
Carbon đóng vai trò chất oxi hóa ở phản ứng nào sau đây?
C + O2 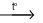 CO2.
CO2.
C + CO2 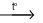 2CO.
2CO.
C + H2O 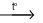 CO + H2.
CO + H2.
C + 2H2 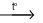 CH4.
CH4.
Nguyên tử sulfur (S) thể hiện tính khử và tính oxi hóa trong chất nào sau đây?
SO3.
SO2.
H2SO4.
H2S.
Chlorine vừa đóng vai trò chất oxi hóa, vừa đóng vai trò chất khử trong phản ứng nào sau đây?
2Na + Cl2 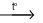 2NaCl.
2NaCl.
H2 + Cl2  2HCl.
2HCl.
2FeCl2 + Cl2 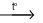 2FeCl3.
2FeCl3.
2NaOH + Cl2  NaCl + NaClO + H2O.
NaCl + NaClO + H2O.
Cho phản ứng hóa học: Fe + CuSO4  FeSO4 + Cu. Trong phản ứng trên xảy ra
FeSO4 + Cu. Trong phản ứng trên xảy ra
sự oxi hóa Fe và sự oxi hóa Cu.
sự khử Fe2+ và sự oxi hóa Cu.
sự oxi hóa Fe và sự khử Cu2+.
sự khử Fe2+ và sự khử Cu2+.
Cho phương trình hóa học:
aAl + bHNO3  cAl(NO3)3 + dNO + eH2O. Tỉ lệ a: b là
cAl(NO3)3 + dNO + eH2O. Tỉ lệ a: b là
1: 3.
2: 3.
2: 5.
1: 4.
Hòa tan hoàn toàn 5,85 gam bột kim loại M vào dung dịch HCl, thu được 0,325 mol khí H2. Kim loại M là
Mg.
Al.
Zn.
Fe.
Đốt cháy hoàn toàn m gam hỗn hợp X gồm Mg và Al cần vừa đủ 3,09875 lít khí O2 (đkc), thu được 9,1 gam hỗn hợp hai oxide. Khối lượng của Mg trong X là
5,1.
2,4.
2,7.
3,9.
a. Số oxi hoá của nguyên tử trong bất kì một đơn chất hoá học nào đều bằng 0
b. Tổng số oxi hoá của tất cả các nguyên tử trong một phân tử và trong một ion đa nguyên tử bằng 0
c. Trong tất cả các hợp chất, hydrogen luôn có số oxi hoá là +1
d. Trong tất cả các hợp chất, oxygen luôn có số oxi hoá là –2
a. I– bị oxi hoá, I trong IO3– bị khử.
b. Số oxi hoá của I trong IO3– là +3
c. IO3– là chất oxi hoá và H2O là chất khử
d. Co2+ là chất oxi hoá.
a. Trong phản ứng trên, số oxi hóa của O giảm từ 0 về –2; của C tăng từ –4 lên +4
b. Trong quá trình oxi hóa, O2 bị oxi hóa từ 0 xuống –2; trong quá trình khử, CH4 bị khử từ –4 lên +4
c. Hệ số cân bằng thu gọn của phản ứng trên lần lượt là 1 : 2 : 1 : 2
d. Khi đốt cháy hoàn toàn 4,958 L khí CH4 (đkc), thì thể tích khí CO2 (đkc) thải ra môi trường là 9,916 L
Cho các phản ứng sau:
(a) SO3 + H2O H2SO4;
(b) CaCO3 + 2HCl CaCl2 + CO2 + H2O;
(c) C + H2O CO + H2;
(d) CO2 + Ca(OH)2 CaCO3 + H2O;
(e) Ca + 2H2O Ca(OH)2 + H2;
(g) 2KMnO4 K2MnO4 + MnO2 + O2.
Số phản ứng oxi hóa – khử là bao nhiêu?
Cho các phản ứng hóa học sau:
(a) CaCO3 CaO + CO2;
(b) CH4 C + 2H2;
(c) 2Al(OH)3 Al2O3 + 3H2O;
(d) 2NaHCO3 Na2CO3 + CO2 + H2O.
Số phản ứng có kèm theo sự thay đổi số oxi hóa của các nguyên tử là bao nhiêu?
Cho các phản ứng sau:
(a) 4HCl + MnO2 MnCl2 + Cl2 + 2H2O.
(b) 2HCl + Fe FeCl2 + H2.
(c) 14HCl + K2Cr2O7 2KCl + 2CrCl3 + 3Cl2 + 7H2O.
(d) 6HCl + 2Al 2AlCl3 + 3H2.
(e) 16HCl + 2KMnO4 2KCl + 2MnCl2 + 5Cl2 + 8H2O.
Số phản ứng trong đó HCl thể hiện tính oxi hóa là bao nhiêu?
Cho phản ứng: FeO + HNO3 Fe(NO3)3 + NO + H2O. Trong phương trình của phản ứng trên, khi hệ số của FeO là 3 thì hệ số của HNO3 là bao nhiêu?
Hòa tan 14 gam Fe trong dung dịch H2SO4 loãng, dư, thu được dung dịch X. Thêm dung dịch KMnO4 1M vào dung dịch X. Biết KMnO4 có thể oxi hóa FeSO4 trong môi trường H2SO4 thành Fe2(SO4)3 và bị khử thành MnSO4. Phản ứng xảy ra hoàn toàn. Tính thể tích dung dịch KMnO4 1M đã phản ứng
Đốt cháy hoàn toàn 2,52 gam hỗn hợp gồm Mg và Al cần vừa đủ 2,479 lít hỗn hợp khí X gồm O2 và Cl2 (đkc), thu được 8,84 gam chất rắn. Xác định số mol electron các chất khử cho và số mol electron các chất oxi hóa nhận trong quá trình phản ứng

