34 câu hỏi
Nguyên tố X có Z = 17. Electron lớp ngoài cùng của nguyên tử nguyên tố X thuộc lớp
K.
L.
M.
N.
Nguyên tố X có Z = 17. Electron lớp ngoài cùng của nguyên tử nguyên tố X thuộc lớp
K.
L.
M.
N.
Nguyên tố Q có số hiệu nguyên tử bằng 14. Electron cuối cùng của nguyên tử nguyên tố Q điền vào lớp, phân lớp nào sau đây?
K, s.
L, p.
M, p.
N, d.
Nguyên tố Q có số hiệu nguyên tử bằng 14. Electron cuối cùng của nguyên tử nguyên tố Q điền vào lớp, phân lớp nào sau đây?
K, s.
L, p.
M, p.
N, d.
Cấu hình electron của nguyên tử 24Cr là
1s22s22p63s23p64s23d4.
1s22s22p63s23p63d44s2.
1s22s22p63s23p63d54s1.
1s22s22p63s23p64s13d5.
Cấu hình electron của nguyên tử 24Cr là
1s22s22p63s23p64s23d4.
1s22s22p63s23p63d44s2.
1s22s22p63s23p63d54s1.
1s22s22p63s23p64s13d5.
Các hạt cấu tạo nên hầu hết các nguyên tử là
electron và proton.
proton và neutron.
neutron và electron.
electron, proton và neutron.
Các hạt cấu tạo nên hầu hết các nguyên tử là
electron và proton.
proton và neutron.
neutron và electron.
electron, proton và neutron.
Nguyên tử của nguyên tố oxygen có 8 electron và 8 neutron. Nguyên tử O có kí hiệu là
A. 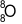 .
.
B.  .
.
C.  .
.
D.  .
.
Nguyên tử của nguyên tố oxygen có 8 electron và 8 neutron. Nguyên tử O có kí hiệu là
\(_8^8O\).
\(_8^{16}O\).
\(_{16}^8O\).
\(_8^{32}O\).
Nguyên tử nào trong các nguyên tử sau đây chứa đồng thời 20 neutron, 19 proton và 19 electron?
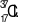
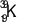


Nguyên tử nào trong các nguyên tử sau đây chứa đồng thời 20 neutron, 19 proton và 19 electron?
\(_{17}^{37}Cl.\)
\(_{19}^{39}K.\)
\(_{18}^{40}Ar.\)
\(_{19}^{40}K.\)
Dãy nào sau đây gồm các đồng vị của cùng một nguyên tố hóa học?
A.  .
.
B.  .
.
C.  .
.
D.  .
.
Dãy nào sau đây gồm các đồng vị của cùng một nguyên tố hóa học?
\(_6^{14}X{\rm{, }}_7^{14}{\rm{Y, }}_8^{14}{\rm{Z}}\).
\(_9^{19}X{\rm{, }}_{10}^{19}{\rm{Y, }}_{10}^{20}{\rm{Z}}\).
\(_{14}^{28}X{\rm{, }}_{14}^{29}{\rm{Y, }}_{14}^{30}{\rm{Z}}\).
\(_{18}^{40}X{\rm{, }}_{19}^{40}{\rm{Y, }}_{20}^{40}{\rm{Z}}\).
Orbital nào sau đây có dạng hình cầu?
s.
px.
py.
pz.
Orbital nào sau đây có dạng hình cầu?
s.
px.
py.
pz.
Lớp electron thứ 2 có bao nhiêu phân lớp?
1.
2.
3.
4.
Lớp electron thứ 2 có bao nhiêu phân lớp?
1.
2.
3.
4.
Nguyên tử O có 8 electron. Biểu diễn sự sắp xếp electron trong nguyên tử O theo orbital nào sau đây là đúng?
A.  .
.
B.  .
.
C.  .
.
D.  .
.
Nguyên tử O có 8 electron. Biểu diễn sự sắp xếp electron trong nguyên tử O theo orbital nào sau đây là đúng?
A. ![]() .
.
B. ![]() .
.
C. ![]() .
.
D. ![]() .
.
Hạt nhân nguyên tử Na có 11 proton và 12 neutron. Số electron trong nguyên tử Na là
12.
11.
23.
22.
Hạt nhân nguyên tử Na có 11 proton và 12 neutron. Số electron trong nguyên tử Na là
12.
11.
23.
22.
Cặp nguyên tử nào sau đây có cùng số neutron?
và  .
.
và 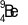 .
.
và  .
.
và  .
.
Cặp nguyên tử nào sau đây có cùng số neutron?
\(_5^{11}B\) và \(_6^{12}C\).
\(_3^7Li\) và \(_4^9Be\).
\(_{12}^{24}Mg\) và \(_{14}^{28}Si\).
\(_7^{14}N\) và \(_8^{16}O\).
Cho nguyên tử R có tổng số hạt cơ bản là 46, số hạt mang điện nhiều hơn số hạt không mang điện là 14. Cấu hình electron của nguyên tử R là
 Cấu hình electron của R: 1s22s22p63s23p3 hoặc [Ne]3s23p3.
Cấu hình electron của R: 1s22s22p63s23p3 hoặc [Ne]3s23p3.
[Ne]3s23p3.
[Ne]3s23p5.
[Ne]3d14s2.
[Ne]4s2.
Đáp án
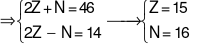
Chọn đáp án A
Cho nguyên tử R có tổng số hạt cơ bản là 46, số hạt mang điện nhiều hơn số hạt không mang điện là 14. Cấu hình electron của nguyên tử R là
[Ne]3s23p3.
[Ne]3s23p5.
[Ne]3d14s2.
[Ne]4s2.
Trong tự nhiên chlorine có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl. Thành phần % theo khối lượng của 37Cl trong HClO4 là
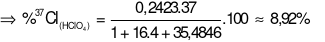
8,43%.
8,79%.
8,92%.
8,56%.
Đáp án
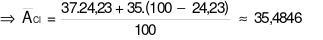
Chọn đáp án C
Trong tự nhiên chlorine có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl. Thành phần % theo khối lượng của 37Cl trong HClO4 là
8,43%.
8,79%.
8,92%.
8,56%.
hổ khối lượng của zirconium được biểu diễn như hình sau đây (điện tích z của các ion đồng vị zirconium đều bằng 1+).
Từ phổ MS ta thấy Zr có 5 đồng vị bền: 90Zr (51,45%), 91Zr (11,22%), 92Zr (17,15%), 94Zr (17,38%) và 96Zr (2,80%)
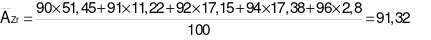
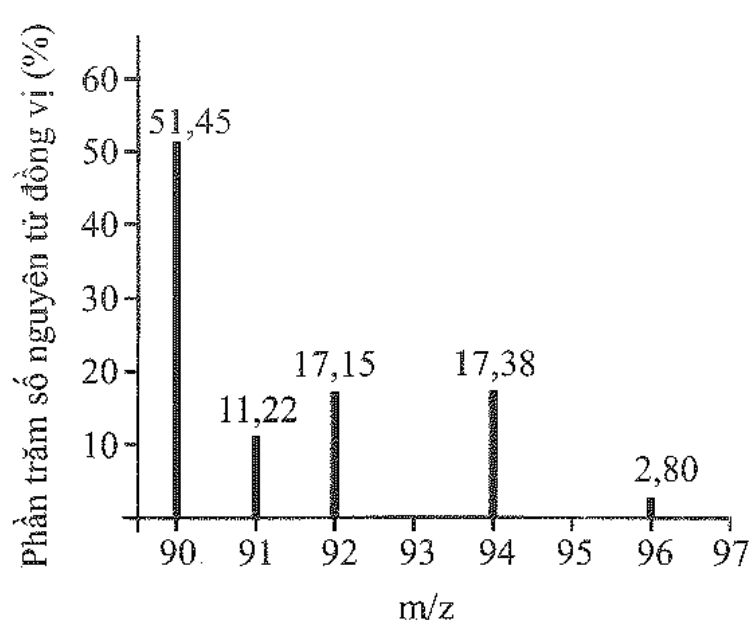
Số lượng đồng vị bền và nguyên tử khối trung bình của zirconium là:
5 đồng vị, nguyên tử khối trung bình bằng 92,60.
5 đồng vị, nguyên tử khối trung bình bằng 91,32.
4 đồng vị, nguyên tử khối trung bình bằng 91,18.
4 đồng vị, nguyên tử khối trung bình bằng 92,00.
Đáp án
Phổ khối lượng của zirconium được biểu diễn như hình sau đây (điện tích z của các ion đồng vị zirconium đều bằng 1+).
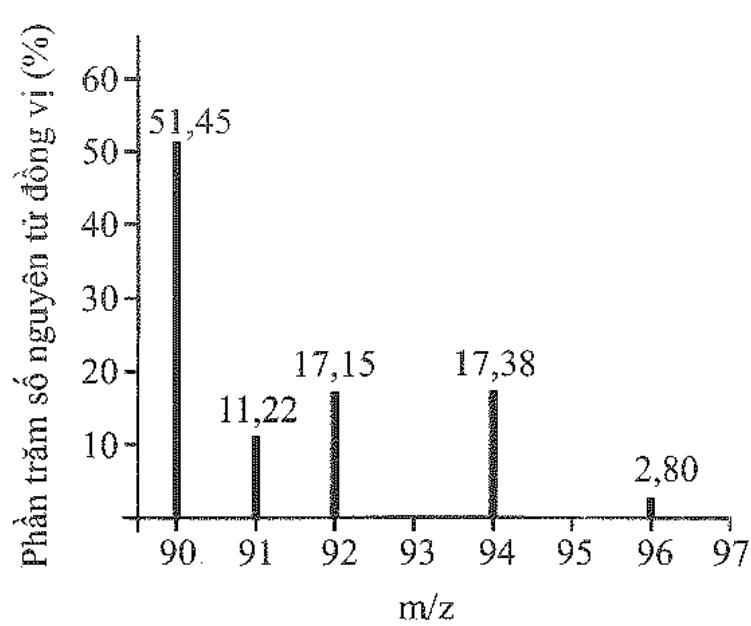 Số lượng đồng vị bền và nguyên tử khối trung bình của zirconium là:
Số lượng đồng vị bền và nguyên tử khối trung bình của zirconium là:
5 đồng vị, nguyên tử khối trung bình bằng 92,60.
5 đồng vị, nguyên tử khối trung bình bằng 91,32.
4 đồng vị, nguyên tử khối trung bình bằng 91,18.
4 đồng vị, nguyên tử khối trung bình bằng 92,00.
Phát biểu nào sau đây là đúng khi nói về nguyên tử?
Trong nguyên tử, số hạt proton luôn bằng số hạt neutron.
Điện tích của một nguyên tử có thể có giá trị âm, dương hoặc bằng 0.
Khối lượng của một nguyên tử (tính theo amu) luôn là số nguyên.
Lớp vỏ nguyên tử tạo nên bởi các electron.
Phát biểu nào sau đây là đúng khi nói về nguyên tử?
Trong nguyên tử, số hạt proton luôn bằng số hạt neutron.
Điện tích của một nguyên tử có thể có giá trị âm, dương hoặc bằng 0.
Khối lượng của một nguyên tử (tính theo amu) luôn là số nguyên.
Lớp vỏ nguyên tử tạo nên bởi các electron.
Cho các phát biểu sau
(a) Những nguyên tử có cùng số electron thuộc cùng một nguyên tố hóa học.
(b) Hai nguyên tử A và B đều có số khối là 14. Vậy hai nguyên tử này thuộc cùng một nguyên tố hóa học.
(c) Những nguyên tử có cùng số neutron thuộc cùng một nguyên tố hóa học.
(d) Hai ion dương (ion một nguyên tử) có điện tích lần lượt là +2 và +3, đều có 26 proton. Vật hai ion này thuộc cùng một nguyên tố hóa học.
Số phát biểu đúng là
3.
2.
4.
1.
Cho các phát biểu sau
(a) Những nguyên tử có cùng số electron thuộc cùng một nguyên tố hóa học.
(b) Hai nguyên tử A và B đều có số khối là 14. Vậy hai nguyên tử này thuộc cùng một nguyên tố hóa học.
(c) Những nguyên tử có cùng số neutron thuộc cùng một nguyên tố hóa học.
(d) Hai ion dương (ion một nguyên tử) có điện tích lần lượt là +2 và +3, đều có 26 proton. Vật hai ion này thuộc cùng một nguyên tố hóa học.
Số phát biểu đúng là
3.
2.
4.
1.
